Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
Коагулационни факториEsperoct
Резюме на наркотиците
Какво е Esperoct?
Esperoct [антихемофилен фактор (рекомбинант) гликопегилиран-exei] е a коагулация Концентрат на фактор VIII, показан за употреба при възрастни и деца с хемофилия А за лечение при поискване и контрол на епизодите на кървене Периоперативно управление на кървенето и рутинната профилактика за намаляване на честотата на епизодите на кървене. Esperoct не е посочен за лечение на болест на фон Уилебранд.
Какви са страничните ефекти на Esperoct?
Esperoct Topper
- кошери
- затруднено дишане
- Подуване на лицето ви устни Език или гърло
- сърбеж
- обрив
- изтръпване
- изтръпване
- треска
- замаяност
- гадене
- Бързи сърдечни удари
- стягане на гърдите
- хрипове
- Бледа кожа
- Студена пот
- Лекоглавия
- припадък
- Повишени епизоди на кървене
- всяко кървене, което няма да спре и
- Болки в гърдите
Получете медицинска помощ веднага, ако имате изброени по -горе симптоми.
Общите странични ефекти на Esperoct включват:
- обрив
- зачервяване
- сърбеж и
- Реакции на инжекционното място
Потърсете медицинска помощ или се обадете на 911 наведнъж, ако имате следните сериозни странични ефекти:
- Сериозни симптоми на очите, като например внезапна загуба на зрение, замъглено зрение Тунел Виждане болка в очите или подуване или виждане на ореоли около светлините;
- Сериозни сърдечни симптоми като бързи нередовни или ударни сърдечни удари; трептене в гърдите ви; задух; и внезапна замаяност замаяност или раздаване;
- Тежка главоболие объркване затънала речева ръка или крак слабост проблем за ходене на загуба на координация, чувствайки се нестабилни много твърди мускули висока треска обилно изпотяване или тремор.
Този документ не съдържа всички възможни странични ефекти, а други могат да възникнат. Консултирайте се с вашия лекар за допълнителна информация за страничните ефекти.
Дозировка за Esperoct
Дозата на Esperoct зависи от използването.
Какви лекарства вещества или добавки взаимодействат с Esperoct?
Esperoct може да взаимодейства с други лекарства. Кажете на Вашия лекар всички лекарства и добавки, които използвате.
Есперокт по време на бременност или кърмене
Кажете на Вашия лекар, ако сте бременна или планирате да забременеете, преди да използвате Esperoct; Не е известно как би се отразил на плода. Не е известно дали Есперокт преминава в кърма или ще се отрази на кърмаче за кърмене. Консултирайте се с Вашия лекар преди кърмене.
Допълнителна информация
Нашият Esperoct [антихемофилен фактор (рекомбинантно) гликопегилиран-exei] лиофилизиран прах за разтвор за интравенозна употреба Страничен център лекарствен център предоставя цялостен поглед върху наличната информация за лекарството върху потенциалните странични ефекти при приемането на това лекарство.
Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Странични ефекти
- Предупреждения
- Предозиране
- Клинична фармакология
- Ръководство за лекарства
Описание за Esperoct
Esperoct е непирогенен лиофилизиран прах без стерилен консервант за интравенозна инжекция след възстановяване с предоставения разредител с физиологичен разтвор. Активната съставка в Esperoct е рекомбинантен аналог на човешкия коагулационен фактор VIII (FVIII), конюгиран с 40-kDa полиетилен гликол (PEG) молекула. Esperoct е формулиран със следните помощни вещества: натриев хлорид L-хистидин захароза полисорбат 80 L-метионин и калциев хлорид.
Активността на FVIII в Esperoct се определя с помощта на хромогенния анализ, описан в европейската фармакопея. Присвояването на дейността използва референтен материал на FVIII, който е проследен за настоящия Международен стандарт на Световната здравна организация (СЗО) за концентрат на FVIII и оценен от подходящи методологии, за да се гарантира точността на резултатите. Esperoct се предлага във флакони с една доза, които съдържат номинално 500 1000 1500 2000 или 3000 IU на FVIII. Всеки флакон с есперокт е обозначен с действителната активност на FVIII. След възстановяване с доставения разредител (NULL,9% физиологичен разтвор) всеки ml от разтвора съдържа приблизително 125 250 375 500 или 750 IU съответно FVIII.
FVIII протеинът в Esperoct се произвежда в клетките на яйчниците на китайски хамстер (CHO), използвайки рекомбинантна ДНК технология и съдържа пресечен В домейн, който е O-гликозилиран. Полипептидната част на молекулата има молекулна маса 166 kDa (изчислена с изключение на пост-транслационни модификации) и представлява хетеродимер на тежка верига и лека верига, които се държат заедно чрез нековалентни взаимодействия. Рекомбинантният FVIII протеин се пречиства с помощта на серия от хроматографски стъпки, един от които е афинитетна хроматография с използването на моноклонално антитяло за селективно изолиране на RFVIII от средата на клетъчната култура. 40-kDa PEG молекулата е конюгирана с O-гликановата част на В домейна, използвайки ензимна реакция за получаване на гликопегилиран FVIII (FVIII-PEG). Процесът на пречистване включва два етапа на вирусен клирънс, а именно лечение с детергент (Triton X-100) за инактивиране на обвити вируси и 20-nm филтрация за отстраняване на обвити и неразвити вируси. Не се използват добавки от човешки или животински произход по време на производствения процес и формулирането на Esperoct.
В кръвообращението, когато FVIII-PEG се активира чрез тромбин, частта от В-домейн с прикрепената PEG част се разцепва и получената активирана FVIII (FVIIIA) е сходна по структура и функция на родния FVIIIA.
Използване за Esperoct
Esperoct ® [Антихемофилен фактор (рекомбинант) гликопегилиран- exei] е рекомбинантен коагулационен фактор, получен от ДНК, показан за употреба при възрастни и деца с хемофилия А за:
- Лечение при поискване и контрол на епизодите на кървене
- Периоперативно управление на кървенето
- Рутинна профилактика за намаляване на честотата на епизодите на кървене
Ограничение на употребата
Esperoct ® не е посочен за лечение на болест на фон Уилебранд. (1)
Дозировка за Esperoct
За интравенозна инфузия само след разтваряне.
Доза
- Дозировката и продължителността на лечението зависят от тежестта на дефицита на фактор VIII от местоположението и степента на кървене и от клиничното състояние на пациента. Необходим е внимателно наблюдение на заместващата терапия в случаи на голяма операция или животозастрашаващи епизоди на кървене.
- Всеки флакон с есперокт ® Съдържа обозначеното количество рекомбинантен фактор VIII в международните звена (IU). Един IU от фактор VIII активност съответства на количеството на фактор VIII в един милилитър от нормална човешка плазма. Изчисляването на необходимата доза на фактор VIII се основава на емпиричната констатация, че един IU от фактор VIII на kg телесно тегло повишава активността на плазмения фактор VIII от два IU/DL.
Лечение с помощ и контрол на епизодите на кървене
Таблица 1 може да се използва за насочване на дозиране на есперокт ® За лечение на епизоди на кървене.
Таблица 1: Дозиране на есперокт ® За контрол на епизодите на кървене
| Вид кървене | Юноши/ възрастни ≥12 години Доза (IU/kg) | Деца <12 years Доза (IU/kg) | Допълнителни дози |
| Минор | |||
| Ранна хемартроза леко кървене от мускули или орално кървене | 40 | 65 | Една доза трябва да е достатъчна |
| Умерен | |||
| По -обширно хемартрозно мускулно кървене или хематом | 40 | 65 | След 24 часа може да се прилага допълнителна доза |
| Основен | |||
| Живот или животозастрашаващи кръвоизливи стомашно-чревни кървящи интракраниални интраабдоминални или интраторакални кървящи фрактури | 50 | 65 | Допълнителна доза (и) може да се прилага приблизително на всеки 24 часа |
Периоперативно управление
Нивото на дозата и интервалите на дозиране за операция зависят от процедурата и местната практика. Ръководство за дозиране с Esperoct ® По време на операцията (периоперативно управление) е дадена в таблица 2 по -долу.
Таблица 2: Дозиране за периоперативно управление с Esperoct ®
| Вид операция | Юноши/ възрастни ≥12 години Pre-operative Доза (IU/kg) | Деца <12 years Pre-operative Доза (IU/kg) | Допълнителни дози |
| Минор | |||
| Включително извличане на зъби | 50 | 65 | Допълнителна доза (и) може да се прилага след 24 часа, ако е необходимо |
| Основен | |||
| Интракраниална интраабдоминална интраторакална или ставна заместителна операция | 50 | 65 | Допълнителни дози can be administered approximately every 24 hours for the first week и then approximately every 48 hours until wound healing has occurred |
Рутинна профилактика
Възрастни и юноши (≥ 12 години): Препоръчителната начална доза е 50 IU от Esperoct ® на kg телесно тегло на всеки 4 дни.
Този режим може да бъде индивидуално коригиран до по -малко или по -чести дозирани въз основа на епизодите на кървене.
Деца ( <12 years): A dose of 65 IU of Esperoct ® на kg телесно тегло два пъти седмично. Този режим може да бъде индивидуално коригиран до по -малко или по -чести дозирани въз основа на епизодите на кървене.
Dosage (IU) = телесно тегло (kg) × желания фактор VIII увеличение (IU/dl или % нормално) × 0,5
- Esperoct ® също може да бъде дозирана за постигане на специфично ниво на активност на целевия фактор VIII в зависимост от тежестта на хемофилията за лечение по поискване/контрол на епизодите на кървене или периоперативно управление. За да постигнете специфичен целеви фактор VIII ниво на активност, използвайте следната формула:
- Основата на дозата и честотата на есперокт ® относно индивидуалния клиничен отговор. Пациентите могат да варират в своите фармакокинетични и клинични отговори.
- Ако се извършва мониторинг на фактор VIII активност, използвайте хромогенен или едноетапен анализ на съсирването, подходящ за използване с есперокт ® [Вижте Предупреждения и предпазни мерки ].
Подготовка и възстановяване
- Винаги измийте ръцете и се уверете, че зоната е чиста, преди да извършите процедурите за възстановяване.
- Използвайте асептична техника по време на процедурите за възстановяване.
- Ако дозата изисква повече от един флакон с есперокт ® на инфузия възстановете всеки флакон съгласно следните инструкции.
Преглед на Esperoct ® Пакет
Преглед
Флакон с есперокт ® прах
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct.webp' > |
Възстановяване
| ® vial and the pre-filled diluent syringe to room temperature. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-1.webp' > |
| ® vial. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-2.webp' > |
 |
| ® флакон на плоска и плътна повърхност. Докато държите защитната капачка, поставете флаколния адаптер над есперокта ® vial and press down firmly on the protective cap until the vial adapter spike penetrates the rubber stopper. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-4.webp' > |
 |
 |
 |
 |
 |
| ® vial until all of the powder is dissolved. Avoid shaking the vial and foaming the solution. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-10.webp' > |
- Донесете есперокта ® флакон и предварително запълнената спринцовка на разреждащи се до стайна температура.
- Извадете пластмасовата капачка от Esperoct ® флакон.
- Избършете гумената запушалка върху флакона със стерилен алкохолен тампон и оставете да изсъхне преди употреба.
- Извадете защитната хартия от адаптера на флакона. Не премахвайте адаптера на флакона от защитната капачка.
- Поставете Есперокт ® флакон на плоска и плътна повърхност. Докато държите защитната капачка, поставете флаколния адаптер над есперокта ® Флаконът и натиснете здраво върху защитната капачка, докато скокът на адаптера на флакона проникне в гумената запушалка.
- Внимателно отстранете защитната капачка от адаптера на флакона.
- Хванете буталото, както е показано на диаграмата. Прикрепете буталото към спринцовката, като държите буталния прът до широкия горен край. Включете буталовата пръчка по посока на часовниковата стрелка в гуменото бутало във вътрешността на предварително запълнената спринцовка за разреждане, докато се усети устойчивост.
- Откъснете капачката на спринцовката от предварително запълнената спринцовка за разреждане, като щракнете перфорацията на капачката.
- Свържете предварително запълнената спринцовка за разреждане към адаптера на флакона, като го завъртите по посока на часовниковата стрелка, докато не бъде закрепена.
- Натиснете буталото, за да инжектирате бавно всички разредители във флакона.
- Без да премахвате спринцовката, леко завъртете есперокта ® флакон, докато целият прах не се разтвори. Избягвайте да разтърсите флакона и да пените разтвора.
Администрация
Само за интравенозна инфузия
- Парентералните лекарствени продукти трябва да се проверяват визуално за прахови частици и обезцветяване преди прилагането, когато разтворът и контейнерът разреши. Решението трябва да е ясно и да няма частици. Не използвайте, ако се наблюдават прахови частици или обезцветяване.
- Не администрирайте Esperoct ® в същата тръба или контейнер с други лекарствени продукти.
- Администрирайте Esperoct ® разтвор незабавно. Ако не съхранява разтвора във флакона с адаптера за флакона и прикрепената спринцовка. Използвайте Esperoct ® в рамките на 4 часа, когато се съхранява при ≤86 ° F (30 ° C) или в рамките на 24 часа, когато се съхранява в хладилник при 36 ° F до 46 ° F (2 ° C до 8 ° C).
| ® vial and slowly draw the solution into the syringe. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-11.webp' > |
- Обърнете есперокта ® Флаконът и бавно начертайте разтвора в спринцовката.
- Отделете спринцовката от адаптера с флакона, като завъртите спринцовката обратно на часовниковата стрелка.
- Прикрепете спринцовката към Luer края на инфузионен игла.
- Вливат възстановения есперокт ® интравенозно бавно над приблизително 2 минути.
- След инфузия безопасно изхвърлете спринцовката с инфузията, задайте флакона с флаконен адаптер, който е неизползван есперокт ® и други отпадъчни материали.
Внимание
Предварително напълнената спринцовка за разреждане е направена от стъкло с вътрешен диаметър на върха 0,037 инча и е съвместима със стандартен конектор Luer-Lock.
Някои безобразими конектори за интравенозни катетри са несъвместими със стъклените разредителни спринцовки (например определени конектори с вътрешен шип като Клав ® /Микроклав ® Invision-plus ® Invision-plus CS ® Invision-Plus Junior ® Bionector ® ) и тяхното използване може да повреди конектора и да повлияе на администрирането. Да администрира Esperoct ® Чрез несъвместими конектори без игли изтеглете възстановения продукт в стандартна 10 ml стерилна пластмасова спринцовка с Luer-Luer.
Колко се доставя
Дозирани форми и силни страни
Esperoct ® се предлага като стерилен бял до бял лиофилизиран прах, доставен във флакони с една доза, съдържащи номинално 500 1000 1500 2000 или 3000 IU. Действителната активност на FVIII се отпечатва на всеки есперокт ® флакон и картонена опаковка.
След възстановяване с 4 ml разредител с физиологичен разтвор, разтвореният разтвор съдържа приблизително 125 250 375 500 или 750 IU на ml есперокт ® съответно.
- Esperoct ® се доставя в пакети, състоящи се от флакон с една доза, съдържащ номинално 500 1000 1500 2000 или 3000 IU на фактор VIII активност; Mixpro ® Предварително напълнена спринцовка за разреждане, съдържаща 0,9% физиологичен разтвор; и стерилен флакон адаптер с 25-микрометров филтър, който служи като безгласно устройство за възстановяване.
- Действителната активност на фактор VIII в IU се посочва на всеки есперокт ® Картотон и етикет за флакон.
Таблица 9: Esperoct ® Презентации
| Номинална сила на дозата | Цвят индикатор на капачката | Картон NDC Номер | Компоненти |
| 500 IU | Червено | NDC 0169 8500 01 |
|
| 1000 IU | Зелено | NDC 0169 8100 01 |
|
| 1500 IU | Сиво | NDC 0169 8150 01 |
|
| 2000 IU | Жълто | NDC 0169 8200 01 |
|
| 3000 IU | Черно | NDC 0169 8300 01 |
|
| IU = международни единици |
- Есперокт ® Флаконите са изработени от стъкло, затворено със запушалка на хлоробутил (не е направена с естествен гумен латекс) и се запечатва с алуминиева капачка.
- Предварително напълнените разредителни спринцовки са изработени от стъкло със силиконизиран бутало с бромобутил (не е направено с гумен латекс).
- Затворените флакони и предварително напълнените спринцовки на разреждания са оборудвани с очевидна капачка за срълване, която е изработена от полипропилен.
Съхранение и обработка
- Съхранявайте Esperoct ® В оригиналния пакет за защита на Esperoct ® флакон от светлина.
- Съхранявайте Esperoct ® В прахообразна форма под хладилник при 36 ° F до 46 ° F (2 ° C до 8 ° C) за до 30 месеца от датата на производство до изтичането на датата на изтичане на етикета. По време на 30-месечния срок на срока Esperoct ® Може да се поддържа при стайна температура:
- до 86 ° F (30 ° C) за не повече от 12 месеца или
- до 104 ° F (40 ° C) за не повече от 3 месеца
- Запишете датата на картонената кашон, когато продуктът е отстранен от хладилника. Не връщайте продукта в хладилника.
- Не замразявайте Есперокт ® .
- Използвайте чакане ® в рамките на 4 часа след възстановяване, когато се съхранява при ≤86 ° F (30 ° C) или в рамките на 24 часа, когато се съхранява в хладилника. Съхранявайте възстановения продукт във флакона.
- Изхвърлете всеки неизползван възстановен продукт.
Произведено от: Novo Nordisk A/S DK-2880 BAGSVAERD DENMARD. Ревизиран: септември 2022 г.
IV течности за странични ефекти на дехидратация
Странични ефекти за Esperoct
Най -често съобщаваните нежелани реакции (честота ≥1%) в клиничните изпитвания са сърбеж на необмислено зачервяване (сърбеж) и реакции на инжекционното място.
Опит с клинични изпитвания
Тъй като клиничните изпитвания се провеждат при широко различни състояния, нежелани реакционни проценти, наблюдавани при клиничните изпитвания на лекарство, не могат да бъдат пряко сравнени с процентите в клиничните изпитвания на друго лекарство и може да не отразяват процентите, наблюдавани в клиничната практика.
Безопасността на Есперокт ® е оценен при 270 лица (202 юноши/възрастни и 68 деца) при пет проспективни многоцентрови клинични проучвания при пациенти, лекувани преди това (PTP) с тежка хемофилия А ( <1% endogenous Facдаr VIII activity) и no hisдаry of inhibiдаrs. All subjects received at least one dose of Esperoct ® . По -рано лекуваният пациент е дефиниран като обект с анамнеза за поне 150 дни на експозиция на други продукти на фактор VIII (субекти за юноши/възрастни) или 50 дни на експозиция на други продукти на фактор VIII (педиатрични субекти). Обща експозиция на Esperoct ® бяха 80425 дни на експозиция, съответстващи на 889 години на лечение на пациентите.
По време на клиничните изпитвания в нежеланите реакции на PTPS се появяват със скорост 0,10 събития на пациентна година на експозиция. Най -често съобщаваните нежелани реакции са реакцията на обрив (NULL,2%) инжекционно място (NULL,6%) зачервяване (NULL,9%) и сърбеж (сърбеж) (NULL,5%).
Имуногенност
Субектите се наблюдават за неутрализиране и не-неутрализиращи антитела, за да фактор VIII полиетилен гликол (PEG) и CHO-гостоприемния клетъчен протеин. Един по -рано лекуван субект разработен потвърждава неутрализиращи антитела към фактор VIII (13.5 Bethesda единици). В допълнение два субекта имат преходно ниско титър FVIII антитяло ( <5 Bethesda Units) test results at a single occasion. Anti-PEG antibodies of no clinical consequence were detected in 45 subjects 32 of whom had pre-existing anti-PEG antibodies. Nine subjects developed anti-CHO host cell protein antibodies of no clinical consequence.
Откриването на антитела е силно зависимо от чувствителността и специфичността на анализа. Освен това наблюдаваната честота на антитялото (включително неутрализиращото антитяло) положителност в анализ може да бъде повлияна от няколко фактора, включително анализ на методологията на пробата за обработка на проби от проби за събиране на проби, съпътстващи лекарства и основно заболяване.
Опит за постмаркетиране
Следните нежелани реакции са идентифицирани по време на след одобрение на есперокт ® . Тъй като тези реакции се отчитат доброволно от популация с несигурен размер, не винаги е възможно надеждно да се оцени тяхната честота или да се установи причинно -следствена връзка с експозицията на лекарства.
Намалена активност на фактор VIII: Има съобщения за намалена активност на фактор VIII при липса на откриваем фактор VIII инхибитори при лекувани преди това пациенти (PTPS) при преминаване към есперокт ® От други продукти на фактор VIII.
Лекарствени взаимодействия за Esperoct
Не е предоставена информация
Предупреждения за Esperoct
Включени като част от 'ПРЕДПАЗНИ МЕРКИ' Раздел
Предпазни мерки за Esperoct
Реакции на свръхчувствителност
Алергични реакции на свръхчувствителност, включително анафилаксия, са възможни с есперокт ® . Продуктът съдържа следи от хамстерни протеини, които при някои пациенти могат да причинят алергични реакции [виж Описание ]. Early signs of allergic reactions which can progress да anaphylaxis may include angioedema стягане на гърдите затруднено дишане хрипове обрив кошери и сърбеж. Observe patients for signs и sympдаms of acute hypersensitivity reactions particularly during the early phases of exposure да the product. Discontinue use of Esperoct ® ако възникнат алергични или анафилактични реакции и инициират подходящо лечение.
Неутрализиране на антитела
Образуването на неутрализиращи антитела (инхибитори) към фактор VIII е възникнало след прилагане на есперокт ® . Следете пациентите за развитието на фактор VIII инхибитори чрез подходящи клинични наблюдения и лабораторни тестове. Ако се очаква фактор VIII активност на плазмата не се постига или ако кървенето не се контролира след есперокт ® Прилагането подозира наличието на инхибитор (неутрализиращо антитяло) [виж Мониторинг на лабораторни тестове ].
Мониторинг на лабораторни тестове
Ако се извършва мониторинг на фактор VIII, използвайте хромогенен или едноетапен анализ на съсирването, подходящ за използване с есперокт ® [Вижте Доза и приложение ].
Нивата на активност на фактор VIII могат да бъдат повлияни от вида на активирания частичен реагент на време за тромбопластин (APTT), използван в анализа. Някои реагенти на APTT на базата на силициев диоксид могат да подценяват активността на Esperoct ® с до 60%; Други реагенти могат да надценят активността с 20%. Ако подходящ едноетапна съсирване или хромогенен анализ не е наличен локално, тогава използвайте референтна лаборатория.
Ако кървенето не се контролира с препоръчителната доза Esperoct ® или ако очакваните нива на активност на фактор VIII в плазмата не се постигат, тогава извършват анализ на BethesDA, за да определите дали са налице фактор VIII инхибитори.
Информация за консултирането на пациентите
Съветвайте пациентите:
- За да прочетете одобреното от FDA етикетиране на пациента ( Информация за пациента и Инструкции за употреба ).
- Че реакциите на свръхчувствителност на алергичен тип или анафилаксия са възможни с използването на есперокт ® . Информирайте пациентите за ранните признаци на реакции на свръхчувствителност, включително обриви на кошерите, които сърбеж на подуване на лицето на гърдите и хрипове. Посъветвайте пациентите да преустановят употребата на Esperoct ® незабавно и се свържете с техния доставчик на здравни грижи и/или потърсете спешна помощ незабавно, ако се появят тези симптоми.
- Да се свържат с техния доставчик на здравни грижи или лечебно заведение за по -нататъшно лечение и/или оценка, ако изпитват липса на клиничен отговор на фактор VIII заместваща терапия, тъй като това може да бъде проява на инхибитор.
Неклинична токсикология
Канцерогенеза мутагенеза Нарушаване на плодовитостта
Не са извършени мутагенеза на карциногенезата и увреждане на изследванията на плодовитостта при животни.
Използване в конкретни популации
Бременност
Обобщение на риска
Няма данни с Esperoct ® Използвайте при бременни жени, за да определите дали има риск, свързан с наркотици. Изследванията за възпроизвеждане на животни не са проведени с Esperoct ® . Не е известно дали Есперокт ® може да причини вреда на плода, когато се прилага на бременна жена или може да повлияе на плодовитостта.
В американското общо население прогнозният основен риск от основни вроден дефект и miscarriage in clinically recognized pregnancies is 2–4% и 15–20% съответно.
Лактация
Обобщение на риска
Няма информация относно наличието на Esperoct ® В човешкото мляко ефектът върху кърменото бебе и ефектите върху производството на мляко. Ползите за развитие и здравето от кърменето трябва да се разглеждат заедно с клиничната нужда на майката от есперокт ® и any potential adverse effects on the breastfed infant from Esperoct ® или от основното състояние на майката.
Педиатрична употреба
Безопасността и ефикасността са оценени при 93 лекувани по -рано педиатрични пациенти <18 years of age who received at least one dose of Esperoct; all received routine prophylaxis [Вижте Клинични изследвания ]. Thirty-four (34) of these subjects (36.6%) were 1 до <6 years of age; 34 subjects (36.6%) were 6 до <12 years of age; и 25 subjects (27%) were 12 до <18 years of age. Pharmacokinetic parameters were evaluated for 27 of these subjects who were treated with Esperoct ® [Вижте Клинична фармакология ].
Няма разлика в профила на безопасност на Esperoct ® се наблюдава между по -рано лекувани педиатрични субекти и възрастни субекти. Фармакокинетични изследвания при деца <12 years of age demonstrated higher clearance a shorter half-life и lower incremental recovery of Facдаr VIII compared да adults but the pharmacokinetic parameters are comparable between young children (1– <6 years) и older children (6- <12 years). Because clearance (per kg body weight) is higher in children ( <12 years) a higher dose и more frequent dosing may be needed in this population [Вижте Клинична фармакология ].
Гериатрична употреба
Клинични проучвания на есперокт ® не включва достатъчен брой субекти на възраст 65 години и повече, за да определи дали реагират по различен начин от по -младите лица. Други отчетени клиничен опит не са установили разлики в отговорите между възрастни и по -млади пациенти. Като цяло изборът на доза за възрастен пациент трябва да бъде предпазлив, обикновено като се започне от ниския край на обхвата на дозиране, отразяващ по -голямата честота на намалената чернодробна бъбречна или сърдечна функция и на съпътстваща болест и друга лекарствена терапия.
Информация за предозиране за Esperoct
Не е предоставена информация
Противопоказания за Esperoct
Esperoct ® е противопоказано при пациенти, които са познати свръхчувствителност към есперокт ® или неговите компоненти (включително протеини за хамстери) [виж Предупреждения и предпазни мерки и Описание ].
Клинична фармакология for Esperoct
Механизъм на действие
Esperoct ® Гликопегилирана форма на рекомбинантния анти-хемофилен фактор временно замества липсващия коагулационен фактор VIII, необходим за ефективна хемостаза при вродена пациенти с хемофилия А. Фактор VIII в Есперокт ® се конюгира с 40-kDa полиетилен гликол молекула, която увеличава полуживота и намалява клирънса в сравнение с непегилираната молекула.
Фармакодинамика
Администрацията на Есперокт ® Увеличава плазмените нива на фактор VIII и временно може да коригира дефекта на коагулацията при пациенти с хемофилия А, отразено от намаляване на активираното частично време на тромбопластин (APTT).
Фармакокинетика
Всички фармакокинетични изследвания с Esperoct ® са проведени при по -рано лекувани лица с тежка хемофилия А (фактор VIII <1%). In даtal 129 single-dose pharmacokinetic profiles of Esperoct ® са оценени при 86 лица (включително 24 педиатрични лица 1– <12 years).
Таблица 3 показва данни за субекти, които всеки са получили по една доза от 50 IU/kg. Плазмените проби бяха анализирани с помощта на едноетапния анализ на съсирването. Имаше тенденция за увеличаване на постепенното възстановяване и AUC и намаляването на клирънса с възрастта.
Таблица 3: Еднодози PK параметри на Esperoct ® 50 IU/kg по възраст, използвайки едноетапен анализ на съсирването (геометрична средна стойност (CV%))
| PK параметър | 1 до <6 years | 6 до <12 years | 12 до <18 years | > 18 години |
| Брой на субектите | N = 12 | N = 10 | N = 3 | N = 42 |
| Брой профили | 12 | 10 | 5 | 78 |
| Ir (iu / d d d di) на i / kg) a | 1.82 (32) | 1.67 (22) | 2.45 (16) | 2.53 (24) |
| Възстановяване на FVIII (IU/DL) a | 103.2 (27) | 98.7 (18) | 117.7 (14) | 130.4 (26) |
| t 1/2 (Часове) | 14.7 (27) | 13.8 (32) | 17.4 (39) | 21.7 (33) |
| Aucinf (iu*hour/dl) | 2305 (42) | 2197 (38) | 3063 (40) | 4110 (38) |
| CL (ml/час/kg) | 2.4 (42) | 2.7 (42) | 1.6 (39) | 1.2 (34) |
| VSS (ml/kg) | 44.2 (25) | 47.3 (28) | 36.4 (12) | 37.3 (26) |
| MRT (часове) | 18.1 (27) | 17.8 (35) | 23.4 (43) | 27.4 (28) b |
| PK параметрите са представени в геометрична средна стойност. Съкращения: IR = инкрементално възстановяване; t 1/2 = терминален полуживот; AUC = площ под времевия профил на активността на FVIII; Cl = клирънс; Vss = обем на разпределение в стационарно състояние; MRT = средно време за пребиваване; Cv% = коефициент на вариация a Възстановяването на IR и FVIII бяха оценени 30 минути след дозиране 50 IU/kg за пациенти ≥12 години и 60 минути след дозиране 50 IU/kg (първа извадка) за деца <12 years. bCalculation based on 64 profiles. |
В оценката на PK с една доза при възрастни лица, чийто индекс на телесна маса (ИТМ) варира от 17-35 кг/м 2 Забелязани са разлики за лица, които са с наднормено тегло (BMI 25 - <30 kg/m 2 ) и затлъстяване (ИТМ 30 - <35 kg/m 2 ). Incremental recovery was increased by approximately 17% и 41% AUC was increased by approximately 10% и 27% и clearance was decreased by approximately 8% и 23% respectively all in comparison да those subjects with BMI <25 kg/m 2 . Няма достатъчно данни, които да препоръчат специфични корекции на дозата за пациенти с наднормено тегло и затлъстяване. Дозата може да бъде коригирана при необходимост по преценка на предписващия лекар.
Наблюдавани нива на плазмен фактор VIII преди дозата (корито) и след дозата (пик) в стационарно състояние по време на профилактично лечение с есперокт ® са представени в таблица 4 чрез режим на доза и възрастов диапазон.
Таблица 4: Стационарно корито и върхова плазмена активност на FVIII по хромогенен анализ на възрастта и дозата (геометрична средна стойност [95% CI])
Можете ли да отрежете оксикодон наполовина
| Доза Regimen | 60 IU/kg два пъти седмично ** (50–75 IU/kg) | 50 IU/KG Q4D* | 75 IU/KG Q7D* | |||
| Възрастов диапазон | <6 years | 6- <12 years | 12-- <18 years | ≥18 години | 12-- <18 years | ≥18 години |
| Не. Пациенти | N = 31 | N = 34 | N = 23 | N = 143 | N = 6 | N = 29 |
| Trough iu/dl | 1.2 (0.8; 1.6) | 2.0 (1.5; 2.7) | 2.7 (1.8; 4.0) | 3.0 (2.6; 3.5) | 0.6 (0.2; 1.6) | 1.3 (0.9; 2.0) |
| Peak IU/DL | 125.0 (118.7; 131.6) | 143.3 (136.8; 150.2) | 125.1 (116.0; 135.0) | 137.9 (133.9; 142.2) | 198.0 (166.8; 235.2) | 197.9 (184.9; 212.7) |
| *Данни, включени в анализа: подрастващи/възрастни основна фаза до посещение 8 (края на основната фаза) 50 IU/kg Q4D и удължаване 1 за 75 IU/kg Q7D. В анализите са включени само измервания, събрани в стационарно състояние за дадената лечение с профилактика. ** Данни, включени в анализа: Педиатрична основна фаза 60 IU/kg (50–75 IU/kg) два пъти седмично. В анализите са включени само измервания, събрани в стационарно състояние за дадената лечение с профилактика. |
Време на фактор VIII активност над 5%
Профилите на активността на фактор VIII за стационарно състояние бяха оценени с помощта на модел с едно отделение с елиминиране от първи ред с PK параметри на клирънс (CL) и обем на разпределение (Таблица 5). Фармакокинетичните прогнози показват, че при всички възрастови групи пациентите дозират два пъти седмично (интервал на дозиране, редуващ се между 3 и 4 дни) или Q4D, ще бъде над 5% фактор VIII активност (т.е. в обхвата на лека хемофилия) през по -голямата част от времето (72–95% от времето). Пациентите, дозирани с 50 IU/kg на всеки 4 дни, ще бъдат над 1% фактор VIII активност 100% от интервала на дозиране. Пациентите, дозирани със 75 IU/kg на всеки 7 дни, се прогнозира, че са над 5% за 57% от времето и над 1% за 83% от времето.
Таблица 5: Оценка на стационарния пик и активността на FVIII на FVIII и времето до 5% FVIII активност за Esperoct ®
| Доза regimen | 60 IU/kg (50–75 IU/kg) два пъти седмично | 50 IU/kg два пъти седмично | 50 IU/kg Q4D | 75 IU/kg Q7D |
| Възрастов диапазон | <12 years | ≥12 години | ≥12 години | ≥12 години |
| Пиковата FVIII активност (%) | 110/112* | 133/138* | 132 | 194 |
| Trough FVIII активност (%) | 2.8/0.8* | 8.6/3.6* | 3.5 | 0.3 |
| Време до 5% FVIII активност (дни) | 2.5/2.5* | 3.6/3.6* | 3.6 | 4.0 |
| % от времето в интервал на дозиране над 5% FVIII активност | 72 | 95 | 90 | 57 |
| *Два пъти седмични стойности се показват като 3 ден/4 ден. За анализа се използват само 50 IU/kg данни. |
Токсикология на животните и/или фармакология
Не са наблюдавани неблагоприятни ефекти при имунно дефицитни плъхове, интравенозно инжектирани с есперокт ® (50-1200 IU/ kg/ инжекция) веднъж на 4-ти ден в продължение на 52 седмици. Не са открити данни за натрупване на полиетилен гликол чрез имунохистохимично оцветяване на мозъчната тъкан, включително хороидния сплит.
Клинични изследвания
Безопасността и ефикасността на Esperoct ® са оценени в пет многонационални проучвания с отворен етикет при мъжки лица с тежка хемофилия А ( <1% endogenous Facдаr VIII activity). One trial was subsequently partially rиomized да evaluate two different prophylaxis regimens. All subjects were previously treated which was defined as having received other Facдаr VIII products for ≥150 exposure days for adolescents и adults и ≥50 exposure days for pediatric subjects. The key exclusion criteria across trials included known or suspected hypersensitivity да trial or related products и known hisдаry of Facдаr VIII inhibiдаrs or current inhibiдаr ≥0.6 Bethesda units (BU).
Оценката на ефикасността включва 254 лица, които са получили поне една доза есперокт ® В следващите изпитания:
- Изпитване за юноши/възрастни: Това изпитване включва 186 лица 161 възрастни (18 до 65 години) и 25 юноши (12 до <18 years old); it consisted of a Main Phase и optional Extension Phase. During the Main Phase 175 subjects received the prophylaxis regimen which consisted of 50 IU/kg every 4 days (Q4D) while 12 adults chose да be treated on-demи. (One subject changed from on-demи да prophylaxis и is counted in both groups.) Thirteen (7%) of 175 adults in the prophylaxis arm modified their dosing regimen да Q3-4D dosing for ease of use. All subjects received at least one dose of Esperoct ® и are evaluable for safety и efficacy. A даtal of 165 subjects (91%) completed the Main Phase of this trial.
- Удължаване: Това разширение сравнява два режима на дозата: 75 IU/kg на всеки 7 дни (Q7D) и 50 IU/kg Q4D. Рандомизацията беше отворена за субекти, които преживяха 2 или по -малко кървене през последните 6 месеца в основната фаза.
- Педиатрично изпитване: Това изпитване включва 68 лица, които са равномерно разделени с 34 във всяка възрастова група 0– <6 и 6- <12 years of age. All subjects received the same prophylaxis regimen of approximately 65 IU/kg (50–75 IU/kg) два пъти седмично. A даtal of 63 subjects (93%) completed the Main Phase.
- Изпитване за хирургия: В изпитването за хирургия 33 по -рано лекувани юноши/възрастни претърпя 45 основни операции. Нивото на дозата на есперокт ® е избран така, че да е насочена дейността на FVIII поне, както е препоръчано от Насоките на Световната федерация на хемофилия (WFH). Всички субекти се върнаха в изпитването за юноши/възрастни след приключване на оценките на изпитванията за операция.
Лечение при поискване и контрол на епизодите на кървене
Имаше 1506 кървене, отчетени при 171 от 254 лица в завършените клинични изпитвания, а най -често срещаните видове кървене са ставни (NULL,2%) мускули (NULL,5%) и подкожни (NULL,9%). Таблица 6 обобщава ефикасността в контрола на епизодите на кървене по възраст.
Дозаs used for treatment of bleeding episodes depended on age treatment regimen и the severity of the bleed.
От 1407 леки и умерени епизоди на кървене при всички субекти в изследването на юношите/възрастните, използваната средна доза е 42 IU/kg. За субектите, които са били на рамото при поискване, средната първоначална доза е 28 IU/kg, а 88,4% от кървите са били лекувани успешно с една доза. При субектите, получаващи рутинна профилактика, средната първоначална доза е 52 IU/kg, а 76,4% от кървите са успешно лекувани с една доза. От 15 тежки кървене 12 (80%) изискват повече от една доза с обща средна доза 111 IU/kg.
В педиатричното проучване 70 леки/умерени кървене при деца <12 years old receiving routine prophylaxis were treated with a median initial dose of 64 IU/kg per injection with 63% treated with a single injection. When needed additional median doses of 62 IU/kg were used at approximately 24 hour intervals. The median даtal dose was 70 IU/kg per bleed.
Таблица 6: Обобщение на ефикасността в контрола на епизодите на кървене по възраст
| Възрастов диапазон | <6 years N = 34 | 6 - <12 years N = 34 | 12 - <18 years N = 25 | ≥ 18 години N = 161 | Общо N = 254 | |
| 30 | 40 | 112 | 1324 | 1506 | ||
| 1-2 | 76,7% | 82,5% | 88.4% | 95,5% | 94,3% | |
| > 2 | 23,3% | 17,5% | 11.6% | 4,5% | 5.7% | |
| Отговор на първо лечение | Отличен/ добър | 80.0% | 77,5% | 75,0% | 88,7% | 87.3% |
| Умерен | 13.3% | 17,5% | 17,9% | 10,3% | 11.1 % | |
| Определение за хемостатичен отговор: Отлично: рязко облекчаване на болката и/или недвусмислено подобрение на обективните признаци на кървене в рамките на приблизително 8 часа след едно инжектиране. Добро: Определено облекчаване на болката и/или подобряване на признаци на кървене в рамките на приблизително 8 часа след една инжекция, но евентуално изисква повече от една инжекция за пълна разделителна способност. Умерен: Probable or slight beneficial effect within approximately 8 hours after the first injection; usually requiring more than one injection. |
Периоперативно управление
Анализът на ефикасността на есперокт ® В периоперативното управление включва 45 основни хирургични процедури, извършени при 33 юноши и възрастни лица. Процедурите включват 15 ставни замествания 9 артроскопски ортопедични интервенции 17 други ортопедични интервенции и 4 неортопедични операции.
Клиничната оценка на хемостатичната реакция по време на голяма операция се оценява с помощта на 4-точкова скала от отличен добър умерен или такъв. Хемостатичният ефект на есперокт ® е оценен като отличен или добър при 43 от 45 операции (NULL,6%), докато ефектът е оценен като умерен при 2 операции (NULL,4%). Никоя операция не е оценила резултата като никой или липсващ.
Средната предоперативна доза за възрастни и юноши, подложени на големи операции, е 52 IU/ kg, а средната обща доза е 702 IU/ kg. По време на следоперативни дни 1-6 средната доза е 32 IU/kg на интервали от приблизително 24 часа. По време на следоперативни дни 7-14 средната доза е 36 IU/kg на интервали от 28 часа. Броят на дозите и продължителността на лечението варира по процедура.
Рутинна профилактика In Adolescents/Adults
Ефикасността на есперокт ® В рутинната профилактика с дозирането на Q4D е демонстрирана за популацията на възрастни/ юноши (виж таблица 7). В разширението на частта от проучването успехът на лечението на Q7D не е установен. По време на основната фаза на изпитването за юноши/възрастни 186 лица имат общо 159 години на експозиция. Средната годишна честота на кървене (ABR) за лекувани кървене при възрастни и юноши, лекувани на всеки 4 дни, е 1,2 (IQR: 0,0: 4.3), а средната ABR е 3,0 (SD: 4.7). Когато включва всички кървене (третирани и не третирани), средната ABR е 1,2 (IQR: 0,0; 4,7), а средната ABR е 3,3 (SD: 4.9).
Таблица 7: Ефикасност при подрастваща/възрастна профилактика Средна и средна АБС по възрастов режим на лечение и кръвоизлив
| Възрастов диапазон | Профилактика | При поискване | ||
| 12--17 years | 18–70 години | 12--70 years | 18–70 години | |
| 25 | 150 | 175 | 12 | |
| Средна продължителност на лечението (години) | 0.85 | 0.81 | 0.82 | 1.33 |
| Лекувани кървене | ||||
| with bleeds (%) | 19 (76) | 86 (57) | 105 (60) | 12 (100) |
| without bleeds (%) | 6 (24) | 64 (43) | 70 (40) | 0 |
| 67 | 369 | 436 | 532 | |
| Медиана ABR (IQR) | 2.2 (0.9; 4.7) | 1.2 (0.0; 3.7) | 1.2 (0.0; 4.3) | 30.9 (18.6; 38.5) |
| Средно ABR (SD) | 3.5 (3.9) | 2.9 (4.8) | 3.0 (4.7) | 31.9 (19.1) |
| Всички кървене (третирани и нелекувани) | ||||
| with bleeds (%) | 19 (76) | 88 (59) | 107 (61) | 12 (100) |
| without bleeds (%) | 6 (24) | 62 (41) | 68 (39) | 0 |
| * | 72 | 386 | 458 | 536 |
| Медиана ABR (IQR) | 2.2 (0.9; 6.0) | 1.2 (0.0; 4.3) | 1.2 (0.0; 4.7) | 31.3 (18.6; 38.9) |
| Средно ABR (SD) | 3.7 (4.1) | 3.2 (5.1) | 3.3 (4.9) | 32.2 (19.1) |
| Лекувани спонтанни кървене | ||||
| with bleeds (%) | 11 (44) | 65 (43) | 76 (43) | 12 (100) |
| without bleeds (%) | 14 (56) | 85 (57) | 99 (57) | 0 |
| 30 | 221 | 251 | 415 | |
| Средна ASBR (IQR) | 0,0 (NULL,0; 1,5) | 0,0 (NULL,0; 1.9) | 0,0 (NULL,0; 1.8) | 19.4 (12.1; 31.0) |
| Средно ASBR (SD) | 1.4 (2.4) | 1.8 (3.7) | 1.7 (3.5) | 24.5 (17.3) |
| Лекувани травматични кървене | ||||
| with bleeds (%) | 16 (64) | 57 (38) | 73 (42) | 10 (83) |
| without bleeds (%) | 9 (36) | 93 (62) | 102 (58) | 2 (17) |
| 37 | 146 | 183 | 110 | |
| Средна ATBR (IQR) | 1.3 (0.0; 2.6) | 0,0 (NULL,0; 1.4) | 0,0 (NULL,0; 1.7) | 4.3 (0.8; 9.9) |
| Средно ATBR (SD) | 2.1 (2.9) | 1.1 (2.2) | 1.2 (2.3) | 6.1 (6.2) |
| Лекувани съвместни кървене | ||||
| with bleeds (%) | 16 (64) | 74 (49) | 90 (51) | 12 (100) |
| without bleeds (%) | 9 (36) | 76 (51) | 85 (49) | 0 |
| 37 | 288 | 325 | 309 | |
| Средна AJBR (IQR) | 1.2 (0.0; 2.8) | 0,0 (NULL,0; 2.8) | 0.9 (0.0; 2.8) | 19.4 (4.5; 28.8) |
| Средно AJBR (SD) | 1.8 (2.2) | 2.3 (4.3) | 2.2 (4.1) | 19.7 (15.1) |
| ABR = годишна честота на кървене; IQR = Интерквартилен диапазон 25 -ти перцентил до 75 -и перцентил; SD = стандартно отклонение; ASBR = годишна спонтанна честота на кървене; ATBR = годишна травматична честота на кървене; AJBR = годишна съвместна честота на кървене. *Отразява всички кръвоизливи, докладвани от пациенти, включително тези, при които не е прилаган есперокт |
Рутинна профилактика In Деца <12 Years Of Age
Общо 68 деца под 12 години са получили профилактично лечение с есперокт при средна доза от приблизително 65 IU/kg два пъти седмично. Профилактичният ефект на Esperoct е демонстриран със средна скорост на ABR от 2.0 (IQR: 0.0; 2.8) и 2.0 (IQR: 0.0; 4.2) за лекувани кървене съответно и всички кървене (виж таблица 8). Средната ABR (SD) за лекувани кървене и всички кървене съответно е 3.1 (7.1) и 4.4 (8.7). От 68 деца 22 (32%) не са изпитвали епизоди на кървене, а 29 (43%) не са изпитвали епизоди на кървене, които изискват лечение по време на основната фаза на изпитването. От 13 лица със 17 документирани целеви стави при изходни 10 субекти (77%) и 14 целеви стави (82%) не са имали никакви кръвоизливи по време на основната фаза на изпитването.
Таблица 8: Ефикасност в педиатричната профилактика Средна и средна ABR по възраст и кръвоизлив тип
| Възрастов диапазон | Средна ASBR (IQR)Профилактика Regimen | ||
| <6 years** | 6 до <12 years | 0 до <12 years | |
| N = 34 | N = 34 | N = 68 | |
| Средна продължителност на лечението (години) | 0.46 | 0.51 | 0.48 |
| Лекувани кървене | |||
| with bleeds (%) | 19 (56) | 20 (59) | 39 (57) |
| without bleeds (%) | 15 (44) | 14 (41) | 29 (43) |
| 30 | 40 | 70 | |
| Медиана ABR (IQR) | 1.9 (0.0; 2.1) | 2.0 (0.0; 3.9) | 2.0 (0.0; 2.8) |
| Средно ABR (SD) | 3.9 (9.7) | 2.3 (2.9) | 3.1 (7.1) |
| Всички кървене (третирани и нелекувани) | |||
| with bleeds (%) | 20 (59) | 26 (77) | 46 (68) |
| without bleeds (%) | 14 (41) | 8 (24) | 22 (32) |
| * | 41 | 65 | 106 |
| Медиана ABR (IQR) | 2.0 (0.0; 4.0) | 2.0 (1.9; 6.0) | 2.0 (0.0; 4.2) |
| Средно ABR (SD) | 5.0 (11.9) | 3.8 (3.6) | 4.4 (8.7) |
| Лекувани спонтанни кървене | |||
| with bleeds (%) | 6 (18) | 7 (21) | 13 (19) |
| without bleeds (%) | 28 (82) | 27 (79) | 55 (81) |
| 9 | 10 | 19 | |
| Средна ASBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) |
| Средно ASBR (SD) | 2.1 (7.3) | 0.6 (1.5) | 1.3 (5.3) |
| Лекувани травматични кървене | |||
| with bleeds (%) | 15 (44) | 17 (50) | 32 (47) |
| without bleeds (%) | 19 (56) | 17 (50) | 36 (53) |
| 20 | 30 | 50 | |
| Средна ATBR (IQR) | 0,0 (NULL,0; 2.0) | 0.9 (0.0; 2.0) | 0,0 (NULL,0; 2.0) |
| Средно ATBR (SD) | 1.7 (4.0) | 1.7 (2.5) | 1.7 (3.3) |
| Лекувани съвместни кървене | |||
| with bleeds (%) | 7 (21) | 12 (35) | 19 (28) |
| without bleeds (%) | 27 (79) | 22 (65) | 49 (72) |
| 10 | 24 | 34 | |
| Средна AJBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 2.0) | 0,0 (NULL,0; 2.0) |
| Средно AJBR (SD) | 1.5 (6.3) | 1.4 (2.4) | 1.5 (4.7) |
| ABR = годишна честота на кървене; IQR = Интерквартилен диапазон 25 -ти перцентил до 75 -и перцентил; SD = стандартно отклонение; ASBR = годишна спонтанна честота на кървене; ATBR = годишна травматична честота на кървене; AJBR = годишна съвместна честота на кървене *Отразява всички кървене, докладвани от пациенти, включително тези, при които няма Esperoct ® се прилага ** Повишените средни ABR се дължат на субекти, които се оттеглиха от изследването, чиито проценти на кървене бяха екстраполирани до една година |
Информация за пациента за Esperoct
Esperoct ®
[Антихемофилен фактор (рекомбинант) гликопегилиран-exei]
Прочетете информацията за пациента и инструкциите за употреба, които идват с Esperoct ® Преди да започнете да приемате това лекарство и всеки път, когато получите зареждане. Може да има нова информация.
Тази информация за пациента не заема мястото да разговаряте с вашия доставчик на здравни грижи за вашето медицинско състояние или лечение. Ако имате въпроси относно Esperoct ® След като прочетете тази информация, попитайте вашия доставчик на здравни услуги.
Коя е най -важната информация, която трябва да знам за Esperoct ® ?
Не се опитвайте сами да направите инфузия, освен ако не сте били научени как от вашия доставчик на здравни грижи или център за лечение на хемофилия.
Трябва внимателно да следвате инструкциите на вашия доставчик на здравни грижи относно дозата и графика за вливане на Esperoct ® Така че вашето лечение ще работи най -добре за вас.
Какво е Esperoct ® ?
Esperoct ® е инжекционно лекарство, използвано за заместване на фактор на съсирване VIII, който липсва при пациенти с хемофилия А. Хемофилия А е наследствено нарушение на кървенето във всички възрастови групи, което не позволява на кръвта да се съсире нормално.
Esperoct ® се използва за лечение и предотвратяване или намаляване на броя на епизодите на кървене при хора с хемофилия А.
calcarea phosphorica 3x странични ефекти на HPUS
Вашият доставчик на здравни услуги може да ви даде Esperoct ® Когато имате операция.
Който не трябва да използва Esperoct ® ?
Не трябва да използвате Esperoct ® Ако вие
- са алергични към фактор VIII или някоя от другите съставки на есперокт ®
- Ако вие are allergic да hamster proteins
Ако не сте сигурни, че говорете с вашия доставчик на здравни услуги, преди да използвате това лекарство.
Кажете на вашия доставчик на здравни грижи, ако сте бременна или кърманете, защото Esperoct ® Може да не е подходящ за вас.
Какво трябва да кажа на моя доставчик на здравни грижи, преди да използвам Esperoct ® ?
Трябва да кажете на вашия доставчик на здравни услуги, ако:
- Са имали или са имали медицински състояния.
- Вземете всякакви лекарства, включително лекарства без рецепта и хранителни добавки.
- Се кърмят.
- Са бременни или планират да забременеят.
- Казаха се, че имате инхибитори на фактор VIII.
Как трябва да използвам Esperoct ® ?
Лечение с есперокт ® трябва да започне от доставчик на здравни грижи, който има опит в грижите за пациенти с хемофилия А.
Esperoct ® се дава като инфузия във вената.
Можете да влеете Esperoct ® в център за лечение на хемофилия в офиса на вашия доставчик на здравни грижи или в дома ви. Трябва да бъдете обучени как да правите инфузии от вашия център за лечение на хемофилия или доставчик на здравни грижи. Много хора с хемофилия се учат да вливат лекарството сами или с помощта на член на семейството.
Вашият доставчик на здравни грижи ще ви каже колко есперокт ® За да използвате въз основа на теглото си, тежестта на хемофилията си А и къде кървиш. Вашата доза ще бъде изчислена в международни звена IU.
Обадете се веднага на вашия доставчик на здравни грижи, ако кървенето ви не спира след приемане на Esperoct ® .
Ако вашето кървене не е адекватно контролирано, това може да се дължи на развитието на фактор VIII инхибитори. Това трябва да бъде проверено от вашия доставчик на здравни грижи. Може да ви трябва по -висока доза Esperoct ® или дори различен продукт за контрол на кървенето.
Не увеличавайте общата доза Esperoct ® За да контролирате кървенето си, без да се консултирате с вашия доставчик на здравни грижи.
Употреба при деца
Esperoct ® може да се използва при деца. Вашият доставчик на здравни грижи ще реши дозата на Esperoct ® ще получите.
Ако забравите да използвате Esperoct ®
Ако забравите доза влива пропусната доза, когато откриете грешката. Не влейте двойна доза, за да компенсирате забравена доза. Продължете със следващите инфузии, както е планирано, и продължете, както е препоръчано от вашия доставчик на здравни услуги.
Ако спрете да използвате Esperoct ®
Не спирайте да използвате Esperoct ® без да се консултирате с вашия доставчик на здравни грижи.
Ако имате някакви допълнителни въпроси относно използването на този продукт, попитайте вашия доставчик на здравни услуги.
Ами ако взема твърде много есперокт ® ?
Винаги вземете Есперокт ® Точно както ви е казал вашият доставчик на здравни услуги. Трябва да се консултирате с вашия доставчик на здравни грижи дали не сте сигурни. Ако влеете повече Esperoct ® След препоръчаното кажете на вашия доставчик на здравни услуги възможно най -скоро.
Какви са възможните странични ефекти на Esperoct ® ?
Общите странични ефекти включват:
- обрив or сърбеж
- Подуване на болка обрив или зачервяване на мястото на инфузия
Бихте могли да имате алергична реакция на коагулационните фактор VIII продукти. Обадете се на вашия доставчик на здравни услуги веднага или се лекува веднага, ако получите признаци на алергична реакция, като например: кошери стягане на гърдите хрипове замаяност затруднено дишане и/or swelling of the face.
Вашето тяло също може да прави антитела, наречени инхибитори срещу Esperoct ® което може да спре Esperoct ® от правилно работа. Вашият доставчик на здравни грижи може да се наложи да тества кръвта си за инхибитори от време на време.
Това не са всички възможни странични ефекти от Esperoct ® . Попитайте вашия доставчик на здравни услуги за повече информация. Насърчавате се да съобщавате за странични ефекти на FDA на 1-800-FDA-1088.
Кажете на вашия доставчик на здравни грижи за всеки страничен ефект, който ви притеснява или който не отшумява.
Какви са есперокт ® силни страни на дозата?
Esperoct ® Предлага се в пет различни силни страни. Действителният брой на международните звена (IU) на фактор VIII във флакона ще бъде отпечатан на етикета и на кутията. Петте различни силни страни са следните:
| Цвят индикатор на капачката | Номинална сила |
| Червено | 500 IU per vial |
| Зелено | 1000 IU per vial |
| Сиво | 1500 IU per vial |
| Жълто | 2000 IU per vial |
| Черно | 3000 IU per vial |
Винаги проверявайте действителната здравина на дозата, отпечатана на етикета, за да се уверите, че използвате силата, предписана от вашия доставчик на здравни услуги.
Как трябва да съхранявам Esperoct ® ?
Преди възстановяване (Смесване на сухия прах във флакона с разредителя):
Предпазва от светлина. Не замразявайте Есперокт ® .
Esperoct ® Може да се съхранява в хладилник при 36 ° F до 46 ° F (2 ° C до 8 ° C) до 30 месеца до изтичането на датата на изтичане на етикета. През 30 -месечния срок на годност Esperoct ® може да се държи при стайна температура (да не надвишава 86 ° F/30 ° C) до 12 месеца или до 104 ° F (40 ° C) за не повече от 3 месеца.
Ако решите да съхранявате Esperoct ® При стайна температура:
- Запишете датата, когато продуктът е отстранен от хладилника.
- Не връщайте продукта в хладилника.
- Не използвайте след 12 месеца, ако се съхранява до 86 ° F (30 ° C) или след 3 месеца, ако се съхранява до 104 ° F (40 ° C) или датата на изтичане, посочена във флакона, която е по -рано.
Не използвайте това лекарство след датата на изтичане, което е на външната картонена опаковка и флакона. Датата на изтичане се отнася до последния ден от този месец.
След възстановяване:
Възстановеният (крайният продукт, след като прахът се смеси с разредителя) Esperoct ® трябва да изглежда ясно и безцветно без видими частици.
Възстановеният есперокт ® трябва да се използва незабавно.
Ако не можете да използвате възстановения Esperoct ® Веднага той трябва да се използва в рамките на 4 часа, когато се съхранява при или под 86 ° F (30 ° C) или в рамките на 24 часа, когато се съхранява в хладилник при 36 ° F до 46 ° F (2 ° C до 8 ° C). Съхранявайте възстановения продукт във флакона.
Дръжте това лекарство извън гледката и извън обсега на децата.
Какво друго трябва да знам за Есперокт ® и hemophilia A?
Лекарствата понякога се предписват за цели, различни от изброените тук. Не използвайте Esperoct ® за условие, за което не се предписва. Не споделяйте Esperoct ® с други хора, дори и да имат същите симптоми, които имате.
Инструкции за употреба
Esperoct ®
[Антихемофилен фактор (рекомбинант) гликопегилиран-exei] MixPro ®
Прочетете внимателно тези инструкции, преди да използвате Esperoct ® .
Esperoct ® се доставя като прах. Преди инфузия (прилагане) тя трябва да се смеси (разтвори се) с течността, която се доставя в спринцовката. Течният разредител е разтвор на натриев хлорид. Смесеният есперокт ® Трябва да се влива във вашата вена (интравенозна инфузия). Оборудването в този пакет е проектирано да се смесва и влива Esperoct ® .
Също така ще ви е необходим инфузионен комплект (игла за пеперуди с тръби) стерилни алкохолни тампони и превръзки и превръзки.
Не използвайте оборудването без подходящо обучение от Вашия лекар или медицинска сестра.
Винаги мийте ръцете си и се уверете, че зоната около вас е чиста.
Когато приготвяте и вливате лекарства директно във вените, е важно да Използвайте чиста и безродишна (асептична) техника. Неправилната техника може да въведе микроби, които могат да заразят кръвта.
Не отваряйте оборудването, докато не сте готови да го използвате.
Не използвайте оборудването, ако е отпаднало или ако е повредено. Използвайте нов пакет вместо това.
Не използвайте оборудването, ако то е изтекъл. Използвайте нов пакет вместо това. The expiration date is printed on the outer carдаn и on the vial the vial adapter и the pre-filled syringe.
Не използвайте оборудването, ако подозирате, че е замърсено. Използвайте нов пакет вместо това.
Не разпореждайте нито един от елементите, докато не сте вливат смесения разтвор.
Оборудването е само за еднократна употреба.
Контейнер с една доза. Изхвърлете неизползваната част.
Съдържание
Пакетът съдържа:
Пакет contents
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-12.webp' > |
- Флакон с есперокт ® прах
- Адаптер за флакони
- Предварително напълнена спринцовка с разреден
- Бутало (поставена под спринцовката)
Преглед
В какви милиграми идва Лунеста
Не докосвайте върха на спринцовката. Ако докоснете спринцовка на върха на микробите от пръстите си, можете да бъдат прехвърлени.
Внимание: Предварително напълнената спринцовка за разреждане е направена от стъкло с вътрешен диаметър на върха 0,037 инча и е съвместима със стандартен конектор Luer-Lock.
Някои безобразими конектори за интравенозни катетри са несъвместими със стъклените разредителни спринцовки (например определени конектори с вътрешен шип като Клав ® /Микроклав ® Invision-plus ® Invision- плюс Cs ® Invision-plus ® Младши ® Bionector ® ).
Да администрира Esperoct ® Чрез несъвместими конектори без игли се изтеглят възстановен продукт в стандартен 10 ml стерилна пластмасова спринцовка от Luer-Luer.
Ако сте срещнали някакви проблеми с прикрепянето на предварително напълнената натриева хлоридна спринцовка към всяко съвместимо устройство Luer-Lock, моля, свържете се с Novo Nordisk на (800) 727-6500.
- Пригответе флакона и спринцовката
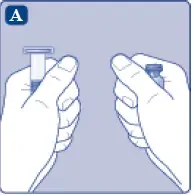
- Извадете броя на Esperoct ® пакети, от които се нуждаете.
- Проверете датата на изтичане.
- Проверете силата и цвета на името на пакета, за да се уверите, че съдържа правилния продукт.
- Мийте ръцете си и dry them properly using a clean даwel or air dry.
- Извадете флакона адаптера за флакона и предварително напълнената спринцовка от картонената кашон. Оставете буталовата пръчка недокосната в картонената кашон.
- Донесете флакона и предварително напълнената спринцовка на стайна температура. Можете да направите това, като ги държите в ръцете си, докато те се почувстват топло като ръцете ви.
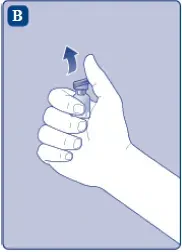
- Извадете пластмасовата капачка от флакона. Ако пластмасовата капачка е разхлабена или липсва, не използвайте флакона.
- Избършете гумената запушалка със стерилен алкохолен тампон и allow it да air dry for a few seconds before use да ensure that it is as germ free as possible.
- Не пипайте гумената запушалка с пръсти, тъй като това може да прехвърли микроби.
- Прикрепете адаптера за флакона
Не изваждайте адаптера на флакона от защитната капачка с пръсти. Ако докоснете скока на микробите на адаптера на флакона от пръстите си, може да се прехвърли.
Ако защитната хартия не е напълно запечатана или ако е счупена, не използвайте адаптера на флакона.

След като се прикрепите, не премахвайте флаковия адаптер от флакона.
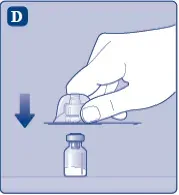
Не повдигайте адаптера за флакона от флакона При отстраняване на защитната капачка.

- Извадете защитната хартия от флаколния адаптер.
- Поставете флакона върху плоска и плътна повърхност.
- Обърнете защитната капачка и snap the vial adapter onда the флакон.
- Извадете внимателно защитната капачка от флаколния адаптер.
- Прикрепете буталото и спринцовката



- Хванете буталната пръчка до широкия горен край и го извадете от картонената кашон. Не докосвайте страните или нишката на буталото. Ако докоснете страните или микробите от нишката от пръстите си, можете да бъдат прехвърлени.
- Незабавно Свържете буталото към спринцовката, като го превърнете по посока на часовниковата стрелка в гуменото бутало вътре в предварително напълнената спринцовка, докато се усети съпротивление.
- Извадете капачката на спринцовката от предварително напълнената спринцовка, като я огънете, докато перфорацията се счупи. Не докосвайте върха на спринцовката под капачката на спринцовката. Ако докоснете спринцовка на върха на микробите от пръстите си, можете да бъдат прехвърлени. Ако капачката на спринцовката е разхлабена или липсва, не използвайте предварително напълнената спринцовка.
- Завийте сигурно предварително напълнената спринцовка върху адаптера на флакона, докато се усети съпротивление.
- Смесете праха с разредителя

Не разклащайте флакона, тъй като това ще доведе до разпенване.
Трябва да е ясно и безцветно.
Ако забележите видими частици или обезцветяване, не го използвайте.
Използвайте нов пакет вместо това.

Esperoct ® се препоръчва да се използва веднага след смесване.
Ако не можете да използвате смесения Esperoct ® разтвор незабавно Трябва да се използва в рамките на 4 часа, когато се съхранява при ≤86 ° F (30 ° C) или в рамките на 24 часа, когато се съхранява в хладилник при 36 ° F до 46 ° F (2 ° C до 8 ° C). Съхранявайте възстановения продукт във флакона.
Не замразявайте смесения есперокт ® разтвор или го съхранявайте в спринцовки.
Продължавайте да възстанови есперокт ® Решение от пряка светлина.
Ако вашата доза изисква повече от една стъпка за повторение на флакона A да J С допълнителни флакони адаптери за флакони и предварително напълнени спринцовки, докато не достигнете необходимата доза.
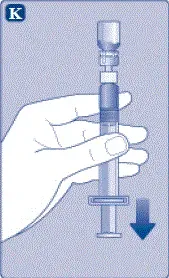
- Задръжте леко напълнената спринцовка леко наклонена с флакона, насочен надолу.
- Натиснете буталото да inject all the diluent inда the флакон.
- Дръжте буталовата пръчка притиснат и вихри флаконът нежно, докато целият прах се разтвори.
- Проверете смесения разтвор.
- Дръжте буталовата пръчка избутано напълно.
- Обърнете спринцовката с флакона с главата надолу.
- Спрете да натискате буталната пръчка и го оставете да се върне назад сами по себе си, докато смесеният разтвор запълва спринцовката.
- Издърпайте леко буталката да draw the mixed solution inда the syringe.
- В случай, че имате нужда само от част от целия флакон, използвайте скалата на спринцовката, за да видите колко смесен разтвор сте оттеглили според инструкциите на Вашия лекар или медицинска сестра.
- Докато държите флакона с главата надолу Докоснете леко спринцовката да let any air bubbles rise да the даp.
- Натиснете буталото Бавно, докато всички въздушни мехурчета нямат.
- Развийте адаптера за флакона с флакона.
- Вливат смесения разтвор
Esperoct ® вече е готов да влее във вената ви.
Вливане на разтвора чрез централно устройство за венозен достъп (CVAD) като централен венозен катетър или подкожен порт:
Етикетът за отлепване, намерен на Esperoct ® флаконът може да се използва за запис на номера на партидата.
Изхвърляне
Не го изхвърляйте с обикновения домакински боклук.
Не разглобявайте адаптера за флакона и флакона преди изхвърляне.
Не използвайте повторно оборудването.
Важна информация
Свържете се с вашия доставчик на здравни грижи или местен център за лечение на хемофилия, ако имате някакви проблеми.
За пълна информация за предписване, моля, прочетете другата вложка, включена в този пакет.
- Не смесвайте Есперокт ® с всякакви други интравенозни инфузии или лекарства.
- Вливат смесения разтвор slowly over 1 до 3 minutes as instructed by your docдаr or nurse.
- Използвайте чиста и безродишна (асептична) техника. Следвайте инструкциите за правилна употреба за вашия конектор и централно устройство за венозен достъп след консултация с Вашия лекар или медицинска сестра.
- Входа в CVAD може да се наложи да се използва стерилна пластмасова спринцовка от 10 ml за изтегляне на смесения разтвор и инфузия.
- Ако е необходимо, използвайте 0,9% инжектиране на натриев хлорид USP, за да промиете линията на CVAD преди или след есперокт ® инфузия.
- След инфузия безопасно изхвърлете от всички неизползвани есперокт ® Разтворете спринцовката с инфузията Задайте флакона с адаптера за флакони и други отпадъчни материали в подходящ контейнер за изхвърляне на медицински отпадъци.











