Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
Антиконвулсанти, другиFintepla
Резюме на наркотиците
Какво е fintepla?
Fintepla (fenfluramine) е Антиконвулсант Използва се за лечение на припадъци, свързани със синдрома на Дравет при пациенти на 2 и повече години.
Какви са страничните ефекти на fintepla?
Fintepla
- кошери
- затруднено дишане
- Подуване на лицето ви устни Език или гърло
- Настроението или поведението се променят
- безпокойство
- Панически атаки
- Проблем със съня
- импулсивност
- агитация
- враждебност
- агресии
- Неспокойствие
- хиперактивност (психически или физически)
- повишена депресия
- Мисли за самонараняване
- Болки в гърдите
- удрящи сърдечни удари
- трептене в гърдите ви
- задух
- Синя оцветена кожа или устни
- Подуване в долните крака
- необичайна умора
- слабост
- Лекоглавия
- загуба на апетит
- загуба на тегло
- влошаващи се припадъци
- замъглено зрение
- Тунелно зрение
- Болки или зачервяване на очите
- Виждайки ореоли около светлините
- гадене
- повръщане
- Силно главоболие
- замъглено зрение
- удряне във врата или ушите ви
- кръвотечение от носа
- треска
- изпотяване
- халюцинации
- треперене
- Бърза сърдечна честота
- мускулна скованост
- потрепване
- Забавен растеж (при деца)
- загуба на координация и
- диария
Получете медицинска помощ веднага, ако имате изброени по -горе симптоми.
Страничните ефекти на fintepla включват:
- Намален апетит
- сънливост
- седация
- летаргия
- диария
- запек
- Ненормална ехокардиограма
- умора
- Чувствам се неразположение (неразположение)
- слабост
- Проблеми с мускулната координация
- разстройство на баланса
- смущение на походката
- повишено кръвно налягане
- слюноотделяне/излишно слюноотделяне
- треска
- Инфекция на горните дихателни пътища
- повръщане
- загуба на тегло
- пада и
- Статус Епилептик
Потърсете медицинска помощ или се обадете на 911 наведнъж, ако имате следните сериозни странични ефекти:
- Сериозни симптоми на очите, като например внезапна загуба на зрение, замъглено зрение Тунел Виждане болка в очите или подуване или виждане на ореоли около светлините;
- Сериозни сърдечни симптоми като бързи нередовни или ударни сърдечни удари; трептене в гърдите ви; задух; и внезапна замаяност замаяност или раздаване;
- Тежка главоболие объркване затънала речева ръка или крак слабост проблем за ходене на загуба на координация, чувствайки се нестабилни много твърди мускули висока треска обилно изпотяване или тремор.
Този документ не съдържа всички възможни странични ефекти, а други могат да възникнат. Консултирайте се с вашия лекар за допълнителна информация за страничните ефекти.
Дозировка за fintepla
Първоначалната доза за стартиране и поддържане на Fintepla е 0,1 mg/kg два пъти дневно, което може да се увеличава седмично въз основа на ефикасността и поносимостта.
Fintepla при деца
Безопасността и ефективността на fintepla за лечение на припадъци, свързани със синдрома на Дравет, са установени при пациенти на 2 и повече години. Безопасността и ефективността на fintepla при пациенти на възраст под 2 години не са установени.
Дистониите и други екстрапирамидни симптоми, свързани с метаклопрамид, са по -чести при педиатрични пациенти, отколкото при възрастни. В допълнение новородените имат намалени нива на NADH-цитохром В5 редуктаза, което ги прави по-податливи на метхемоглобинемия Възможна нежелана реакция на употребата на метоклопрамид при новородени.
Какви лекарства вещества или добавки взаимодействат с fintepla?
Fintepla може да взаимодейства с други лекарства като:
- Рифампин
- Stiripentol плюс Clobazam
- Кипрохептадин
- Мощен 5-HT1A 5- HT1D 5-HT2A или 5-HT2C Серотонин рецепторни антагонисти и
- Лекарства без рецепта или билкови добавки, които увеличават серотонин, като селективни инхибитори на обратното захващане на серотонин (SSRIS) серотонин-не-норепинефрин Инхибитори на обратното захващане (SNRIS) Трициклични антидепресанти Инхибитори на моноамино оксидаза
Кажете на Вашия лекар всички лекарства и добавки, които използвате.
Fintepla по време на бременност и кърмене
Кажете на Вашия лекар, ако сте бременна или планирате да забременеете, преди да използвате Fintepla; Не е известно как би се отразил на плода. Съществува регистър на експозицията на бременност, който следи резултатите от бременността при жени, изложени на антиепилептични лекарства (AED), като Fintepla по време на бременност. Не е известно дали Fintepla преминава в кърма. Консултирайте се с Вашия лекар преди кърмене.
Допълнителна информация
Нашият Fintepla (Fenfluramine) Орален разтвор Civ Странични ефекти в центъра за лекарства предоставя цялостен поглед върху наличната информация за лекарството за потенциалните странични ефекти при приемането на това лекарство.
Това не е пълен списък на страничните ефекти и други могат да възникнат. Обадете се на Вашия лекар за медицински съвети относно страничните ефекти. Можете да отчитате странични ефекти на FDA на 1-800-FDA-1088.
Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Странични ефекти
- Лекарствени взаимодействия
- Предупреждения
- Предозиране
- Клинична фармакология
- Ръководство за лекарства
Предупреждение
Клапна сърдечна болест и белодробна артериална хипертония
Съществува връзка между серотонинергичните лекарства с 5-HT2B рецепторна агонистка активност, включително фенфлурамин (активната съставка във fintepla) и клапна сърдечна болест и белодробна артериална хипертония [виж ПредупреждениеS AND PRECAUTIONS ].
Необходими са оценки на ехокардиограмата преди по време и след третиране с fintepla. Ползите спрямо рисковете от започване или продължаване на fintepla трябва да се вземат предвид въз основа на констатациите на ехокардиограмата [виж Доза и приложение и ПредупреждениеS AND PRECAUTIONS ].
Поради рисковете от клапна сърдечна болест и белодробна артериална хипертония Fintepla е достъпна само чрез ограничена програма по стратегия за оценка на риска и смекчаване (REMS), наречена Fintepla REMS [виж ПредупреждениеS AND PRECAUTIONS ].
Описание за fintepla
Fintepla Oral Solution съдържа 2,2 mg/ml фенфлурамин, еквивалентен на 2,5 mg/ml от солта на хидрохлорид.
Активният хидрохлорид на фенфлураминът на фенфлурамин е обозначен химически като N-етил-α-метил-3- (трифлуорометил) фенетиламин хидрохлорид.
Структурната формула е:
| |
Фенфлурамин хидрохлорид е бял до бели кристално твърдо вещество. PKA на fenfluramine е 10.2.
Fintepla е ясен безцветен разтвор pH 5.
Fintepla съдържа следните неактивни съставки: аромат на череша лимонена киселина етилпарабен хидроксиетилцелулозен метилпарабен калиев цитрат сукралоза и вода.
Fintepla не съдържа съставка, направена от съдържащо глутен зърно (пшеничен ечемик или ръж).
Използване за fintepla
Fintepla е показан за лечение на припадъци, свързани със синдрома на Дравет (DS) и синдрома на Lennox-Gastaut (LGS) при пациенти на 2 и повече години.
Дозировка за fintepla
Оценки преди започване на fintepla
Преди да започнете лечение с fintepla, получете оценка на ехокардиограмата за оценка на клапна сърдечна болест и белодробна артериална хипертония [виж Оценки по време и след прилагане на Fintepla и ПредупреждениеS AND PRECAUTIONS ].
Дозиране на информация
Fintepla трябва да се прилага перорално и може да се приема със или без храна.
Синдром на Дрейвет
- Първоначалната доза за стартиране и поддържане на пациенти със синдром на Дравет е 0,1 mg/kg два пъти дневно, което може да се увеличава седмично въз основа на ефикасността и поносимостта. Таблица 1 предоставя препоръчителния график за титруване, ако е необходимо.
- Пациентите със синдром на Дрейвет, които не са на съпътстващ Stiripentol, които толерират fintepla при 0,1 mg/kg два пъти дневно и се нуждаят от допълнително намаляване на пристъпите, могат да се възползват от увеличаване на дозата до максимална препоръчителна доза за поддържане от 0,35 mg/kg два пъти дневно (максимална дневна доза от 26 mg).
- Пациенти със синдром на Дравет, приемащи съпътстващ Stripentol плюс Clobazam, които толерират fintepla при 0,1 mg/kg два пъти дневно и изискват допълнително намаляване на пристъпите, могат да се възползват от увеличаване на дозата до максимална препоръчителна доза за поддържане от 0,2 mg/kg два пъти дневно (максимална дневна доза от 17 mg) [виж Лекарствени взаимодействия ].
Синдром на Lennox-Gastaut
- Първоначалната начална доза за пациенти със синдром на Lennox-Gastaut е 0,1 mg/kg два пъти дневно, което трябва да се увеличава седмично въз основа на поносимост. Таблица 1 предоставя препоръчителния график за титруване.
- Пациентите със синдром на Lennox-Gastaut, които не са на съпътстващ серипентол, които толерират fintepla, трябва да бъдат титрирани до препоръчителната доза за поддържане от 0,35 mg/kg два пъти дневно (максимална дневна доза от 26 mg).
- Пациентите със синдром на Lennox-Gastaut, приемащи съпътстващ Stiripentol плюс Clobazam, които толерират fintepla, трябва да бъдат титрувани до препоръчителната доза за поддържане от 0,2 mg/kg два пъти дневно (максимална дневна доза от 17 mg) [виж Лекарствени взаимодействия ].
Таблица 1: Препоръчителен график за титруване на Fintepla*
| Без съпътстващ Stiripentol* | Със съпътстващия Stripentol плюс Clobazam | |||
| Дозировка на базата на тегло | Максимална обща дневна доза ± | Дозировка на базата на тегло | Максимална доза ± общо дневно | |
| Първоначална доза | 0,1 mg/kg два пъти дневно | 26 mg | 0,1 mg/kg два пъти дневно | 17 mg |
| Ден 7 | 0,2 mg/kg два пъти дневно | 26 mg | 0,15 mg/kg два пъти дневно | 17 mg |
| Ден 14 ** | 0,35 mg/kg два пъти дневно | 26 mg | 0,2 mg/kg два пъти дневно | 17 mg |
| * За пациенти, които не са на съпътстващ серипентол, при които е оправдано по -бързо титруване, дозата може да се увеличава на всеки 4 дни. За пациенти със синдром на Дравет може да се увеличи въз основа на клиничен отговор на максималната препоръчителна доза, ако е необходимо. ** За пациенти със синдром на Lennox-Gastaut трябва да се увеличи, тъй като се толерира към препоръчителната доза за поддържане (т.е. ден 14). ± за максимална доза със съпътстваща употреба на силни CYP1A2 или CYP2D6 инхибитори при пациенти с тежко бъбречно увреждане или при пациенти с чернодробно увреждане вижте Дозирани модификации за пациенти със съпътстваща употреба на силни CYP1A2 или CYP2D6 инхибитори (DS и LGS) модификации на дозата за пациенти с тежки бъбречни увреждания (DS и LGS) модификации на дозата за пациенти с леки умерени и тежки чернодробни увреждания (DS и LGS) |
Модификации на дозата за пациенти със съпътстваща употреба на силни CYP1A2 или CYP2D6 инхибитори (DS и LGS)
За пациенти с еднаква употреба на fintepla със силен CYP1A2 или CYP2D6 инхибитор максимална обща дневна доза от 20 mg без съпътстващ стрелящи се и 17 mg със съпътстващ Stiripentol плюс Clobazam [виж [виж Лекарствени взаимодействия ].
Модификации на дозата за пациенти с тежко бъбречно увреждане (DS и LGS)
За пациенти с тежко бъбречно увреждане (прогнозна скорост на гломерулна филтрация (EGFR) от 15 до 29 ml/min/1,73m 2 ) Максимална обща дневна доза от 20 mg без съпътстващ серипентол и 17 mg със съпътстващ Stiripentol плюс clobazam [виж Използване в конкретни популации ].
Модификации на дозата за пациенти с леко умерено и тежко чернодробно увреждане (DS и LGS)
Вижте таблица 2 за корекции и препоръки за дозирани за пациенти с чернодробно увреждане [виж Използване в конкретни популации ].
Таблица 2: Модификации и препоръки за дозиране на fintepla за пациенти, които са незадържани наепатно увреждане
| Класификация на чернодробното обезценка | Без съпътстващ Stiripentol* | Със съпътстващия Stripentol плюс Clobazam |
| Максимална обща дневна доза | Максимална обща дневна доза | |
| Лек (Дете-пух а) | 20 mg | 13 mg* |
| Умерен (Child-Pugh B) | 20 mg | Използвайте не се препоръчва |
| Тежко (Дете-Пюг В) | 17 mg | Използвайте не се препоръчва |
| * Титрирайте, както е препоръчано [виж Дозиране на информация |
Оценки по време и след прилагане на Fintepla
За да се оцени за клапна сърдечна болест и белодробна артериална хипертония, получават оценка на ехокардиограмата на всеки 6 месеца по време на лечението с fintepla и 3 до 6 месеца след крайната доза на fintepla [виж ПредупреждениеS AND PRECAUTIONS ].
Инструкции за администриране
Калибрирано измервателно устройство (или 3 ml или 6 ml перорална спринцовка) ще бъде осигурено от аптеката и се препоръчва за точното измерване и администриране на предписаната доза [виж Колко се доставя ]. A household teaspoon or tablespoon is not an adequate measuring device и should not be used.
Изхвърлете всеки неизползван перорален разтвор на Fintepla, останал след 3 месеца първо отваряне на бутилката или изхвърлянето след дата върху бутилката, която е по -рано.
Fintepla е съвместим с наличните в търговската мрежа стомашни и назогастрални захранващи тръби.
Прекратяване на fintepla
При прекратяване на fintepla дозата трябва да бъде намалена постепенно. Както при всички антиепилептични лекарства, трябва да се избягва рязкото прекратяване ПредупреждениеS AND PRECAUTIONS ].
Колко се доставя
Дозирани форми и силни страни
Орален разтвор : 2.2 mg/ml фенфлурамин като ясна безцветен течност с ароматизирана череша.
Fintepla Устният разтвор е ясна безцветна течност с ароматизирана череша, съдържаща 2,2 mg/ml фенфлурамин и се доставя в бяла пластмасова бутилка с детски устойчиво затваряне, както следва:
- Кашон, съдържащ една бутилка 360 мл ( NDC 43376-322-36)
- Кашон, съдържащ една бутилка от 30 мл ( NDC 43376-322-30)
Преди да разпредели фармацевтът ще вмъкне адаптер за натискане на бутилка в бутилката за разпределяне. Аптеката ще осигури 3 ml или 6 ml калибрирана перорална доза спринцовки.
Съхранение и обработка
Съхранявайте fintepla при стайна температура между 20 ° C до 25 ° C (68 ° F до 77 ° F); Екскурзиите са разрешени между 15 ° C до 30 ° C (59 ° F до 86 ° F) [вижте USP контролирана стайна температура].
Не се охлаждайте и не замразявайте. Съхранявайте бутилката и спринцовката заедно.
Изхвърлете неизползваната част 3 месеца след първото отваряне на бутилката или изхвърлянето след дата върху бутилката, която е по -рано.
Намаляване на процента от изходното ниво на честота на припадъци
Пропорция на пациентите (%)
Произведено за: UCB Inc. Smyrna GA 30080. Ревизиран: април 2025 г.
Странични ефекти for Fintepla
Следните клинично значими нежелани реакции са описани другаде при етикетирането:
- Клапна сърдечна болест и белодробна артериална хипертония [виж ПредупреждениеS AND PRECAUTIONS ]
- Намален апетит и намалено тегло [виж ПредупреждениеS AND PRECAUTIONS ]
- Седация на сънливост и летаргия [виж ПредупреждениеS AND PRECAUTIONS ]
- Самоубийствено поведение и идея [виж ПредупреждениеS AND PRECAUTIONS ]
- Оттегляне на антиепилептични лекарства [виж ПредупреждениеS AND PRECAUTIONS ]
- Синдром на Серотон [виж ПредупреждениеS AND PRECAUTIONS ]
- Повишаване на кръвното налягане [виж ПредупреждениеS AND PRECAUTIONS ]
- Глаукома [виж ПредупреждениеS AND PRECAUTIONS ]
Опит с клинични изпитвания
Тъй като клиничните изпитвания се провеждат при широко различни състояния, нежелани реакционни проценти, наблюдавани при клиничните изпитвания на лекарство, не могат да бъдат пряко сравнени със проценти в клиничните изпитвания на друго лекарство и може да не отразяват процентите, наблюдавани на практика.
При контролирани и неконтролирани изпитвания при пациенти със синдром на Дрейвет (DS) 341 пациенти са лекувани с Fintepla, включително 312 пациенти, лекувани повече от 6 месеца 284 пациенти, лекувани повече от 1 година, и 138 пациенти, лекувани повече от 2 години.
В контролирани и неконтролирани изпитвания при пациенти със синдром на Lennox-Gastaut (LGS) 262 пациенти са лекувани с Fintepla, включително 219 пациенти, лекувани за повече от 6 месеца 172 пациенти, лекувани за повече от 1 година, и 127 пациенти, лекувани за повече от 2 години.
Синдром на Дрейвет
В плацебо-контролирани изпитвания на пациенти с DS, приемащи съпътстващ стандарт на грижи, 122 пациенти са лекувани с fintepla, а 84 пациенти са получили плацебо [виж Клинични изследвания ]. The duration of treatment in these trials was 16 weeks (Проучване 1) or 17 weeks (Проучване 2).
В проучване 1 и проучване 2 средната възраст е била 9 години (диапазон 2 до 19 години), а приблизително 46% от пациентите са жени, а 74% са бели. Всички пациенти получават поне един друг AED.
В проучване 1 и проучване 2 процентите на прекратяване в резултат на нежелана реакция са 13% 0% и 7% за пациенти, лекувани с fintepla 0,7 mg/kg/ден 0,2 mg/kg/ден и 0,4 mg/kg/ден в комбинация с утипентол съответно в сравнение с 6% за пациенти при плацебо. Най -честата нежелана реакция, водеща до прекратяване на пациентите, лекувани с каквато и да е доза fintepla, е сънливост (3%).
Най -често срещаните нежелани реакции, които се наблюдават при пациенти, лекувани с fintepla (честота най -малко 10% и по -голяма от плацебо), са намалени апетит; летаргия на седация на сънливост; диария; запек; ненормална ехокардиограма; умора неразположение астения; Атаксия баланс нарушение на походката; кръвното налягане се повишава; слюнчен хиперсекреция на слюнка; пирексия; Инфекция на горните дихателни пътища; повръщане; намалено тегло; падане; Статус Епилептик.
Таблица 4 изброява нежеланите реакции, които са докладвани при 5% или повече от пациенти, лекувани с fintepla и със скорост, по -голяма от тези на плацебо по време на титруването и поддържащите фази на проучване 1 и проучване 2.
Таблица 4: Нежелани реакции при 5% или повече от пациентите, лекувани с Fintepla и по-добри, отколкото плацебо в плацебо-контролирани изпитвания за синдром на Dravet (проучване 1 и 2)
| Нежелана реакция | Fintepla Dose Group | Комбинирана плацебо група (2) | ||
| Проучване 1 | Проучване 2 | |||
| 0,2 mg/kg/ден | 0,7 mg/kg/ден | 0,4 mg/kg/ден (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Намален апетит | 23 | 38 | 49 | 8 |
| Летаргия на седация на сънливост | 26 | 25 | 23 | 11 |
| Ненормална ехокардиограма (3) | 18 | 23 | 9 | 6 |
| Диария | 31 | 15 | 23 | 6 |
| Запек | 3 | 10 | 7 | 0 |
| Умора неразположение астения | 15 | 10 | 30 | 5 |
| Атаксия баланс нарушение на походката нарушение на походката | 10 | 10 | 7 | 1 |
| Ненормално поведение | 0 | 8 | 9 | 0 |
| Кръвното налягане се увеличава | 13 | 8 | 0 | 5 |
| Слюнлено хиперсекреция на слюнка | 13 | 8 | 2 | 0 |
| Хипотония | 0 | 8 | 0 | 0 |
| Обрив | 8 | 8 | 5 | 4 |
| Кръвният пролактин се увеличава | 0 | 5 | 0 | 0 |
| Втрисане | 0 | 5 | 2 | 0 |
| Намалена активност | 0 | 5 | 0 | 1 |
| Дехидратация | 0 | 5 | 0 | 0 |
| Безсъние | 0 | 5 | 5 | 2 |
| Пирексия | 15 | 5 | 21 | 14 |
| Стереотипи | 0 | 5 | 0 | 0 |
| Инфекция на горните дихателни пътища | 21 | 5 | 7 | 10 |
| Повръщане | 10 | 5 | 5 | 8 |
| Теглото намалява | 13 | 5 | 7 | 1 |
| Крупа | 5 | 3 | 0 | 1 |
| Ушна инфекция | 8 | 3 | 9 | 5 |
| Гастроентерит | 8 | 3 | 2 | 0 |
| Увеличена сърдечна честота | 5 | 3 | 0 | 2 |
| Раздразнителност | 0 | 3 | 9 | 2 |
| Ринит | 8 | 3 | 7 | 2 |
| Тремор | 3 | 3 | 9 | 0 |
| Уринарна инконтиненция | 5 | 3 | 0 | 0 |
| Намалена кръвна глюкоза | 0 | 0 | 9 | 1 |
| Бронхит | 3 | 0 | 9 | 1 |
| Контузия | 5 | 0 | 0 | 0 |
| Екзема | 0 | 0 | 5 | 0 |
| Enuresis | 5 | 0 | 0 | 0 |
| Падане | 10 | 0 | 0 | 4 |
| Главоболие | 8 | 0 | 0 | 2 |
| Ларингит | 0 | 0 | 5 | 0 |
| Негативизъм | 5 | 0 | 0 | 0 |
| Статус Епилептик | 3 | 0 | 12 | 2 |
| Инфекция на пикочните пътища | 5 | 0 | 5 | 0 |
| Вирусна инфекция | 0 | 0 | 5 | 1 |
| (1) 0,4 mg/kg/ден was not an intermediate dose. Patients on the 0,4 mg/kg/ден dose were also taking concomitant Stiripentol плюс Clobazam which increases exposure of Fintepla. (2) Пациентите в плацебо групи от проучвания 1 и 2 са обединени. (3) Се състои от следи и мека митрална регургитация и проследяване на аортата, които се считат за физиологична |
Синдром на Lennox-Gastaut
В плацебо-контролираното изпитване на пациенти с LGS, приемащи съпътстващ стандарт на грижа за AED (проучване 3) 176 пациенти са лекувани с fintepla, а 87 пациенти са получили плацебо [виж Клинични изследвания ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) и 29% of patients were at least 18 years of age 45% of patients were female и 79% were White. All patients were receiving at least one other AED.
Степента на прекратяване в резултат на нежелана реакция е 6% и 5% за пациенти, лекувани с fintepla 0,7 mg/kg/ден и 0,2 mg/kg/ден съответно в сравнение с 1% за пациентите на плацебо. Най -честите нежелани реакции, водещи до прекратяване на пациентите, лекувани с каквато и да е доза fintepla, са припадък (2%) и сънливост (2%).
Общите нежелани реакции, които се наблюдават при пациенти, лекувани с fintepla (честота най -малко 10% и по -голяма от плацебо), са диария; намален апетит; умора; сънливост; повръщане.
Таблица 5 изброява нежеланите реакции, които са докладвани при 5% или повече от пациенти, лекувани с fintepla и със скорост, по -голяма от тези на плацебо по време на титруването и поддържащите фази на проучване 3.
Таблица 5: Нежелани реакции при 5% или повече от пациентите, лекувани с Fintepla и по-големи от плацебо в плацебо-контролираното изпитване за синдром на Lennox Gastaut (проучване 3)
| Нежелана реакция | Fintepla Dose Group | ||
| Проучване 3 | Плацебо група | ||
| 0,2 mg/kg/ден | 0,7 mg/kg/ден | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Намален апетит | 20 | 36 | 12 |
| Умора неразположение астения | 14 | 24 | 16 |
| Летаргия на седация на сънливост | 12 | 22 | 16 |
| Диария | 11 | 13 | 5 |
| Запек | 6 | 9 | 6 |
| Повръщане | 14 | 8 | 6 |
| Теглото намалява | 2 | 8 | 2 |
| Инфекция на горните дихателни пътища | 8 | 7 | 3 |
| Припадък | 9 | 5 | 7 |
| Раздразнителност | 8 | 3 | 6 |
Ехокардиографски оценки на безопасността на клапните сърдечни заболявания и белодробната артериална хипертония
Вълновите сърдечни заболявания и белодробната артериална хипертония са оценени в проучванията за разширение на плацебококонтролирането и отворената етикет чрез ехокардиография за продължителност до 3 години при пациенти с 341 DS и 263 пациенти с LGS [виж ПредупреждениеS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation и assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
В тези клинични проучвания двама пациенти с LGS проявяват лека аортна регургитация (AR), но нито един пациент е имал сърдечни признаци или симптоми или доказателства за клапна структурни промени.
Нито един пациент не е имал VHD. Степента на леки AR съответства на тези, наблюдавани в периода на скрининг преди лечението (3 пациенти при LGS и 1 пациент в клинични изпитвания на DS).
Опит за постмаркетиране
Следните нежелани реакции са идентифицирани по време на използването на fintepla след придружител. Тъй като тези реакции се отчитат доброволно от популация с несигурен размер, не винаги е възможно надеждно да се оцени тяхната честота или да се установи причинно -следствена връзка с експозицията на лекарства.
Психиатрични разстройства : агресия
Лекарствени взаимодействия for Fintepla
Ефект на други лекарства върху fintepla
Stiripentol плюс Clobazam
Съвместно приложение на fintepla с viripentol плюс clobazam със или без валпроат увеличава плазмените концентрации на фенфлурамин [виж Клинична фармакология ]. If Fintepla is coadministered with Stiripentol плюс Clobazam the maximum daily dosage of Fintepla is 0,2 mg/kg два пъти дневно (maximum daily dosage of 17 mg) [see Доза и приложение ].
Силни CYP1A2 CYP2B6 или CYP3A индуктори
Коадминацията на fintepla със силни CYP1A2 CYP2B6 или CYP3A индукторите ще намалят плазмените концентрации на фенфлурамин, които могат да понижат ефикасността на fintepla [виж Клинична фармакология ].
Препоръчва се да се избегнат съвместно приложение на силни CYP1A2 CYP2B6 или CYP3A индуктори. Ако съвместното приложение на силен CYP1A2 CYP2B6 или CYP3A индуктор с fintepla е необходимо, наблюдавайте пациента за намалена ефикасност и помислете за увеличаване на дозата на fintepla, ако е необходимо; Въпреки това не надвишават максималната дневна доза на fintepla [виж Доза и приложение ].
Ако силен CYP1A2 CYP2B6 или CYP3A индуктор е прекратен по време на поддържащо лечение с fintepla, помислете за постепенно намаляване на дозата на fintepla към дозата, приложена преди започване на индуктора [виж ПредупреждениеS AND PRECAUTIONS ].
Силни инхибитори на CYP1A2 или CYP2D6
Коадминацията на fintepla със силни инхибитори на CYP1A2 или CYP2D6 ще увеличи концентрациите на плазмата на фенфлурамин [виж Клинична фармакология ]. If Fintepla is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of Fintepla is 20 mg [see Доза и приложение ].
Ако инхибиторът на CYP1A2 или CYP2D6 е прекратен по време на поддържащо лечение с fintepla, вземете предвид постепенното увеличаване на дозата на fintepla към дозата, препоръчана без CYP1A2 или CYP2D6 инхибитори; Въпреки това не надвишават максималната дневна доза на fintepla [виж Доза и приложение ].
Ако fintepla е съвместно с Stiripentol и силен CYP1A2 или CYP2D6 инхибитор, не надвишава максималната дневна доза на Fintepla от 17 mg [виж Доза и приложение ].
Ефекти на антагонистите на серотониновите рецептори
Ципрохептадин и мощен 5-HT1A 5-HT1D 5-HT2A и 5-HT2C антагонисти на серотонинови рецептори могат да намалят ефикасността на fintepla. Ако ципрохептадин или мощен 5-HT1A 5-HT1D 5-HT2A или 5-HT2C антагонисти на серотонинови рецептори се съвпадат с пациенти с Fintepla, трябва да бъдат наблюдавани по подходящ начин.
Серотонергични лекарства
Съпътстващо приложение на fintepla и лекарства (напр. SSRIS SNRIS TCAS MAO инхибитори на инхибитори и др.) Лекарства без рецепта (напр. Декстрометорфан) или билкови добавки (напр. ПредупреждениеS AND PRECAUTIONS ]. Concomitant use of Fintepla is contraindicated within 14 days of taking MAOIs. Use Fintepla with caution in patients taking other medications that increase Серотонин.
Предупреждения за Fintepla
Включени като част от 'ПРЕДПАЗНИ МЕРКИ' Раздел
Предпазни мерки за fintepla
Клапна сърдечна болест и белодробна артериална хипертония
Fintepla can cause valvular heart disease (VHD) и pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in Fintepla) и valvular heart disease и pulmonary arterial hypertension. Although no patients receiving Fintepla developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS и LGS of up to 3 years in duration cases of valvular heart disease и pulmonary arterial hypertension have been reported during use of Fintepla in the postmarketing setting [see Предупреждение за кутия и Нежелани реакции ].
Поради този рисков сърдечен мониторинг е необходим преди започване на лечение по време на лечението и след лечението с Fintepla приключва. Сърдечният мониторинг чрез ехокардиограма може да идентифицира доказателства за клапна сърдечна болест и белодробна артериална хипертония, преди пациентът да стане симптоматичен, подпомагащ ранното откриване на тези състояния.
Мониторинг
Преди да започне лечението, пациентите трябва да преминат ехокардиограма, за да се оцени за клапна сърдечна болест и белодробна артериална хипертония.
Ехокардиограмите трябва да се повтарят на всеки 6 месеца и веднъж 3-6 месеца след лечението с Fintepla.
Предписвачът трябва да вземе предвид ползите спрямо рисковете от започване или продължаване на лечението с fintepla, ако някой от следните признаци се наблюдава чрез Echo:
- Клапанна аномалия или нова аномалия чрез ехокардиограма.
- VHD, както е показано чрез лека или по -голяма аортна регургитация или умерена или по -голяма митрална регургитация с допълнителни характеристики на VHD (например удебесяване на клапана или ограничаване на движението на клапана).
- PAH, както е посочено от повишено налягане на дясното сърце/белодробна артерия (PASP> 35 mm Hg).
Fintepla is available only through a restricted program under a REMS [see Fintepla REMS Program ].
Fintepla REMS Program
Fintepla is available only through a restricted distribution program called the Fintepla REMS program because of the risk of valvular heart disease и pulmonary arterial hypertension [see Клапна сърдечна болест и белодробна артериална хипертония ].
Забележителните изисквания на програмата Fintepla REMS включват:
- Предписаните трябва да бъдат сертифицирани, като се запишат в програмата Fintepla REMS.
- Предписващите трябва да съветват пациентите, получаващи Fintepla за риска от клапна сърдечна болест и белодробна артериална хипертония как да се разпознаят признаци и симптоми на клапна сърдечна болест и белодробна артериална хипертония, необходимостта от изходно ниво (предварително лечение) и периодичен сърдечен мониторинг чрез ехокардиограма по време на лечение с финтепла и сърдечно наблюдение след лечение на Fintepla.
- Пациентите трябва да се запишат в програмата REMS и да спазват текущите изисквания за мониторинг [виж Клапна сърдечна болест и белодробна артериална хипертония ].
- Аптеката трябва да бъде сертифицирана чрез записване в програмата REMS и трябва да се освободи само на пациенти, които са упълномощени да получават fintepla.
- Търговците на едро и дистрибуторите трябва да разпространяват само до сертифицирани аптеки.
Допълнителна информация е достъпна на www.finteplarems.com или по телефона на 1-877-964-3649.
Намален апетит и намалено тегло
Fintepla can cause decreases in appetite и weight. In placebo-controlled studies for DS (Проучване 1 и Проучване 2 combined) approximately 37% of patients treated with Fintepla reported as an adverse reaction Намален апетит и approximately 9% reported намалено тегло as compared to 8% и 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Проучване 3) approximately 28% of patients treated with Fintepla reported as an adverse reaction Намален апетит и approximately 5% reported намалено тегло as compared to 15% и 2% respectively of patients on placebo [see Нежелани реакции ]. By the end of the controlled studies 19% (Studies 1 и 2 combined) of DS patients и 7% (Проучване 3) of LGS patients treated with Fintepla had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Проучване 1 и 2) и 0% (Проучване 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on Fintepla 0,7 mg/kg/ден (Проучване 1) 19% of patients on Fintepla 0,4 mg/kg/ден in combination with stiripentol (Проучване 2) и 13% of patients taking Fintepla 0,2 mg/kg/ден (Проучване 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on Fintepla 0,7 mg/kg/ден (Проучване 3) и 6% of patients on Fintepla 0,2 mg/kg/ден (Проучване 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS и most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with Fintepla should be carefully monitored. Weight should be monitored regularly during treatment with Fintepla и dose modifications should be considered if a decrease in weight is observed.
Седация на сънливост и летаргия
Fintepla can cause somnolence седация и летаргия. In controlled studies for DS (Проучване 1 и Проучване 2 combined) the incidence of somnolence седация и летаргия was 25% in patients treated with Fintepla compared with 11% of patients on placebo. In the controlled study for LGS (Проучване 3) the incidence of somnolence седация и летаргия was 19% in patients treated with Fintepla compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Нежелани реакции ].
Други депресанти на централната нервна система (ЦНС), включително алкохол, могат да потенцират тези ефекти на Fintepla. Предписаните трябва да наблюдават пациентите за сънливост и седация и трябва да съветват пациентите да не шофират или експлоатират машини, докато не натрупат достатъчен опит на Fintepla, за да преценят дали това се отразява неблагоприятно върху способността им да управляват или работят с машини.
Самоубийствено поведение и идея
Антиепилептичните лекарства (AED), включително Fintepla, увеличават риска от самоубийствени мисли или поведение при пациенти, приемащи тези лекарства за всякакви индикации. Пациентите, лекувани с AED за каквато и да е индикация, трябва да бъдат наблюдавани за появата или влошаването на депресионните самоубийствени мисли или поведение или всякакви необичайни промени в настроението или поведението.
Събраните анализи на 199 плацебо-контролирани клинични изпитвания (моно- и допълнителна терапия) на 11 различни AED, които не включват fintepla, показват, че пациентите, рандомизирани на един от AEDs, имат приблизително два пъти по-голям от риска (коригиран относителен риск 1,8 95% CI: 1.2 2.7) на суицидално мислене или поведение в сравнение с пациенти, раждащи на плацебо. В тези изпитвания, които имат средна продължителност на лечението от 12 седмици, прогнозната честота на честотата на самоубийствено поведение или идеята сред 27863 пациенти, лекувани с AED, е 0,43% в сравнение с 0,24% сред 16029 пациенти, лекувани с плацебо, представляващи увеличение на приблизително един случай на самоубийствено мислене или поведение при всеки 530 пациенти, лекувани. Имаше четири самоубийства при пациенти, лекувани с лекарства при изпитванията и нито един при пациенти, лекувани с плацебо, но броят им е твърде малък, за да позволи някакъв заключение за лекарствения ефект върху самоубийството.
Повишеният риск от самоубийствени мисли или поведение с AED се наблюдава още 1 седмица след стартиране на лечение с лекарства с AED и се запазва за продължителността на оцененото лечение. Тъй като повечето изпитвания, включени в анализа, не се простират след 24 седмици, рискът от самоубийствени мисли или поведение след 24 седмици не може да бъде оценен.
Рискът от самоубийствени мисли или поведение като цяло е последователен сред лекарствата в анализираните данни. Откриването на повишен риск с AED с различни механизми на действие и в редица показания предполага, че рискът се прилага за всички AED, използвани за всякакви индикации. Рискът не варира значително до възраст (5-100 години) в анализираните клинични изпитвания. Таблица 3 показва абсолютен и относителен риск чрез индикация за всички оценени AED.
Таблица 3: Риск от самоубийствени мисли или поведение чрез индикация за антиепилептични лекарства при обединения анализ
| Индикация | Пациенти с плацебо със събития на 1000 пациенти | Пациенти с лекарства със събития на 1000 пациенти | Относителен риск: честота на събитията при пациенти с лекарства/ честота при пациенти с плацебо | Разлика на риска: Допълнителни пациенти с лекарства със събития на 1000 пациенти |
| Епилепсия | 1.0 | 3.4 | 3.5 | 2.4 |
| Психиатрична | 5.7 | 8.5 | 1.5 | 2.9 |
| Други | 1.0 | 1.8 | 1.9 | 0.9 |
| Общо | 2.4 | 4.3 | 1.8 | 1.9 |
Относителният риск от самоубийствени мисли или поведение е бил по -висок при клиничните изпитвания при пациенти с епилепсия, отколкото при клинични изпитвания при пациенти с психиатрични или други състояния, но абсолютните различия в риска са сходни за епилепсията и психиатричните показания.
Всеки, който обмисля да предпише fintepla или друг AED, трябва да балансира риска от самоубийствени мисли или поведение с риск от нелекувани заболявания. Епилепсията и много други заболявания, за които са предписани AED, са самите свързани с заболеваемост и смъртност и повишен риск от самоубийствени мисли и поведение. Ако по време на лечението се появят самоубийствени мисли и поведение, помислете дали появата на тези симптоми при даден пациент може да бъде свързано с болестта, която се лекува.
Оттегляне на антиепилептични лекарства
Както при повечето AED Fintepla обикновено трябва да се изтегля постепенно поради риска от повишена честота на припадъци и епилептик на състоянието. Ако е необходимо оттегляне поради сериозна нежелана реакция, може да се вземе предвид бързото прекратяване.
Синдром на Серотон
Синдром на серотонин може да възникне потенциално животозастрашаващо състояние с fintepla, особено при съпътстващо приложение на fintepla с други серотонинергични лекарства, включително, но не само селективно серотонин-норепинефрин затискащи инхибитори на серотонина-норепипинефрин (SNRIS) селективни инхибитори на серотонина (SSRIS) селективни инхибитори на серотонина (SSRIS) (SSRIS) селективни инхибитори на серотонина (SSRIS) (SSRIS)) селективни инхибитори на серотонина (SSRIS) (SSRIS) (SSRIS) (SSRIS) инхибитори на SSRIS) (SSRIS) (SSRIS) (SSRIS) (SSRIS) инхибитори на трициклис)) антидепресанти (TCAS) Bupropion Triptans Диетични добавки (напр. Сейнт Джонс Триптофан) Лекарства, които нарушават метаболизма на серотонин (включително инхибитори на моноаминооксидазата [MAOI], които са противопоказани с финтепли [виж Противопоказания ] Dextromethorphan Литиев трамадол и антипсихотици със серотонинергична агонистка активност. Patients should be monitored for the emergence of signs and symptoms of serotonin syndrome which include mental status changes (e.g. agitation hallucinations coma) autonomic instability (e.g. tachycardia labile blood pressure hyperthermia) neuromuscular signs (e.g. hyperreflexia incoordination) and/or gastrointestinal symptoms (e.g. nausea vomiting diarrhea). Ако синдромът на серотонин се подозира, че лечението с Fintepla трябва да бъде спряно незабавно и трябва да се започне симптоматично лечение.
Увеличаване на кръвното налягане
Fintepla can cause an increase in blood pressure [see Нежелани реакции ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving Fintepla developed a hypertensive crisis. Monitor blood pressure in patients treated with Fintepla.
Глаукома
Fenfluramine може да причини мидриаза и да утаи затварянето на ъгъла глаукома . Помислете за прекратяване на лечението с fintepla при пациенти с остро намаляване на зрителната острота или очната болка.
Информация за консултирането на пациентите
Посъветвайте се на пациента да прочете одобреното от FDA етикетиране на пациента ( Ръководство за лекарства и Instructions for Use ).
Информация за администрацията
Посъветвайте се на пациенти, на които се предписват Fintepla, да използват спринцовите с устно дозиране, предоставени от аптеката [виж Доза и приложение и Инструкции за употреба ]. Instruct patients to discard any unused Fintepla 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Колко се доставя ].
Клапна сърдечна болест и белодробна артериална хипертония
Съветвайте пациентите, че сърдечният мониторинг трябва да се извърши с помощта на ехокардиография, за да се наблюдават сериозни промени в сърдечния клапан или високо кръвно налягане в артериите на белите дробове [виж ПредупреждениеS AND PRECAUTIONS ].
Fintepla REMS Program
Fintepla is available only through a restricted program called the Fintepla REMS program [see ПредупреждениеS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- Пациентите трябва да се запишат в програмата и да спазват текущите изисквания за мониторинг на ехокардиограмата [виж ПредупреждениеS AND PRECAUTIONS ].
Fintepla is only prescribed by certified health care providers и only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number и website for information on how to obtain the product [see ПредупреждениеS AND PRECAUTIONS ].
Намален апетит и намалено тегло
Посъветвайте пациентите, че намаленият апетит е често по време на лечението с fintepla, което може да причини намаляване на теглото [виж ПредупреждениеS AND PRECAUTIONS ].
Седация на сънливост и летаргия
Информирайте пациентите, че fintepla могат да причинят седация на сънливост и летаргия. Внимавайте пациентите относно експлоатацията на опасни машини, включително моторните превозни средства, докато не са разумно сигурни, че Fintepla не ги засяга неблагоприятно (напр. Уврежда се в преценката мислене или двигателни умения) [виж ПредупреждениеS AND PRECAUTIONS ].
Самоубийствено мислене и поведение
Съветвайте пациентите, които се грижат за тях, и техните семейства, че антиепилептичните лекарства могат да увеличат риска от самоубийствени мисли и поведение и да ги посъветват да бъдат нащрек за появата или влошаването на симптомите на депресия всякакви необичайни промени в настроението или поведението или спестяването на самоубийствени мисли поведение или мисли за самохар. Инструктирайте пациентите, които се грижат за тях ПредупреждениеS AND PRECAUTIONS ].
Оттегляне на антиепилептични лекарства (AEDs)
Посъветвайте се с пациентите да не прекратяват употребата на fintepla, без да се консултирате със своя доставчик на здравни грижи. Fintepla обикновено трябва постепенно да се изтегля, за да се намали потенциала за повишена честота на припадъци и епилептик на състоянието [виж Доза и приложение и ПредупреждениеS AND PRECAUTIONS ].
Синдром на Серотон
Информирайте пациентите за риска от синдром на серотонин, който може да бъде животозастрашаващ. Посъветвайте пациентите за признаците и симптомите на синдрома на серотонин и че някои лекарства без рецепта и билкови добавки могат да увеличат този риск [виж ПредупреждениеS AND PRECAUTIONS ].
Увеличаване на кръвното налягане
Информирайте пациентите, че fintepla може да доведе до повишаване на кръвното налягане [виж ПредупреждениеS AND PRECAUTIONS ].
Глаукома
Информирайте пациентите, че fintepla могат да причинят мидрааза и могат да утаяват глаукома за затваряне на ъгъла.
Инструктирайте пациентите да се свържат с техния доставчик на здравни грижи, ако имат остри намаления на зрителната острота или очна болка [виж ПредупреждениеS AND PRECAUTIONS ].
Регистър на бременността
Посъветвайте пациентите да уведомят своя доставчик на здравни грижи, ако забременеят или възнамеряват да забременеят по време на терапията с Fintepla. Насърчавайте жените, които приемат Fintepla, да се запишат в регистъра на бременността в Северна Америка (NAAED), ако забременеят.
Този регистър събира информация за безопасността на антиепилептичните лекарства по време на бременност [виж Използване в конкретни популации ].
Неклинична токсикология
Канцерогенеза мутагенеза Нарушаване на плодовитостта
Карциногенеза
Перорално приложение на мишки от фенфлурамин до tg.rash2 (0 4.3 13.0 34.6 или 51,8 mg/kg/ден) в продължение на 26 седмици и на мъжки и женски плъхове (0 0.9 2.2 или 6.9 mg/kg/ден) за всеки от 89 и 97 седмици, които не доведоха до доказателства за индуцирани от лекарства тумори при всеки вид. При плазмените експозиции на плъхове (AUC) на фенфлурамин и норфенфлурамин (основният метаболит) при най -високата тествана доза са приблизително 5 и 11 пъти съответно тези при хората при максимално препоръчаната доза на човека (MRHD) от 26 mg/ден.
Мутагенеза
Fenfluramine е отрицателен в in vitro бактериална мутация (AMES) анализ и an напразно Микронуклеус и анализ на кометата при плъхове.
Увреждане на плодовитостта
Oral administration of fenfluramine (0 3.0 6.9 or 17.3 mg/kg/day) to male and female rats prior to and throughout mating and continuing in females to day 7 of gestation resulted in a decrease in fertility and increases in abnormal sperm and epithelial vacuolation of the epididymis at the highest dose tested and altered estrous cyclicity decreased corpora lutea and implantations и повишена ембриолеталност в средната и високата доза. Тези дози са свързани с родителска токсичност. Дозите без ефект за неблагоприятни ефекти върху плодовитостта и репродуктивните показатели при плъхове (NULL,9 и 3,0 mg/kg/ден при мъже и жени съответно) са свързани с плазмените експозиции на фенфлурамин (AUC) приблизително съответно 3 и 0,6 пъти съответно и норфенфлурамин експозиции приблизително 5 и 3 пъти повече от това при излагане на HUS.
Използване в конкретни популации
Бременност
Бременност Exposure Registry
Съществува регистър на експозицията на бременност, който следи резултатите от бременността при жени, изложени на антиепилептични лекарства (AED), като Fintepla по време на бременност. Насърчете жените, които приемат Fintepla по време на бременността, да се запишат в регистъра на бременността в Северна Америка (NAAED), като се обадите на безплатния номер 1-888-233-2334 или посещавате https://www.aedpregnancygistrygry.org.
Обобщение на риска
Няма данни за употребата на fintepla при бременни жени. Наличните данни от епидемиологични проучвания с фенфлурамин или дексфенфлурамин са недостатъчни за оценка на асоцииран с лекарства риск от основни вродени дефекти спонтанен аборт или други неблагоприятни резултати от майката или плода. Fintepla може да причини намален апетит и намалено тегло [виж ПредупреждениеS AND PRECAUTIONS ]; Монитор за адекватно наддаване на тегло по време на бременност. In animal studies administration of fenfluramine throughout organogenesis (rat and rabbit) or throughout gestation and lactation (rat) resulted in adverse effects on development (fetal malformations embryofetal and offspring mortality and growth impairment) in the presence of maternal toxicity at clinically relevant maternal plasma levels of fenfluramine and its major active metabolite (see Данни ).
Прогнозният фонов риск от големи вродени дефекти и спонтанен аборт за посоченото население е неизвестен. Всички бременности имат основен риск от вроден дефект загуба или други неблагоприятни резултати. В общата популация на САЩ прогнозният фонов риск от големи вродени дефекти и спонтанен аборт в клинично признатите бременности е съответно от 2 до 4% и 15 до 20%.
Данни
Данни за животните
Оралното приложение на фенфлурамин (0 4,5 8,6 или 34,6 mg/kg/ден) на бременни плъхове по време на органогенезата доведе до намаляване на телесното тегло на плода и значително увеличение на тестваните от плода малформации (външна висцерална и скелетна) при най -високата тествана доза, която е свързана с майчината на майчината. При доза без ефект (NULL,6 mg/kg/ден) за неблагоприятни ефекти върху развитието на ембриофеталното развитие при плъхове на плазмената експозиция на майката (AUC) на фенфлурамин и норфенфлурамин (основният метаболит) са приблизително 2 и 5 пъти съответно тези при хора при максимално препоръчаната човешка доза (MRHD) от 26 mg/ден.
Оралното приложение на фенфлурамин (0 4.3 8.6 13.0 mg/kg/ден) на бременни зайци по време на органогенезата доведе до повишена смъртност на ембриофеталната смърт при всички дози и увеличаване на феталните малформации (външна и скелетна) при най -високата тествана доза, която е свързана с майчината токсичност. Не е идентифицирана доза без актуални ефекти за неблагоприятни ефекти върху развитието на ембриофетала при зайци. При най -ниската доза, тествана при зайци (NULL,3 mg/kg/ден) плазма на майката на фенфлурамин и норфенфлурамин, са по -ниски от тези при хората при МРХ.
Устното прилагане на фенфлурамин (0 4.3 86 или 34,6 mg/kg/ден) на женски плъхове по време на гестацията и лактацията доведе до значително увеличение на мъртвородените кученца и неонаталното потомство при смъртта на най -високата доза и забавяне на растежа и рефлексното развитие по време на преобладаващия период на всички дози. Наддаването на телесно тегло на майката е намалено при всички дози по време на бременност и при двете най -високи дози по време на лактация. Не е определена доза без ефект за неблагоприятни ефекти върху преди и следродилното развитие при плъхове. При най -ниската доза, тествана при плъхове (NULL,3 mg/kg/ден) плазма на майката на фенфлурамин и норфенфлурамин, са приблизително 0,5 и 3 пъти съответно тези при хора при MRHD.
Лактация
Обобщение на риска
Няма данни за наличието на фенфлурамин или неговите метаболити в човешкото мляко ефектите върху кърменото кърмаче или ефектите върху производството на мляко.
Ползите за развитие и здравето от кърменето трябва да се разглеждат заедно с клиничната нужда от Fintepla на майките и всякакви потенциални неблагоприятни ефекти върху кърменото бебе от Fintepla или от основното състояние на майката.
Жени и мъже с репродуктивен потенциал
Безплодие
При изследвания на животни оралното приложение на фенфлурамин доведе до неблагоприятни репродуктивни ефекти при мъже и жени при клинично значими дози при наличие на родителска токсичност [виж Неклинична токсикология ].
Педиатрична употреба
Безопасността и ефективността на fintepla за лечение на припадъци, свързани с DS и LGS, са установени при пациенти на 2 и повече години.
Използването на fintepla за лечение на припадъци, свързани с DS при пациенти на 2 и повече години, се подкрепя от две рандомизирани двойно-слепи плацебо-контролирани проучвания при 202 пациенти на възраст 2 до 18 години. Използването на fintepla за лечение на припадъци, свързани с LGS, се подкрепя от рандомизирано двойно-сляпо плацебо-контролирано проучване при 263 пациенти на възраст от 2 до 35 години, включително 187 пациенти по-малко от 18 години [виж Предупреждение за кутия ПредупреждениеS AND PRECAUTIONS Нежелани реакции и Клинични изследвания ].
Fintepla can cause decreases in appetite и weight. The growth of pediatric patients treated with Fintepla should be carefully monitored.
Безопасността и ефективността при пациенти на възраст под 2 години не са установени.
Данни за непълнолетни животни
Оралното приложение на фенфлурамин (0 3.0 78 или 17,3 mg/kg/ден) на млади плъхове в продължение на 10 седмици, започващи на следродилния ден 7, доведе до намалено телесно тегло и невроби -поведенчески промени (намалена локомоторна активност и учене и дефицит на паметта) при всички тествани дози. Невробихевиоралните ефекти продължават след дозиране, се прекратяват. Размерът на костите е намален в средната и високите дози; Размерът на мозъка е намален при най -високата доза. Частично или пълно възстановяване се наблюдава за тези крайни точки. Не е идентифицирана доза без ефект за постнатална токсичност за развитие. Тестваната с най -ниска доза (NULL,0 mg/kg/ден) се свързва с плазмените експозиции на фенфлурамин (AUC) по -малко от тази при хората при максимална препоръчителна доза на човека (MRHD) от 26 mg/ден и норфенфлурамин (метаболит) експозиция (AUC) приблизително 2 пъти по -голяма от тази в MRHD.
Гериатрична употреба
Клиничните проучвания на Fintepla за лечение на DS или LGS не включват пациенти на 65 години и повече, за да се определи дали реагират различно от по -младите пациенти. Като цяло изборът на доза за възрастен пациент трябва да бъде предпазлив обикновено, като се започне от ниския край на обхвата на дозиране, отразяващ по -голямата честота на намалена чернодробна бъбречна или сърдечна функция и на съпътстваща болест или друга лекарствена терапия.
Дългосрочни странични ефекти на невронтина
Бъбречно увреждане
При пациенти с прогнозна скорост на гломерулна филтрация (EGFR) 15 до 29 ml/min/1,73m 2 Не надвишавайте максималната дневна доза на Fintepla от 20 mg. При пациенти с EGFR 15 до 29 ml/min/1,73m 2 и concomitant stiripentol use do not exceed the maximum daily dosage of Fintepla of 17 mg [see Доза и приложение и Клинична фармакология ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Чернодробно увреждане
Комбинираните моларни експозиции на фенфлурамин и норфенфлурамин се увеличават при лица с различни степени на чернодробно увреждане (детско-пух от клас B и C), налагащи корекция на дозата при тези пациенти [виж Доза и приложение и Клинична фармакология ].
Информация за предозиране за fintepla
Не е наблюдавано предозиране в програмата за клинични изпитвания на Fintepla. Обаче предозиране на фенфлурамин Активната съставка във Fintepla се съобщава при по -високи дози от тези, включени в програмата за клинични изпитвания. Някои от случаите бяха фатални. Събитията, отчетени след предозиране, включват мидриаза тахикардия за промиване на тремори/потрепване/мускулни спазми разбъркване/неспокойствие/тревожност повишен мускулен тонус/строгост/опихотонос респираторен дистрес или неуспех и припадък. Пристъпи на кома и кардиореспираторен арест са докладвани в повечето фатални предозиране.
Няма наличен специфичен антидот срещу реакциите на предозиране на fintepla. В случай на предозиране със стандартна медицинска практика за управление на предозиране на лекарства. Трябва да се осигури адекватна оксигенация и вентилация на дихателните пътища; Препоръчва се мониторинг на сърдечния ритъм и измерване на жизнените знаци. За актуализирана информация за управлението на предозиране с Fintepla трябва да се свърже с сертифициран център за контрол на отрови.
Противопоказания за fintepla
Fintepla is contraindicated in patients with:
- Свръхчувствителност към фенфлурамин или някой от помощните вещества във fintepla [виж Описание ]
- Едновременна употреба или в рамките на 14 дни след прилагането на моноаминово оксидазна инхибитори поради повишен риск от синдром на серотонин [виж ПредупреждениеS AND PRECAUTIONS ]
Клинична фармакология for Fintepla
Механизъм на действие
Точният механизъм, чрез който фенфлураминът упражнява своите терапевтични ефекти при лечението на припадъци, свързани със синдрома на Дрейвет и синдрома на Lennox-Gastaut, не е известен. Фенфлураминът и метаболитът норфенфлурамин проявяват агонистка активност при серотонин 5-HT2 рецептори. Съществува връзка между серотонинергични лекарства с 5-HT2B рецепторна агонистка активност, включително фенфлурамин и норфенфлурамин и клапна сърдечна болест и белодробна артериална хипертония.
Фармакодинамика
Сърдечна електрофизиология
В доза 4 пъти повече от максималната препоръчителна доза fintepla не удължи QT интервала, когато се тества при възрастна популация.
Фармакокинетика
Фармакокинетиката на фенфлурамин и норфенфлурамин е проучена при здрави пациенти при педиатрични пациенти с DS и при педиатрични и възрастни пациенти с LGS. Стационарната системна експозиция (CMAX и AUC) на фенфлурамин е малко по-голяма от пропорционалната доза в диапазона на дозата от 13 до 51,8 mg два пъти дневно фенфлурамин (т.е. 1 до 4 пъти повече от максималната препоръчителна доза). При педиатрични пациенти с DS, които са получили fintepla 0,7 mg/kg/ден до обща дневна доза от 26 mg fenfluramine, геометричната средна стабилно състояние на фенфлурамин (коефициент на вариация) е 68,0 (41%) ng/ml и AUC0-24H е 1390 (44%) Ng*H/ML.
Абсорбция
Fenfluramine има време за максимална плазмена концентрация (TMAX) от 3 до 5 часа в стабилно състояние. Абсолютната бионаличност на фенфлурамин е приблизително 68-74%. Няма ефект на храната върху фармакокинетиката на фенфлурамин или норфенфлурамин.
Разпределение
Геометричната средна стойност (CV%) очевиден обем на разпределение (VZ/F) на фенфлурамин е 11,9 (NULL,5%) L/kg след перорално приложение на Fintepla при здрави индивиди. Fenfluramine е 50% обвързан с човешки плазмени протеини in vitro и binding is independent of drug concentrations.
Елиминиране
Елиминиращият полуживот на фенфлурамин е 20 часа, а геометричната средна стойност (CV%) клирънс (CL/F) е 24,8 (29%) L/H след перорално приложение на Fintepla при здрави индивиди.
Метаболизъм
Над 75% от фенфлурамин се метаболизира до норфенфлурамин преди елиминирането предимно от CYP1A2 CYP2B6 и CYP2D6. Други CYP ензими, участващи в малка степен, са CYP2C9 CYP2C19 и CYP3A4/5. Както фенфлураминът, така и норфенфлураминът са фармакологично активни. Норфенфлураминът е допълнително деаминиран и окислен, за да образува неактивни метаболити.
Екскреция
По -голямата част от орално приложената доза фенфлурамин (по -голяма от 90%) се отделя в урината като фенфлурамин норфенфлурамин или други метаболити с фенфлурамин и норфенфлурамин, представляващ по -малко от 25% от общия брой; По -малко от 5% се намира в изпражненията.
Специфични популации
Ефектът от възрастта (диапазон: 2 до 50 години) полът и расата нямат клинично значим ефект върху фармакокинетиката на фенфлурамин.
Пациенти с бъбречно увреждане
В специализирано клинично проучване, сравняващо фармакокинетиката на една доза 0,35 mg/kg fintepla при лица с тежко бъбречно увреждане (EGFR <30 mL/min/1.73m 2 Определени от MDRD) и съвпадащи здрави доброволци CMAX и AUC0-INF на фенфлурамин се увеличават съответно с 20% и 88%, а CMAX и AUC0-INF на норфенфлурамин съответно се увеличават с 13% и 21% при пациенти с тежко бъбречно уплътнение [вж. Използване в конкретни популации ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 (определено от MDRD). Не е известно дали фенфлураминът или норфенфлураминът е диализируем.
Пациенти с чернодробно увреждане
В проучване, сравняващо фармакокинетиката на една доза от 0,35 mg/kg fintepla при лица с леко умерено или тежко чернодробно увреждане (детско-пух от клас A B или C) и лица с нормална чернодробна функция AUC0-T на фенфлурамин се увеличават с 95% 113% и 185% при субекти с меки с мек и северно-непатични съответно. CMAX на фенфлурамин се увеличава с 19% 16% и 29% при лица съответно с леко умерено и тежко чернодробно увреждане. AUC0-T на норфенфлурамин се увеличава с 18% при леко чернодробно увреждане 4% при умерено чернодробно увреждане и намалява с 11% при тежко чернодробно увреждане. CMAX на норфенфлурамин намалява с 21% 36% и 45% при лица съответно с леко умерено и тежко чернодробно увреждане. Комбинираният моларен AUC0-T на фенфлурамин и норфенфлурамин се увеличава с 55% 56% и 82% при лица съответно с леко умерено и тежко чернодробно увреждане. Комбинираният моларен CMAX на фенфлурамин и норфенфлурамин нараства със 7,5% 1,3% и 8% при лица съответно с леко умерено и тежко чернодробно увреждане. Максималната дневна доза на fintepla трябва да бъде намалена при пациенти с леко чернодробно увреждане с/без viripentol плюс clobazam. Максималната дневна доза на fintepla трябва да бъде намалена при пациенти с умерено или тежко чернодробно увреждане без viripentol плюс clobazam [виж Доза и приложение и Използване в конкретни популации ].
Проучвания за взаимодействие с лекарства
Клинични изследвания
Ефект от единична доза Clobazam на Stiripentol и комбинация от валпроева киселина
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination in healthy volunteers increased the AUC0-inf of fenfluramine by 69% and the Cmax by 18% and decreased the AUC0-72 hours of norfenfluramine by 41% and the Cmax by 42% as compared to FINTEPLA администриран самостоятелно.
Ефект на стабилно State Stiripentol плюс Clobazam със или без валпроат
Фенфлураминните фармакокинетични данни се събират от пациенти след получаване на множество администриране на фенфлурамин в проучване 1, както и проучване 2. Популационното фармакокинетично моделиране и симулация са използвани за оценка на ефекта на Stiripentol плюс Clobazam с или без валпроат върху фармакокинетиката на фенфлурамин. Ефектът на Clobazam на Stiripentol плюс с или без валпроат върху фармакокинетиката на фенфлурамин е по-голям, когато Fintepla е в стабилно състояние, отколкото за първата доза Fintepla. At steady state in the patient population the coadministration of 0.1 mg/kg twice daily (0.2 mg/kg/day) maximum 17 mg/day of FINTEPLA with stiripentol plus clobazam with or without valproate is expected to result in a 166% increase in fenfluramine AUC0-24 and a 38% decrease in norfenfluramine AUC0-24 as compared to 0.2 mg/kg/ден максимум 26 mg/ден доза fintepla, прилагана самостоятелно [виж Доза и приложение и Лекарствени взаимодействия ].
Ефект на стационарно канабидиол
Коадминацията на единична 0,35 mg/kg доза fintepla с многократни дози канабидиол повишава AUC0-inf на фенфлурамин с 59% и CMAX с 10% и намалява AUC0-inf на Norfenfluramine с 22% и CMAX с 33% в сравнение с финфлурамин самостоятелно. Не се очаква това взаимодействие да бъде клинично значимо.
Ефект на силни CYP1A2 или CYP2D6 инхибитори
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with fluvoxamine (a strong CYP1A2 inhibitor) at steady state (50 mg once daily) in healthy volunteers increased the AUC0- inf of fenfluramine by 102% and the Cmax by 22% and decreased the AUC0-inf of norfenfluramine by 22% and the Cmax by 44% as compared to Fintepla, администриран самостоятелно [виж Лекарствени взаимодействия ].
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with paroxetine (a strong CYP2D6 inhibitor) at steady state (30 mg once daily) in healthy volunteers increased the AUC0-inf of fenfluramine by 81% and the Cmax by 13% and decreased the AUC0-inf of norfenfluramine by 13% and the Cmax by 29% as compared to Fintepla, администриран самостоятелно [виж Лекарствени взаимодействия ].
Ефект на силни индуктори на CYP1A2 CYP2B6 или CYP3A
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with rifampin (a CYP1A2 CYP2B6 and CYP3A inducer) at steady state (600 mg once daily) in healthy volunteers decreased the AUC0-inf of fenfluramine by 58% and the Cmax by 40% and decreased the AUC0-inf of norfenfluramine by 50% and increased the Cmax на Norfenfluramine с 13% в сравнение с Fintepla, прилаган самостоятелно [виж Лекарствени взаимодействия ].
Ефект на fintepla върху други лекарства
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination did not affect the pharmacokinetics of stiripentol nor the pharmacokinetics of clobazam or its N.desmethyl-metabolite norclobazam nor the pharmacokinetics of valproic acid as compared to the самостоятелна комбинация на Clobazam и валпроева киселина самостоятелно. Коадминацията на единична доза 0,35 mg/kg финтепли с многократни дози канабидиол не влияе на фармакокинетиката на канабидиола в сравнение само с канабидиола.
In vitro изследвания
Фенфлураминът се метаболизира предимно от CYP1A2 CYP2B6 и CYP2D6 in vitro . Други CYP ензими, участващи в малка степен, са CYP2C9 CYP2C19 и CYP3A4/5.
Ефект на фенфлурамин и норфенфлурамин върху CYP субстрати: фенфлурамин и норфенфлурамин не са инхибитори или индуктори на CYP1A2 CYP2B6 CYP2C8 CYP2C9 CYP2C19 CYP2D6 или CYP3A4 при клинично уместни концентрации.
Ефект на транспортери върху фенфлурамин и норфенфлурамин: фенфлурамин и норфенфлурамин не са субстрати на P-G BCRP OAT1 OAT3 OCT2 Mate1 или Mate2-K Transporters.
Ефект на fintepla върху транспортиращите: fenfluramine и norfenfluramine не са инхибитори на P-gp BCRP OAT1B1 OATP1B3 OAT1 OAT3 OCT2 Mate1 или Mate2-K Transporters.
Клинични изследвания
Синдром на Дрейвет
Ефективността на fintepla за лечение на припадъци, свързани с DS при пациенти на 2 и повече години, е установена в две рандомизирани двойно-слепи плацебо-контролирани проучвания при пациенти на възраст от 2 до 18 години.
Проучване 1 (N=117) compared a 0,7 mg/kg/ден и a 0,2 mg/kg/ден dose of Fintepla with placebo in patients who were not receiving stiripentol (NCT02682927 и NCT02826863).
Проучване 2 (N=85) compared a 0,4 mg/kg/ден dose of Fintepla with placebo in patients who were receiving stiripentol и either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS и were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic и focal with observable motor signs. The baseline period was followed by rиomization into a 2- week (Проучване 1) or 3-week (Проучване 2) titration period и a subsequent 12-week maintenance period where the dose of Fintepla remained stable.
В проучване 1 98% от пациентите са приемали между 1 и 4 съпътстващи AED. Най -често използваните съпътстващи AED (при поне 25%от пациентите) са валпроат (61%) Clobazam (59%) и топирамат (25%). В проучване 2 100% от пациентите приемат между 2 и 4 съпътстващи AED. Най -често използваните съпътстващи AED (при най -малко 25%от пациентите) са Clobazam (94%) и валпроат (89%).
Основната крайна точка на ефикасността и в двете проучвания е промяната от изходното ниво на честотата на конвулсивните припадъци на 28 дни по време на комбинираните 14-седмични (проучване 1) или 15-седмично (проучване 2) периоди на титруване и поддържане (т.е. период на лечение). Оценява се и средният най -дълъг интервал между конвулсивните припадъци.
В проучване 1 и проучване 2 намаляването на конвулсивната честота на пристъпите на 28 дни е статистически значително по -голямо за всички дозови групи на Fintepla в сравнение с плацебо (Таблица 6). Наблюдава се намаляване на конвулсивните припадъци в рамките на 3 до 4 седмици след стартирането на Fintepla и ефектът остава като цяло последователен през 14- или 15-седмичния период на лечение.
Таблица 6: Промяна в конвулсивната честота на припадъци по време на пациентите с лечение със синдром на Дрейве (проучване 1 и проучване 2)
| Конвулсивна честота на припадък (на 28 дни) | Плацебо | Fintepla 0,2 mg/kg/ден | Fintepla 0,7 mg/kg/ден | Fintepla 0,4 mg/kg/ден |
| Проучване 1 | N = 39 | N = 38 | N = 40 | Na |
| Основен период средна | 29.4 | 18.1 | 18.7 | Na |
| % Разлика в сравнение с плацебо* | -31.7% | -70.0% | Na | |
| p-стойност в сравнение с плацебо | 0.043 | <0.001 | ||
| Проучване 2 | N = 42 | Na | Na | N = 43 |
| Основен период средна | 11.5 | Na | Na | 15.0 |
| % Разлика в сравнение с плацебо* | Na | -59,5% | ||
| p-стойност в сравнение с плацебо | <0.001 | |||
| *Извлечен от модела на първичния анализ ± Всички 0,4 mg/kg/ден пациенти също приемат съпътстващ Stiripentol, което увеличава излагането на fintepla. |
Фигура 1 и Фигура 2 показват процента на пациентите по категория на реакция на припадъци от изходното ниво в конвулсивна честота на припадъци (на 28 дни) през периода на лечение в проучване 1 и проучване 2 съответно.
Фигура 1: Пропорция на пациентите по категория отговор на припадъци за Fintepla и плацебо при пациенти със синдром на Дрейве (проучване 1)
| |
Фигура 2: Пропорция на пациентите по категория отговор на припадъци за Fintepla и плацебо при пациенти със синдром на Дрейве (проучване 2)
| |
В проучване 1 3 от 40 (8%) пациенти във Fintepla 0,7 mg/kg/дневна група и 3 от 38 (8%) пациенти във Fintepla 0,2 mg/kg/ден група съобщават, че няма конвулсивни припадъци през 14-седмичния период на лечение в сравнение с 0 пациенти в плацебо групата. В проучване 2 1 от 43 (2%) пациенти в групата на Fintepla 0,4 mg/kg/ден съобщават, че няма конвулсивни припадъци през 15-седмичния период на лечение в сравнение с 0 пациенти в плацебо групата.
В проучване 1 и проучване 2 fintepla се свързва със статистически значим по -дълъг интервал между конвулсивни припадъци в сравнение с плацебо (Фигура 3).
Фигура 3: Среден най -дълъг интервал между конвулсивни припадъци при пациенти със синдром на Дравет (проучване 1 и проучване 2)
| |
Синдром на Lennox-Gastaut
Ефективността на fintepla за лечение на припадъци, свързани с LGS при пациенти на 2 и повече години, е установена в рандомизирано двойно-сляпо плацебо-контролирано проучване при 263 пациенти на възраст 2 до 35 години (проучване 3; NCT03355209).
Проучване 3 compared a 0,7 mg/kg/ден и a 0,2 mg/kg/ден dose of Fintepla with placebo.
Пациентите са имали диагноза LGS и са били недостатъчно контролирани на поне един AED с или без вагулен нервен стимулация и/или кетогенна диета. Проучването е имало 4-седмичен базов период, през който пациентите са били длъжни да имат минимум 8 капки припадъци, докато са на стабилна AED терапия. Припадъците на капки бяха генерализирани тонично-клонични вторично генерализирани тонично-клонични тонични атонични или тонични атонични припадъци, които бяха потвърдени, че водят до капки. Основният период е последван от рандомизация в двуседмичен период на титруване и последващ 12-седмичен период на поддържане, при който дозата на Fintepla остава стабилна.
В проучване 3 99% от пациентите са приемали между 1 и 4 съпътстващи AED. Най -често използваните съпътстващи AED (при поне 25%от пациентите) са ламотригин (34%) и валпроат (56%).
Основната крайна точка на ефикасността в проучване 3 е средната процентна промяна от изходното ниво на честотата на пристъпите на спад на 28 дни през комбинираните 14-седмични периоди на титруване и поддържане (т.е. период на лечение). Делът на пациентите, които постигат подобрение (минимално много или много подобрени) в клиничното глобално впечатление за промяна (CGI-I), оценени от главния изследовател, е вторична крайна точка.
В проучване 3 средната процентна промяна от изходното ниво (намаляване) на честотата на пристъпите на спад на 28 дни е значително по -голяма за 0,7 mg/kg/дневна доза група fintepla в сравнение с плацебо (Таблица 7). Наблюдава се намаляване на пристъпите на спад в рамките на 2 седмици след започване на лечение с Fintepla и ефектът остава като цяло последователен през 14-седмичния период на лечение.
Средният процент намаление от изходното ниво на честота на припадъци на спад на 28 дни за по -ниската доза Fintepla (NULL,2 mg/kg/ден) не достига статистическа значимост в сравнение с плацебо (Таблица 7).
Таблица 7: Промяна на честотата на припадъци по време на периода на лечение при пациенти с синдрома на Lennox-Gastaut (проучване 3)
| Честота на припадък (на 28 дни) | Плацебо | Fintepla 0,2 mg/kg/ден | Fintepla 0,7 mg/kg/ден |
| Проучване 3 | N = 85* | N = 86* | N = 83* |
| Основен период средна Припадък Frequency | 55.0 | 77.8 | 80.0 |
| Среден процент промяна от изходното ниво по време на лечението | -8.7% | -13.2% | -23,7% |
| p-стойност в сравнение с плацебо | 0.1917 | 0.0037 | |
| *Общият брой на пациентите, на които се основава анализът на ефикасността, е по-малък от общия брой, рандомизиран в двойно-сляпото плацебо-контролирано проучване, тъй като пациентите с липсващи данни са били изключени от анализа на ефикасността. |
Фигура 4 показва процента на пациентите по категория на намаляване от изходното ниво на честота на припадък на капка на 28 дни през периода на лечение в проучване 3.
Фигура 4: Пропорция на пациентите по категория отговор на припадъци за fintepla и плацебо при пациенти със синдром на Lennox.gastaut (проучване 3)
| |
Числени по-големи подобрения на CGI-I от изследовател са наблюдавани при пациенти, лекувани с fintepla в сравнение с плацебо.
Информация за пациента за fintepla
FinteplaR ®
(Fin-tep-la)
(Фенфлурамин) Орален разтвор
Прочетете това ръководство за лекарства, преди да започнете да приемате fintepla и всеки път, когато получите зареждане. Може да има нова информация. Тази информация не заема мястото да разговаряте с вашия доставчик на здравни грижи за вашето медицинско състояние или лечение.
Коя е най -важната информация, която трябва да знам за Fintepla?
Fintepla can cause serious side effects including :
1. Проблеми с клапаните в сърцето (клапна сърдечна болест) и високо кръвно налягане в артериите на белите дробове (белодробна артериална хипертония) са били свързани с fintepla. Вашият доставчик на здравни грижи ще направи тест, наречен ехокардиограма, за да провери сърцето ви и за високо кръвно налягане в артериите на белите дробове, преди да започнете да приемате Fintepla отново на всеки 6 месеца по време на лечението и едно време 3 до 6 месеца, след като вземете последната си доза финепла.
Обадете се на вашия доставчик на здравни услуги веднага, ако развиете някой от тези признаци и симптоми на проблеми със сърцето или белите дробове по време на лечението с Fintepla:
- задух
- Болки в гърдите
- умора или слабост
- усещания за бързо трептящо сърцебиене
- Особено с повишена активност (сърцебиене)
- Лекоглавия or припадък
- нередовен пулс
- подути глезени или крака
- синкав цвят на устните и кожата ви (цианоза)
Поради риска от проблеми с сърдечните клапани (клапна сърдечна болест) и високо кръвно налягане в артериите на белите дробове (белодробна артериална хипертония) Fintepla е достъпна само чрез ограничена програма, наречена програма за оценка на риска и смекчаване на риска Fintepla (REMS). Преди вие или вашето дете да получите fintepla, вашият доставчик на здравни грижи или фармацевт ще се уверите, че ще разберете как да приемате Fintepla безопасно. Ако имате въпроси относно fintepla, попитайте вашия доставчик на здравни услуги, посетете www.finteplarems.com или се обадете на 1-877-964-3649.
2. Намален апетит и намалено тегло. Намален апетит и намалено тегло are both serious и common side effects of Fintepla in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Теглото ви трябва да се проверява редовно по време на лечението ви с Fintepla.
- Вашият доставчик на здравни услуги може да се наложи да направи промени в дозата на вашата финтепла, ако теглото ви намалява. В някои случаи може да се наложи да се спря.
3. Сънливост седация и липса на енергия (летаргия). Това са както сериозни, така и често срещани странични ефекти на Fintepla при хора със синдром на Dravet (DS) или синдром на Lennox-Gastaut (LGS). Приемането на fintepla с депресанти на централната нервна система (CNS), включително алкохол, може да увеличи сънливостта. Не управлявайте работа с тежки машини или не правете други опасни дейности, докато не разберете как Fintepla ви влияе.
4. Подобно на всички други антиепилептични лекарства fintepla може да причини самоубийствени мисли или действия в много малък брой хора (около 1 на 500).
Обадете се на вашия доставчик на здравни услуги веднага, ако имате някой от тези симптоми, особено ако те са нови по -лоши или се притеснявате:
- мисли за самоубийство или умиране
- Ново или по -лошо безпокойство
- Проблем със съня (безсъние)
- действайки върху опасни импулси
- Опити за самоубийство
- Чувствате се развълнувани или неспокойни
- Нова или по -лоша раздразнителност
- Изключително увеличаване на активността и говоренето (мания)
- нова или по -лоша депресия
- Панически атаки
- действащ агресивен, като е ядосан или насилствен
- Други необичайни промени в поведението или настроението
Как мога да гледам за ранни симптоми на самоубийствени мисли и действия?
- Обърнете внимание на всякакви промени, особено внезапни промени в мислите или чувствата на поведението на настроението.
- Запазете всички последващи посещения с вашия доставчик на здравни грижи по план.
Самоубийствените мисли или действия могат да бъдат причинени от неща, различни от лекарства. Ако имате самоубийствени мисли или действия, вашият доставчик на здравни услуги може да провери за други причини.
5. Не спирайте да приемате Fintepla, без първо да говорите с вашия доставчик на здравни услуги. Спирането на лекарство за припадъци като Fintepla внезапно може да ви накара да имате припадъци по -често или припадъци, които не спират (статус епилептик).
Обадете се на вашия доставчик на здравни услуги между посещенията, ако е необходимо, особено ако се притеснявате от симптомите.
Какво е fintepla?
- Fintepla is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) и Lennox- Gastaut syndrome (LGS) in patients 2 years of age и older.
- Не е известно дали Fintepla е безопасен и ефективен при деца на възраст под 2 години.
Не приемайте fintepla, ако вие:
- са алергични към фенфлурамин или някоя от съставките във fintepla. Вижте края на това ръководство за лекарства за пълен списък на съставките във Fintepla.
- приемат или са спрели да приемат лекарства, наречени инхибитори на моноамин оксидаза (MAOI) през последните 14 дни. Това може да доведе до сериозен или животозастрашаващ проблем, наречен синдром на серотонин. Ако не сте сигурни дали приемате или не от тези лекарства, свържете се с вашия доставчик на здравни услуги.
Преди да вземете fintepla, кажете на вашия доставчик на здравни грижи за всички ваши медицински състояния, включително ако вие:
- имат сърдечни проблеми
- са имали или са имали загуба на тегло
- са имали или са имали проблеми с настроението на депресия или самоубийствени мисли или поведение
- имат проблеми с бъбреците
- имат чернодробни проблеми
- са бременни или планират да забременеят. Кажете на вашия доставчик на здравни услуги веднага, ако забременеете, докато приемате fintepla. Вие и вашият доставчик на здравни грижи ще решите дали трябва да вземете Fintepla, докато сте бременна.
- Ако забременеете, докато приемате Fintepla, говорете с вашия доставчик на здравни грижи за регистрация в регистъра на бременността на антиепилептичните лекарства в Северна Америка. Можете да се запишете в този регистър, като се обадите на 1-888-233-2334 или отидете на www.
- aedpregnancyregistry.org. Целта на този регистър е да събира информация за безопасността на антиепилептичните лекарства по време на бременност.
- са кърмещи или планират да кърмят. Не е известно дали Fintepla преминава в кърмата ви. Говорете с вашия доставчик на здравни грижи за най -добрия начин да нахраните бебето си, докато приемате fintepla.
Кажете на вашия доставчик на здравни грижи за всички лекарства, които приемате включително лекарства за рецепта и лекарства без рецепта витамини и билкови добавки.
Познайте лекарствата, които приемате. Запазете списък с тях, за да покажете на вашия доставчик на здравни грижи или фармацевт, когато получите ново лекарство.
Как трябва да взема fintepla?
- Прочетете Инструкции за употреба В края на това ръководство за лекарства за информация по правилния начин за използване на fintepla.
- Вземете Fintepla точно както вашият доставчик на здравни грижи ви казва да го вземете.
- Вашият доставчик на здравни услуги ще ви каже колко fintepla да вземете и кога да го вземете.
- Fintepla may be taken with or without food.
- Измерете дозата си Fintepla, като използвате спринцовката за дозиране, която се предоставя от аптеката. Не използвайте домакинска чаена лъжичка или супена лъжица.
- Fintepla can be given through gastric и nasogastric feeding tubes
Какво трябва да избягвам, докато приемам fintepla?
- Не Drive работи с тежки машини или извършвайте други опасни дейности, докато не разберете как Fintepla ви влияе. Fintepla може да ви накара да се чувствате сънливи.
Какви са възможните странични ефекти на fintepla?
Fintepla may cause serious side effects including:
Обадете се на вашия доставчик на здравни услуги веднага, ако имате някой от следните симптоми на синдрома на серотонин.
- Вижте „Коя е най -важната информация, която трябва да знам за Fintepla?“
- Серотонин syndrome. Синдромът на серотонин е животозастрашаващ проблем, който може да се случи при хора, които приемат fintepla, особено ако fintepla се приема с някои други лекарства, за да включва:
- Антидепресантни лекарства, наречени SSRIS SNRIS TCAS и MAOI
- Сейнт Джонс
- триптофан
- Dextromethorphan
- Литий
- Трамадол
- Антипсихотици
- Промени в психичния статус, като виждат неща, които не са там (халюцинации) или кома
- Бързо сърцебиене
- Гадене повръща диария
- Промени в кръвното налягане
- Висока телесна температура
- стегнати мускули
- Проблем с ходенето
- Високо кръвно налягане (хипертония). Хипертонията е едновременно сериозен и често срещан страничен ефект. Fintepla може да доведе до повишаване на кръвното ви налягане, дори ако никога досега не сте имали високо кръвно налягане. Вашият доставчик на здравни услуги ще провери кръвното ви налягане, докато приемате fintepla.
- Повишено налягане в очите (глаукома). Симптомите на глаукома могат да включват:
- Червени очи
- Намалено зрение
- Виждане на ореоли или ярки цветове около светлините
- Болки в очите или дискомфорт
- гадене или повръщане
- замъглено зрение
Ако имате някой от тези симптоми, обадете се на вашия доставчик на здравни услуги веднага.
Най -често срещаните странични ефекти на fintepla, когато се използват за лечение на синдром на Дравет (DS), включват:
- Намален апетит
- диария
- ниска енергия
- сънливост
- Проблеми с баланса на движението и ходенето
- Повишено дрогиране
- дихателна инфекция
- повишено кръвно налягане
- намалено тегло
- повръщане
- треска
- пада
- запек
- Припадъци, които не спират
- Ненормална ехокардиограма
- слабост
Най-често срещаните странични ефекти на fintepla, когато се използват за лечение на синдром на Lennox-Gastaut (LGS), включват:
- диария
- умора
- повръщане
- сънливост
- Намален апетит
Това не са всички възможни странични ефекти на fintepla. За повече информация попитайте вашия доставчик на здравни грижи или фармацевт.
Кажете на вашия доставчик на здравни грижи, ако имате някакъв страничен ефект, който ви притеснява или който не отшумява.
Обадете се на Вашия лекар за медицински съвети относно страничните ефекти. Можете да отчитате странични ефекти на FDA на 1-800-FDA-1088.
Как трябва да съхранявам fintepla?
- Съхранявайте fintepla при стайна температура между 68 ° F до 77 ° F (20 ° C и 25 ° C).
- Не хладилник или замразяване.
- Съхранявайте бутилката Fintepla и спринцовка заедно в чиста зона.
- Изхвърлете (изхвърлете) всяка неизползвана fintepla 3 месеца след първото отваряне на бутилката или ако изхвърлянето след датата на пакета или бутилката е преминал. Който и да е на първо място.
Дръжте Fintepla и всички лекарства извън обсега на децата.
Обща информация за безопасното и ефективно използване на fintepla.
Лекарствата понякога се предписват за цели, различни от тези, изброени в ръководство за лекарства. Не използвайте fintepla за условие, за което не е предписано. Не давайте fintepla на други хора, дори ако те имат същите симптоми, които имате. Може да им навреди.
Можете да попитате вашия фармацевт или доставчик на здравни грижи за информация за Fintepla, която е написана за здравни специалисти.
Какви са съставките във Fintepla?
Активна съставка: Фенфлурамин хидрохлорид
Неактивни съставки: Шери аромат лимонена киселина Етилпарабен хидроксиетилцелулозен метилпарабен калиев цитрат сукралоза и вода.
Fintepla contains no ingredient made from gluten-containing grain (wheat barley or rye) и contains not more than 0.1% of въглехидрати което е от ароматизацията на черешите.
Това ръководство за лекарства е одобрено от американската администрация по храните и лекарствата.
Инструкции за употреба
Fintepla ®
(Fin-tep-la)
(Фенфлурамин) Орален разтвор 2.2 mg/mL
Уверете се, че четете разбиране и следвайте тези инструкции, преди да започнете да използвате Fintepla Oral Solution и всеки път, когато получите зареждане. Може да има нова информация.
Тези инструкции за употреба съдържат информация за това как да вземете fintepla. Тази информация не заема мястото да разговаряте с вашия доставчик на здравни грижи за вашето медицинско състояние или лечение.
Какво е включено с Fintepla?
Следните елементи са включени за подготовка и даване на устна доза Fintepla:
- 1 бутилка Fintepla перорален разтвор (NULL,2 mg/ml)
- 2 устни спринцовки за многократна употреба
| |
Обадете се на фармацевта на 1-844-288-5007, ако не сте получили изброените по-горе елементи или ако имате нужда от помощ, като ги използвате.
Важна информация за fintepla
- Fintepla is an oral medicine (taken by mouth) и is given 2 пъти всеки ден . Следвайте инструкциите на вашите доставчици на здравни услуги за приемане или даване на дози Fintepla.
- Ако имате въпроси как да се подготвите или да дадете на Fintepla да се свържете с вашия доставчик на здравни услуги или да се обадите на вашия фармацевт.
- Винаги използвайте устните спринцовки, осигурени с fintepla, за да сте сигурни, че е дадена правилната доза. Ако имате нужда от нова спринцовка, свържете се с вашия фармацевт. Не Използвайте домакинска чаена лъжичка или супена лъжица.
Орални спринцовки, снабдени с fintepla от аптеката.
С Fintepla ще получите 2 устни спринцовки за многократна употреба.
2 перорални спринцовки, които могат да измерват до 3 ml
Или
2 перорални спринцовки, които могат да измерват до 6 ml
| |
Обадете се на фармацевта на 1-844-288-5007, ако имате въпроси относно спринцовките, предоставени с fintepla.
Части от устната спринцовка
| |
Приготвяне на доза
Стъпка 1 . Уверете се, че имате:
- Бутилката с перорален разтвор на fintepla и
- Чиста суха орална спринцовка за многократна употреба, която беше снабдена с fintepla.
Стъпка 2. Проверете изхвърлянето след дата (mm/dd/yyyy).
| |
- Не Използвайте лекарството, ако изминава датата на хвърляне (изхвърляне).
- Ако датата е близо до вашата аптека или доставчик на здравни грижи, за да получите зареждане или ново предписание.
- Ако датата е преминала, разпоредете с неизползвана финтепла.
Стъпка 3. Натиснете надолу и обърнете защитната капачка вляво (обратно на часовниковата стрелка) и я отстранете от бутилката.
- Оставете капачката настрана (не изхвърляйте).
| |
Стъпка 4. Уверете се, че адаптерът е на бутилката.
- Ако бутилката няма адаптер, свържете се с фармацевта.
- Винаги оставяйте адаптера на място В бутилката медицина.
| |
Стъпка 5. Извадете орална спринцовка от опаковката му, ако е необходимо.
Използвайте само устните спринцовки, осигурени с fintepla.
Ако оралната спринцовка е повредена или не можете да прочетете маркировките на дозата:
- Използвайте другата предоставена устна спринцовка или
- Свържете се с фармацевта, за да получите нов.
| |
Стъпка 6. Уверете се, че буталото е избутано докрай в устната спринцовка.
| |
Стъпка 7. Дръжте бутилката лекарство здраво върху твърда плоска повърхност.
Стъпка 8. Натиснете върха на устната спринцовка в отвора на адаптера, докато той не може да бъде избутан по -нататък.
| |
Стъпка 9. Дръжте устната спринцовка и бутилката заедно и обърнете с главата надолу.
| |
Стъпка 10. Бавно издърпайте буталото на устната спринцовка, за да изтеглите предписаната доза.
| |
| |
| |
Подготовка на доза (продължение)
Стъпка 11. Подредете края на буталото с маркировката за предписаната доза на оралната спринцовка.
Съвети за получаване на правилната доза
- Ако извадите твърде много лекарства:
- Оставете устната спринцовка в адаптера.
- Натиснете буталото бавно обратно в спринцовката, докато стигнете до предписаната доза.
- Ако видите въздушни мехурчета в лекарството:
- Оставете устната спринцовка в адаптера.
- Издърпайте буталото по -надолу.
- Оставете мехурчетата да се издигнат до върха на спринцовката.
- Натиснете буталото през целия път.
- Бавно издърпайте буталото на предписаната доза.
Забележка: Много малки мехурчета в течността са нормални.
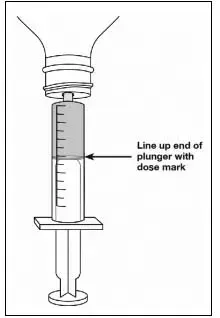
Стъпка 12. Дръжте устната спринцовка и бутилката заедно и след това обърнете бутилката от дясната страна нагоре.
| |
Стъпка 13. Държейки бутилката здраво внимателно издърпайте устната спринцовка от адаптера на бутилката.
| |
Стъпка 14. Уверете се, че дозата в оралната спринцовка все още съвпада с предписаната доза.
Ако дозата не съвпада:
- Поставете спринцовката обратно в адаптер.
- Вижте стъпки от 9 до 11, за да регулирате дозата според нуждите.
Даване на fintepla
Стъпка 15. Поставете върха на устната спринцовка срещу вътрешността на бузата.
Стъпка 16. Нежно натиснете буталото, докато не се даде цялото лекарство в устната спринцовка.
| |
- Не Скурайте или насилствено натиснете лекарството в гърба на гърлото. Това може да причини задушаване.
Стъпка 17. Поставете капачката обратно върху бутилката, като обърнете капачката надясно (по посока на часовниковата стрелка), докато спре.
- Винаги оставяйте адаптера на място in the bottle
- Капачката ще се побере над нея.
| |
Почистване на спринцовката
- Изплакнете устната спринцовка с чиста вода от чешмата и я оставете да изсъхне на въздух след всяка употреба.
- Уверете се, че изплакнете вътрешността на спринцовката и буталото.
Съвети за почистване:
- Издърпайте чистата чешмяна вода в спринцовката с буталото и го изтласкайте няколко пъти, за да почистите спринцовката.
- Извадете буталото от цевта на устната спринцовка
- Изплакнете и двете части под чешмяна вода
- Уверете се, че спринцовката и буталото са напълно сухи преди следващата употреба.
- Спринцовката също е безопасна за почистване в съдомиялната машина.
| |
Как трябва да съхранявам fintepla?
- Съхранявайте fintepla при стайна температура между 68 ° F до 77 ° F (20 ° C до 25 ° C).
- Не хладилник или замразяване.
- Дръжте капачката плътно затворена и бутилката изправена.
- Съхранявайте бутилката Fintepla и спринцовка заедно в чиста зона.
- Изхвърлете (изхвърлете) всяка неизползвана fintepla 3 месеца след първото отваряне на бутилката или ако изхвърлянето след датата на пакета или бутилката е преминал. Който и да е на първо място.
- Дръжте Fintepla и всички лекарства извън обсега на децата.
Тези инструкции за употреба са одобрени от американската администрация по храните и лекарствата.
