Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
Ерго производниИстина
Резюме на наркотиците
Какво е Trudhesa?
Trudhesa (дихидроерготамин мезилат) носният спрей е ерготаминово производно, използвано за лечение на мигрена със или без аура при възрастни.
Какви са страничните ефекти на Trudhesa?
Истина
- кошери
- затруднено дишане
- Подуване на лицето ви устни Език или гърло
- Бавен или бърз сърдечен ритъм
- слабост в краката
- мускулна болка в ръцете или краката
- изтръпване или изтръпване
- Студ в ръцете и краката
- сини пръсти и пръсти
- силна стомашна болка
- челюст или болка в лявата ръка
- Болки в гърдите или налягане
- внезапна умора
- слабост от едната страна на тялото
- Проблем в говоренето
- Визията се променя
- Психични или промени в настроението
- объркване
- обрив
- сърбеж и
- Тежка замаяност
Получете медицинска помощ веднага, ако имате изброени по -горе симптоми.
Страничните ефекти на Trudhesa включват:
- течен нос
- гадене
- променен смисъл с вкус
- Реакции на сайта на приложението
- замаяност
- повръщане
- сънливост
- възпалено гърло и
- диария.
Потърсете медицинска помощ или се обадете на 911 наведнъж, ако имате следните сериозни странични ефекти:
- Сериозни симптоми на очите, като например внезапна загуба на зрение, замъглено зрение Тунел Виждане болка в очите или подуване или виждане на ореоли около светлините;
- Сериозни сърдечни симптоми като бързи нередовни или ударни сърдечни удари; трептене в гърдите ви; задух; и внезапно замаяност Лекоглавия или раздаване;
- Тежка главоболие объркване затънала речева ръка или крак слабост проблем за ходене на загуба на координация, чувствайки се нестабилни много твърди мускули висока треска обилно изпотяване или тремор.
Този документ не съдържа всички възможни странични ефекти, а други могат да възникнат. Консултирайте се с вашия лекар за допълнителна информация за страничните ефекти.
Дозировка за Trudhesa
Препоръчителната доза назален спрей на Trudhesa е 1,45 mg (прилагана като един дозиран спрей от 0,725 mg във всяка ноздра). Дозата може да се повтори, ако е необходимо минимум 1 час след първата доза.
Trudhesa при деца
Безопасността и ефективността на носния спрей на Trudhesa е при педиатрични пациенти не са установени.
Какви лекарства вещества или добавки взаимодействат с Trudhesa?
Назален спрей на Trudhesa може да взаимодейства с други лекарства като:
- Бета-блокери
- Никотин
- селективен инхибитор на обратното захващане на серотонин ( Ако ) антидепресанти (например флуоксетин флувоксамин пароксетин сертралин)
- протеазни инхибитори (напр. Ритонавир нелфинавир Индинавир)
- макролид Антибиотици (напр. Еритромицин кларитромицин)
- Противогъбични (напр. Кетоконазол итраконазол)
- триптани и
- Вазоконстриктори.
Кажете на Вашия лекар всички лекарства и добавки, които използвате.
Trudhesa по време на бременност и кърмене
Кажете на Вашия лекар, ако сте бременна или планирате да забременеете, преди да използвате спрей за нос на Trudhesa. Това може да увеличи риска от преждевременно доставка и може да навреди на плода. Не е известно дали спрей за нос на Trudhesa преминава в кърма; Въпреки това ерготамин, свързано с лекарството, присъства в кърмата. Поради потенциала за намалено снабдяване с мляко и сериозни нежелани събития при кърменето, включително диария, повръщайки слаб пулс и нестабилно кърмене на кръвно налягане, не се препоръчва по време на лечение с назален спрей на Trudhesa и в продължение на 3 дни след последната доза. Доставката на кърма през това време трябва да се изпомпва и изхвърли.
Допълнителна информация
Нашият Trudhesa (дихидроерготамин мезилат) Назален спрей страничен център лекарства предоставя изчерпателен поглед върху наличната информация за лекарството върху потенциалните странични ефекти при приемането на това лекарство.
Това не е пълен списък на страничните ефекти и други могат да възникнат. Обадете се на Вашия лекар за медицински съвети относно страничните ефекти. Можете да отчитате странични ефекти на FDA на 1-800-FDA-1088.
Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Странични ефекти
- Лекарствени взаимодействия
- Предупреждения
- Предозиране
- Противопоказания
- Клинична фармакология
- Ръководство за лекарства
Предупреждение
Периферна исхемия след съвместно приложение със силни CYP3A4 инхибитори
Сериозна и/или животозастрашаваща периферна исхемия е свързана със съвместното приложение на дихидроерготамин със силни CYP3A4 инхибитори. Тъй като инхибирането на CYP3A4 повишава серумните нива на дихидроерготамин, рискът от вазоспазъм, водещ до мозъчна исхемия и/или исхемия на крайниците, се увеличава. Следователно съпътстващата употреба на Trudhesa със силни CYP3A4 инхибитори е противопоказана [виж Противопоказания ПредупреждениеS AND PRECAUTIONS и Лекарствени взаимодействия ].
Описание за Trudhesa
Trudhesa (дихидроерготамин мезилат) носният спрей е комбиниран продукт за лекарства с еднократна доза, съдържащ дихидроерготамин мезилатен състав на лекарството и съставка на устройството за спрей на носа.
Химическото наименование за дихидроерготамин мезилат е Ergotaman-3 '6' 18-Trione 910-дихидро- 12'-хидрокси-2'-метил-5'- (фенилметил)-(5'a)-монометансулфонат. Молекулното му тегло е 679,78, а молекулната му формула е c 33 H 37 N 5 O 5 • гл 4 O 3 С. С.
Химическата структура е:
 |
Съставката на лекарството е дихидроерготамин мезилатен разтвор. Всеки милилитър (ml) разтвор съдържа дихидроерготамин мезилат 4,0 mg (еквивалентен на 3,43 mg дихидроерготамин) и следните неактивни съставки: кофеин (NULL,0 mg) въглероден диоксид (q.s.) декстроза (50.0 mg) и вода (Q.S.
Назален спрей на Trudhesa след сглобяване и грундиране осигурява 0,725 mg дихидроерготамин мезилат на спрей. Обща доза от 1,45 mg дихидроерготамин мезилат се доставя в 2 спрея. Устройството за спрей на носа съдържа гориво хидрофлуороалкан-134А (HFA).
Използване за Trudhesa
Trudhesa е показан за остра третиране на мигрена със или без аура при възрастни.
Ограничения на употребата
Trudhesa не е посочен за превантивно третиране на мигрена.
Trudhesa не е посочен за управление на хемиплегична или базиларна мигрена.
Дозировка за Trudhesa
Дозиране на информация
Препоръчителната доза Trudhesa е 1,45 mg, прилагана като две измервани спрея в носа (един спрей от 0,725 mg във всяка ноздра).
Дозата може да се повтори, ако е необходимо минимум 1 час след първата доза. Не използвайте повече от 2 дози Trudhesa в рамките на 24-часов период или 3 дози в рамките на 7-дневен период.
Оценка преди първата доза
Преди започване на Trudhesa се препоръчва сърдечно -съдова оценка [виж ПредупреждениеS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Важни инструкции за администрация
Trudhesa е само за прилагане на носа и не трябва да се инжектира.
Trudhesa трябва да бъде сглобен преди употреба (виж Инструкции за употреба ). Използване или изхвърляне на Trudhesa в рамките на 8 часа, след като флаконът е отворен или продуктът е сглобен.
Направете сглобената Trudhesa преди първоначалната употреба, като пуснете 4 спрея. Използвайте Trudhesa веднага след грундиране. Изхвърлете Trudhesa веднага след употреба. Отворете и пригответе нов Trudhesa, ако е необходима допълнителна доза.
Колко се доставя
Дозирани форми и силни страни
Trudhesa (дихидроерготамин мезилат) носният спрей е комбиниран продукт за лекарства с една доза, съдържащ флакон с дихидроерготамин мезилат с ясен и безцветно до слабо жълто разтвор и интраназално устройство за доставяне. Всеки спрей осигурява 0,725 mg дихидроерготамин мезилат.
Trudhesa (дихидроерготамин мезилат) носен спрей (NULL,725 mg на спрей) се доставя като пакет от 4 единични единици с една доза ( NDC 77530-725-04). Всяка единица с една доза съдържа:
- Едно кехлибарено стъкло флакон ( NDC 77530-725-01), съдържащ 4 mg дихидроерготамин мезилат в 1 ml бист и безцветна до слабо жълт разтвор. Запушалката не е направена с естествен каучуков латекс.
- Едно устройство за спрей на носа.
Съхранение и обработка
Съхранявайте Trudhesa при контролирана стайна температура 20 ° C до 25 ° C (68 ° F до 77 ° F) с екскурзии, разрешени между 15 ° C до 30 ° C (59 ° F до 86 ° F). Не се охлаждайте и не замразявайте.
Произведено от: Mipharm S.P.A. Милано Италия. Ревизиран: септември 2021 г.
Странични ефекти for Trudhesa
Следните клинично значими нежелани реакции са описани другаде в етикетирането:
- Периферна исхемия след съвместно приложение със силни CYP3A4 инхибитори [виж Предупреждение за кутия и ПредупреждениеS AND PRECAUTIONS ]
- Миокардна исхемия и/или инфаркт Други неблагоприятни сърдечни събития и жертви [виж ПредупреждениеS AND PRECAUTIONS ]
- Цереброваскуларни нежелани реакции и жертви [виж ПредупреждениеS AND PRECAUTIONS ]
- Други нежелани реакции, свързани с вазоспазма [виж ПредупреждениеS AND PRECAUTIONS ]
- Повишаване на кръвното налягане [виж ПредупреждениеS AND PRECAUTIONS ]
- Лекарства за свръх използване на главоболие [виж ПредупреждениеS AND PRECAUTIONS ]
- Преждевременно труд [виж ПредупреждениеS AND PRECAUTIONS ]
- Фиброзни усложнения [виж ПредупреждениеS AND PRECAUTIONS ]
- Местно дразнене [виж ПредупреждениеS AND PRECAUTIONS ]
Опит с клинични изпитвания
Тъй като клиничните изпитвания се провеждат при широко различни състояния, нежелани реакционни проценти, наблюдавани при клиничните изпитвания на лекарство, не могат да бъдат пряко сравнени със проценти в клиничните изпитвания на друго лекарство и може да не отразяват процентите, наблюдавани на практика.
Нежелани реакции в плацебо-контролирани изпитвания с дихидроерготамин (DHE) мезилатен спрей на носа [виж Клинични изследвания ]
От 1796 пациенти и лица, лекувани с DHE носни спрей дози 2 mg или по -малко в САЩ и чуждестранни клинични проучвания 26 (NULL,4%), прекратени поради нежелани събития. Нежеланите събития, свързани с прекратяването, бяха в намаляващ ред на честотата: ринит (13) замаяност (2) оток на лицето (2) и един пациент, всеки поради студена изпотяване случайна травма депресия Елективна хирургия Сомнина алергия Хипотония и параестезия.
Странични ефекти на Tretinoin Cream 0,05
Таблица 1 обобщава честотата на честотата на нежеланите реакции, отчетени от най-малко 1% от пациентите, които са получили спрей за нос на DHE за лечение на мигрена по време на плацебо-контролирани клинични проучвания и са по-чести, отколкото при тези пациенти, получаващи плацебо. Най -често съобщаваните нежелани реакции (по -големи от 1% от пациентите, които са получили DHE носен спрей) са ринит гадене, променено усещане за реакции на приложението на приложението Реакции на замаяност повръща сомолетен фарингит и диария. В повечето случаи тези събития бяха преходни и самостоятелни и не доведоха до прекратяване на пациента от проучване.
Таблица 1 Нежелани реакции, отчетени от най-малко 1% от пациентите с лекуван спрей, лекуван с нос на DHE, и се срещат по-често, отколкото в плацебогрупата в мигренозните плацебо-контролирани изпитвания
| И носен спрей N = 597 % | Плацебо N = 631 % | |
| Дихателна система | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Стомашно -чревна система | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Специални сетива други | ||
| Altered Sense of Taste | 8 | 1 |
| Сайт за кандидатстване | ||
| Сайт за кандидатстване Reaction | 6 | 2 |
| Централна и периферна нервна система | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Тяло като цяло генерал | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Мускулно -скелетна система | ||
| Stiffness | 1 | <1 |
Нежелани реакции в проучвания с Trudhesa
Проведено е открито проучване при възрастни (на възраст от 18 до 66 години), за да се оцени безопасността и поносимостта на Trudhesa повторно използване на Trudhesa в продължение на 6 до 12 месеца. Общо 354 пациенти с мигрена са получили поне една доза Trudhesa. Сто и осемдесет и пет пациенти, лекувани средно поне две мигрена на месец в продължение на 6 месеца, а 55 пациенти са лекували средно поне две мигрена на месец в продължение на 12 месеца. От пациентите, които са получавали поне една доза Trudhesa 185 (NULL,3%) пациенти, изпитват локални напоени симптоми. От тях най -често срещаните локални напоени симптоми са назофарингит ринит назален дискомфорт продукт Вкус на вкуса/дисгеузия синузит синус дискомфорт обонятелен тест Ненормален епистаксис фарингит назален лигавичен разстройство в миризма на ухото дискомфорт и ринорея [виж ПредупреждениеS AND PRECAUTIONS ].
Опит за постмаркетиране
Следните нежелани реакции са идентифицирани по време на след прилагане употреба на дихидроерготамин мезилат. Тъй като тези реакции се отчитат доброволно от популация с несигурен размер, не винаги е възможно надеждно да се оцени тяхната честота или да се установи причинно -следствена връзка с експозицията на лекарства:
Вазоспазъм Парестезия Хипертония замаяност Тревожност Диспнея главоболие Промиване на диария обрив повишава изпотяването и плевралната и ретроперитонеалната фиброза след дългосрочна употреба на дихидроерготамин. Съобщава се за случаи на миокарден инфаркт и инсулт след използването на дихидроерготамин мезилат [виж ПредупреждениеS AND PRECAUTIONS ].
Лекарствени взаимодействия for Trudhesa
CYP3A4 инхибитори
There have been rare reports of serious adverse events in connection with the coadministration of intravenous administration of dihydroergotamine and strong CYP3A4 inhibitors such as protease inhibitors (e.g. ritonavir nelfinavir indinavir) macrolide antibiotics (e.g. erythromycin clarithromycin) and antifungals (e.g. ketoconazole итраконазол), което води до вазоспазъм, довел до церебрална исхемия и/или исхемия на крайниците [виж ПредупреждениеS AND PRECAUTIONS ]. The use of strong CYP3A4 with dihydroergotamine is contraindicated [see Противопоказания ]. Administer moderate CYP3A4 (e.g. saquinavir Нефазодон Флуконазол grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Триптани
Триптани (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm и its effect could be additive with TRUDHESA. Therefore триптани и TRUDHESA should not be taken within 24 часа of each other [see Противопоказания ].
Бета блокери
Има съобщения, че пропранолол може да потенцира вазоконстриктивното действие на ерготамин, като блокира вазодилиращото свойство на епинефрин.
Вазоконстриктори
Trudhesa е противопоказано за употреба с периферни и централни вазоконстриктори, тъй като комбинацията може да причини синергично повишаване на кръвното налягане [виж ПредупреждениеS AND PRECAUTIONS ].
Никотин
Никотин may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see ПредупреждениеS AND PRECAUTIONS ].
Селективни инхибитори на обратното захващане на серотонин
Съобщава се рядко хиперрефлексия и некоординация на слабостта, когато 5-НТ 1 Агонистите са били съвместни със селективни инхибитори на обратното захващане на серотонин (например флуоксетин флувоксамин пароксетин сертралин).
Злоупотреба с наркотици и зависимост
Контролирано вещество
Trudhesa съдържа дихидроерготамин (като мезилатна сол), който не е контролирано вещество.
Злоупотреба
Злоупотреба is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Зависимост
Физическата зависимост е състояние, което се развива в резултат на физиологична адаптация в отговор на многократна употреба на лекарства, проявена чрез признаци на оттегляне и симптоми след рязко прекратяване или значително намаляване на дозата на лекарството. Понастоящем наличните данни не са демонстрирали физическа или психологическа зависимост с дихидроерготамин. Въпреки това са съобщени случаи на психологическа зависимост при пациенти от други форми на ерго терапия.
Предупреждения за Trudhesa
Включени като част от 'ПРЕДПАЗНИ МЕРКИ' Раздел
Предпазни мерки за Trudhesa
Периферна исхемия след съвместно приложение със силни CYP3A4 инхибитори
Сериозна и/или животозастрашаваща периферна исхемия е свързана със съвместното приложение на дихидроерготамин със силни CYP3A4 инхибитори, включително протеазни инхибитори макролидни антибиотици и противогъбични. Тъй като инхибирането на CYP3A4 повишава серумните нива на дихидроерготамин, рискът от вазоспазъм, водещ до мозъчна исхемия и/или исхемия на крайниците, се увеличава. Следователно съпътстващата употреба на Trudhesa със силни CYP3A4 инхибитори е противопоказана [виж Противопоказания и Лекарствени взаимодействия ].
Миокардна исхемия и/или инфаркт Други сърдечни нежелани реакции и жертви
Потенциалът за нежелани сърдечни нежелани реакции съществува при лечение на Trudhesa. Сериозни неблагоприятни сърдечни събития, включително някои, които са били фатални, са настъпили след използването на дихидроерготамин мезилат. Тези събития включват остра миокардна инфарктна нарушение на нарушенията на сърдечния ритъм (напр. Вентрикуларна тахикардия и камерна фибрилация) вазоспазъм на коронарната артерия и преходна миокардна исхемия.
Преди започване на Trudhesa се препоръчва сърдечно -съдова оценка, за да се определи дали пациентът е без коронарна артерия и исхемична миокардна болест или други значими основни сърдечно -съдови заболявания. Ако по време на сърдечно -съдовата оценка медицинската история на пациента (включително рискови фактори) или находки на електрокардиографско изследване са в съответствие с вазоспазма на коронарната артерия или миокардната исхемия Trudhesa [виж Противопоказания ].
For patients with risk factors predictive of coronary artery disease (e.g. hypertension hypercholesterolemia smoker obesity diabetes strong family history of coronary artery disease females who are surgically or physiologically postmenopausal or males who are over 40 years of age) who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place В обстановката на оборудвано здравно заведение, освен ако пациентът преди това не е получил дихидроерготамин мезилат. По време на интервала непосредствено след първата употреба на Trudhesa се препоръчва електрокардиограма при тези пациенти с рискови фактори, тъй като исхемията може да възникне при липса на клинични симптоми.
Цереброваскуларни нежелани реакции и жертви
Потенциалът за неблагоприятни мозъчно -съдови нежелани реакции съществува при лечение на Trudhesa. Съобщават се, че при пациенти са съобщени, че при пациенти, лекувани с дихидроерготамин мезилат; а някои са довели до жертви. В редица случаи изглежда възможно, че мозъчните събития са били първични, дихидроерготамин мезилатът е бил прилаган с неправилно убеждение, че преживяните симптоми са следствие от мигрена, когато не са били. Трябва да се отбележи, че пациентите с мигрена могат да бъдат изложени на повишен риск от определени мозъчно -съдови събития (например преходна исхемична атака на инсулт). Преустановете Трудеса, ако се подозира мозъчно -съдово събитие.
Други нежелани реакции, свързани с вазоспазъм
Trudhesa като други алкалоиди от ерго може да причини вазоспастични реакции, различни от вазоспазма на коронарната артерия. Съобщава се за миокардна периферна съдова и дебелина на исхемията с дихидроерготамин мезилат.
Дихидроерготамин мезилат, свързани с вазоспастични явления, също могат да причинят мускулни болки изтръпване на студната бледност и цианоза на цифрите. При пациенти с компрометирана циркулация персистиращият вазоспазъм може да доведе до гангрена или смърт. Trudhesa трябва да бъде прекратен незабавно, ако се развият признаци или симптоми на вазоконстрикция.
Пациентите, които изпитват други симптоми или признаци, подсказващи за намален артериален поток, като синдром на исхемичен синдром на червата или синдром на Рейно след използването на всеки 5-НТ агонист, включително Trudhesa, трябва да бъдат оценени от доставчик на здравни грижи.
Увеличаване на кръвното налягане
Съобщава се за значително повишаване на кръвното налягане при редки случаи при пациенти със и без анамнеза за хипертония, лекувана с дихидроерготамин мезилат. Trudhesa е противопоказано при пациенти с неконтролирана хипертония [виж Противопоказания ].
Увеличаването на средното налягане на белодробната артерия с 18% се наблюдава след дозиране с още 5- HT 1 Агонист в проучване, оценяващо субектите, подложени на сърдечна катетеризация.
Лекарства за прекомерно използване на главоболие
Прекомерната употреба на остри мигренозни лекарства (напр. Ерготамини триптани опиоиди или комбинация от тези лекарства в продължение на 10 или повече дни на месец) може да доведе до обостряне на главоболие (т.е. лекарства за прекомерно използване на главоболие). Лечебното прекомерно използване на главоболието може да се представи като ежедневно главоболие, подобни на мигрена или като значително увеличение на честотата на мигренозните атаки. Може да се наложи детоксикация на пациенти, включително оттегляне на прекалено използваните лекарства и лечение на симптоми на оттегляне (което често включва преходно влошаване на главоболието).
Преждевременно труд
Въз основа на механизма на действие на дихидроерготамин и открития от публикуваната литература Trudhesa може да причини преждевременно труд. Избягвайте използването на Trudhesa по време на бременност [виж Използване в конкретни популации ]
Фиброзни усложнения
Потенциалът за фиброзни усложнения съществува при лечение на Trudhesa. Има съобщения за плеврална и ретроперитонеална фиброза при пациенти след продължителна ежедневна употреба на дихидроерготамин мезилат. Рядко удължената ежедневна употреба на други алкалоидни лекарства ерго е свързана със сърдечна клапаварна фиброза. Съобщава се и за редки случаи във връзка с използването на дихидроерготамин мезилат; Въпреки това в тези случаи пациентите също са получавали лекарства, за които се знае, че са свързани със сърдечна клапна фиброза.
Прилагането на Trudhesa не трябва да надвишава насоките за дозиране и не трябва да се използва за хронично ежедневно приложение [виж Доза и приложение ].
Местно дразнене
Съобщават се, че локалните напоени симптоми при 52% от пациентите, лекувани с поне една доза Trudhesa в отворено белязано проучване, което позволява многократна употреба на Trudhesa за 6 до 12 месеца. The most common local irritative symptoms (at least 1% of patients) were nasopharyngitis (21%) rhinitis (19%) nasal discomfort (7%) product taste abnormal/dysgeusia (6%) sinusitis (5%) sinus discomfort (4%) olfactory test abnormal [defined based on a change in score at a prespecified threshold on the University of Pennsylvania Smell Identification Тест (UPSIT)] (4%) Епистаксис (3%) Фарингит (3%) Назална лигавична разстройство (2%) Промяна в миризмата (1%) Дискомфорт на ухото (1%) и ринорея (1%). Ако възникне тежко местно събитие за раздразнение по никакви други приписващи причини, които Trudhesa трябва да бъде временно спрян, докато събитието не се разреши. Ако събитието не се разреши или то се повтаря с повторно предизвикателство Trudhesa, трябва да бъде прекратено за постоянно. Прилагането на Trudhesa не трябва да надвишава насоките за дозиране и не трябва да се използва за хронично ежедневно приложение [виж Доза и приложение ].
Назалната тъкан при животни, лекувани с дихидроерготамин мезилат дневно, показва леко дразнене на лигавицата, характеризиращо се с лигавична клетъчна и преходна клетъчна хиперплазия и плоскоклетъчна метаплазия. Промените в носната лигавица на плъхове на 64 седмици бяха по -малко тежки, отколкото при 13 седмици. Местните ефекти върху дихателната тъкан след хронична интраназална доза при животни не са оценени.
Информация за консултирането на пациентите
Посъветвайте се на пациента да прочете одобреното от FDA етикетиране на пациента ( Ръководство за лекарства и Инструкции за употреба ).
Какво се използва Норвас за лечение
Сериозни и/или животозастрашаващи реакции с съвместно приложение на CYP3A4 инхибитори
Inform patients that serious and/or life-threatening peripheral ischemia (cerebral ischemia and/or ischemia of the extremities) has been associated with the coadministration of dihydroergotamine mesylate and strong CYP3A4 inhibitors such as macrolide antibiotics and protease inhibitors [see Противопоказания ПредупреждениеS AND PRECAUTIONS и Лекарствени взаимодействия ].
Миокардна исхемия и/или инфаркт Други сърдечни събития мозъчно -съдови събития и жертви
Информирайте пациентите за риска от сериозни сърдечни мозъчно -съдови и други събития, свързани с вазоспазъм. Посъветвайте пациентите да уведомят своя доставчик на здравни грижи, ако развият рискови фактори или симптоми, докато приемат Trudhesa. Информирайте пациентите, че никотинът може да провокира вазоконстрикция, предразполагаща към по -голям исхемичен отговор [виж ПредупреждениеS AND PRECAUTIONS ].
Лекарства за прекомерно използване на главоболие
Информирайте пациентите, че употребата на лекарства за лечение на мигренови атаки в продължение на 10 или повече дни на месец може да доведе до обостряне на главоболие и да насърчи пациентите да запишат честота на главоболие и употреба на лекарства (например чрез водене на дневник за главоболие) [виж ПредупреждениеS AND PRECAUTIONS ].
Местно дразнене
Посъветвайте пациентите да уведомят своя доставчик на здравни грижи, ако имат притеснително местно раздразнение [виж ПредупреждениеS AND PRECAUTIONS ].
Лекарствени взаимодействия
Посъветвайте пациентите да информират своите доставчици на здравни грижи, ако приемат или планират да приемат някакви лекарства без рецепта или без рецепта, тъй като има потенциал за взаимодействия [виж Лекарствени взаимодействия ].
Бременност
Консултирайте пациентите за риска от преждевременно раждане. Съветват жените да информират своя доставчик на здравни грижи, ако са бременни или възнамеряват да забременеят [виж ПредупреждениеS AND PRECAUTIONS Използване в конкретни популации ]
Лактация
Посъветвайте пациентите да не кърмят по време на лечението с Trudhesa [виж Използване в конкретни популации ].
Важни инструкции за администрация
Посъветвайте се пациентите, че Trudhesa трябва да бъде сглобена преди употреба и преди прилагането устройството трябва да бъде грундирано (т.е. изпомпвано 4 пъти). Инструктирайте пациентите да използват или изхвърлят Trudhesa в рамките на 8 часа, след като флаконът е отворен или продуктът е сглобен.
Неклинична токсикология
Канцерогенеза мутагенеза Нарушаване на плодовитостта
Карциногенеза
Оценка на канцерогенния потенциал на дихидроерготамин мезилат при мишки и плъхове не е оценена.
Мутагенеза
Дихидроерготамин мезилатът е отрицателен в in vitro тест за мутагенност (AMES) и положителен в in vitro Хромозомна аберация (V79 китайска клетка за хамстер с метаболитна активация и лимфоцит на периферна кръв на човека). Дихидроерготаминът е отрицателен в напразно Микронуклеус Анализи при мишка и хамстер.
Увреждане на плодовитостта
Няма данни за увреждане на плодовитостта при плъхове, дадени интраназални дози дихидроерготамин мезилат до 1,6 mg/ден, което е свързано с плазмени експозиции (AUC) приблизително 3 пъти, че при хора при максимална препоръчителна доза от 2,9 mg/ден.
Използване в конкретни популации
Бременност
Обобщение на риска
Наличните данни от публикуваната литература показват повишен риск от преждевременно раждане с употреба на Trudhesa по време на бременност. Избягвайте използването на Trudhesa по време на бременност [виж ПредупреждениеS AND PRECAUTIONS ]. Данни collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
In animal studies adverse effects on embryofetal development were observed following administration of dihydroergotamine mesylate during pregnancy (decreased fetal body weight and/or skeletal ossification) in rats and rabbits or during pregnancy and lactation in rats (decreased body weight and impaired reproductive function in the offspring) in rats at doses less than those used clinically and which were not associated with maternal toxicity (see Данни ).
Прогнозната честота на основните вродени дефекти (NULL,2%до 2,9%) и спонтанен аборт (17%) сред доставките на жени с мигрена са подобни на процентите, отчетени при жени без мигрена. Всички бременности имат основен риск от загуба на вроден дефект или други неблагоприятни резултати. В общата популация на САЩ прогнозният фонов риск от големи вродени дефекти и спонтанни аборти при клинично признати бременности е съответно 2% до 4% и 15% до 20%.
Данни
Данни за животните
Интраназалното приложение на дихидроерготамин мезилат на бременни плъхове през целия период на органогенеза води до намалено телесно тегло на плода и/или скелетна осификация при дози 0,16 mg/ден (свързани с плазмените експозиции [AUC] по -малко от хората при максимума, препоръчана човешка доза [MRHD] от 2.9 mg) или по -големи. Ниво на ембриофетална токсичност не е идентифицирано при плъхове. Интраназалното приложение на дихидроерготамин мезилат към бременни зайци по време на органогенезата доведе до намаляване на скелетната осификация при 3,6 mg/ден. При дозата без ефект (NULL,2 mg/ден) за неблагоприятни ефекти върху развитието на ембриофеталното развитие при плазмени експозиции на зайци (AUC) са по-малки от тези при хората при МРХ.
Интраназалното приложение на дихидроерготамин мезилат към женски плъхове по време на бременност и лактация води до намаляване на телесното тегло и нарушена репродуктивна функция (намалени индекси на чифтосване) се наблюдават при потомството при дози 0,16 mg/ден или по -голямо. Не е установена доза без ефект за неблагоприятни ефекти на развитие при плъхове.
Ефектите върху развитието са възникнали при дози под тези, които дават доказателства за значителна майчинска токсичност в тези проучвания.
Индуцираният с дихидроерготамин забавяне на вътрематочния растеж се приписва на намален матоплацентален кръвен поток в резултат на продължителна вазоконстрикция на маточните съдове и/или увеличен миометриален тонус.
Лактация
Обобщение на риска
Няма данни за наличието на дихидроерготамин в човешкото мляко; Въпреки това ерготамин, свързано с лекарството, присъства в човешкото мляко. Съществуват съобщения за диария, повръщайки слаб пулс и нестабилно кръвно налягане при кърмани бебета, изложени на ерготамин. Trudhesa може да намали снабдяването с мляко, тъй като може да намали нивата на пролактин. Поради потенциала за намалено снабдяване с мляко и сериозни нежелани събития при кърмалото бебе, включително диария, повръщайки слаб пулс и нестабилно кръвно налягане, съветват пациентите да не кърмят по време на лечението с Трудехе и в продължение на 3 дни след последната доза. Доставката на кърма през това време трябва да се изпомпва и изхвърли.
Педиатрична употреба
Безопасността и ефективността при педиатрични пациенти не са установени.
Гериатрична употреба
Клиничните проучвания на Trudhesa и други дихидроерготамин мезилатни продукти не включват достатъчен брой лица на възраст 65 и повече години, за да се определи дали реагират по различен начин от по -младите лица. Като цяло изборът на доза за възрастен пациент трябва да бъде предпазлив обикновено, като се започне от ниския край на обхвата на дозиране, отразяващ по -голямата честота на намалена чернодробна бъбречна или сърдечна функция и на съпътстваща болест или друга лекарствена терапия.
Предозиране Information for Trudhesa
Симптоми
Прекомерните дози дихидроерготамин могат да доведат до периферни признаци и симптоми на ерготизъм. Като цяло симптомите на предозиране с остра Trudhesa са подобни на тези на предозиране на ерготамин, въпреки че може да има по -слабо изразено гадене и повръщане с Trudhesa. Симптомите на предозиране на ерготамин включват следното: изтръпване на болката в изтръпване и цианоза на крайниците, свързани с намалени или отсъстващи периферни импулси; дихателна депресия; увеличение и/или намаляване на кръвното налягане обикновено в този ред; объркване делириум конвулсии и кома; и/или някаква степен на гадене повръщане и коремна болка.
При лабораторни животни дихидроерготаминът е смъртоносен, когато се прилага при интравенозни дози от 44 mg/kg при мишки 130 mg/kg при плъхове и 37 mg/kg при зайци.
Лечение
Лечение includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators и nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Противопоказания for Trudhesa
Trudhesa е противопоказано при пациенти:
как да пътувате с ограничен бюджет
- Със съпътстваща употреба на силни CYP3A4 инхибитори като протеазни инхибитори (напр. Ритонавир нелфинавир или Индинавир) макролидни антибиотици (например еритромицин или кларитромицин) и антифунгали (кетоконазол или итраконазол) [виж. ПредупреждениеS AND PRECAUTIONS и Лекарствени взаимодействия ]
- С исхемична сърдечна болест (ангина пекторис анамнеза за инфаркт на миокарда или документирана безшумна исхемия) или пациенти, които имат клинични симптоми или находки, съответстващи на вазоспазма на коронарната артерия, включително вариантния ангина на принтала [виж ПредупреждениеS AND PRECAUTIONS ]
- с неконтролирана хипертония [виж ПредупреждениеS AND PRECAUTIONS ]
- с периферна артериална болест
- със сепсис
- след съдова хирургия
- с тежко чернодробно увреждане
- с тежко бъбречно увреждане
- с известна свръхчувствителност към ерго алкалоиди
- С скорошна употреба (т.е. в рамките на 24 часа) от други 5-HT 1 агонисти (напр. Суматриптан) или съдържащи ерготамин или лекарства от тип Ergot [виж Лекарствени взаимодействия ]
- С едновременна употреба на периферни и централни вазоконстриктори, тъй като комбинацията може да доведе до адитивно или синергично повишаване на кръвното налягане [виж ПредупреждениеS AND PRECAUTIONS ]
Клинична фармакология for Trudhesa
Механизъм на действие
Дихидроерготамин се свързва с висок афинитет към 5-НТ 1da и 5-HT 1db рецептори. Терапевтичната активност на дихидроерготамин при мигрена обикновено се приписва на агонистките ефекти при 5-HT 1d рецептори.
Фармакодинамика
Съобщава се за значително повишаване на кръвното налягане при пациенти със и без анамнеза за хипертония [виж ПредупреждениеS AND PRECAUTIONS ].
Дихидроерготамин притежава окситокични свойства [виж ПредупреждениеS AND PRECAUTIONS ].
Фармакокинетика
Абсорбция
Средното време от дозиране до максимална плазмена концентрация след прилагане на Trudhesa е приблизително 0,5 часа.
Разпределение
Дихидроерготамин мезилатът е 93% обвързан с плазмен протеин. Очевидният стационарен обем на разпределение е приблизително 800 литра.
Елиминиране
Метаболизъм
Четири дихидроерготамин мезилатни метаболити са идентифицирани в човешката плазма след перорално приложение. Основният метаболит 8'-ß-хидрокси дихидроерготамин показва афинитет, еквивалентен на неговия родител за адренергични и 5-НТ рецептори и демонстрира еквивалентна потентност в няколко модела на активност на веноконстриктор напразно и in vitro . Другите метаболити, т.е. дихидролизергинова киселина Дихидролисергичен амид и метаболит, образуван от окислително отваряне на пролиновия пръстен, са от незначително значение. След администрацията на носа общите метаболити представляват само 20% до 30% от плазмения AUC. Системният клирънс на дихидроерготамин мезилат след интравенозно и интрамускулно приложение е 1,5 L/min. Количествената фармакокинетична характеристика на четирите метаболита не е извършена.
Екскреция
Основният екскретен път на дихидроерготамин е чрез жлъчката в изпражненията. Общият клирънс на тялото е 1,5 L/min, което отразява главно чернодробния клирънс. Само 6% до 7% от непроменен дихидроерготамин се отделя в урината след интрамускулна инжекция. Бъбречният клирънс (NULL,1 L/min) не се влияе от пътя на дихидроерготаминното приложение.
Средната очевидна полуживот на прилагането на носа на Trudhesa при здрави индивиди е приблизително 12 часа.
Специфични популации
Не са проведени проучвания върху ефекта на етническата принадлежност или бременността на бъбречно или чернодробно увреждане на фармакокинетиката на дихидроерготамин [виж Противопоказания Използване в конкретни популации ].
Проучвания за взаимодействие с лекарства
CYP3A4 инхибитори
Rare reports of ergotism have been obtained from patients treated with dihydroergotamine and macrolide antibiotics (e.g. clarithromycin erythromycin) and from patients treated with dihydroergotamine and protease inhibitors (e.g. ritonavir) presumably due to inhibition of CYP3A metabolism of ergotamine [see Противопоказания ].
Други лекарства
Фармакокинетиката на дихидроерготамин не изглежда значително повлияна от съпътстващата употреба на локален вазоконстриктор.
Множество перорални дози от β-адренорецепторен антагонист пропранолол, използван за мигренална профилактика, нямат значително влияние върху CMAX TMAX или AUC на дихидроерготамин дози до 4 mg. Въпреки това пропранолол може да потенцира вазоконстриктивното действие на ерготамин [виж Лекарствени взаимодействия ].
Ефектът на устните контрацептиви върху фармакокинетиката на Trudhesa не е проучен.
Клинични изследвания
Ефикасността на Trudhesa се основава на относителната бионаличност на носния спрей на Trudhesa в сравнение с дихидроерготамин мезилатен спрей при здрави индивиди.
Описаните по -долу клинични проучвания са проведени с помощта на дихидроерготамин мезилатен спрей за нос.
Ефективността на дихидроерготамин мезилатен спрей за нос за остро лечение на мигренозно главоболие е оценена в четири рандомизирани двойно-слепи плацебо контролирани проучвания в САЩ, населението на пациентите за изпитванията е била предимно женски (87%) и кавказки (95%) със средна възраст от 39 години (диапазон 18 до 65 години). Пациентите лекуват еднократно до тежко мигренозно главоболие с една доза лекарство за изследване и оценяваха тежестта на болката през 24 часа след лечението. Реакцията на главоболие се определя 0,5 1 2 3 и 4 часа след дозирането и се определя като намаляване на тежестта на главоболието до лека или никаква болка. В проучвания 1 и 2 е използвана скала за интензивност на болката в четири точки; В проучвания 3 и 4 се използва петточкова скала за запис на реакция на болка. Въпреки че спасителните лекарства са били разрешени и в четирите проучвания пациентите са били инструктирани да не ги използват през четиричасовия период на наблюдение. В проучвания 3 и 4 общата доза от 2 mg е сравнена с плацебо. В проучвания 1 и 2 дози от 2 и 3 mg се оценяват и не показват предимство на по -високата доза за едно лечение. Във всички проучвания пациентите получават режим, състоящ се от 0,5 mg във всяка ноздра, повторен за 15 минути (и отново за още 15 минути за 3 mg доза в проучвания 1 и 2).
Процентът на пациентите, постигащи отговор на главоболие 4 часа след лечението, е значително по -голям при пациенти, получаващи 2 mg дози дихидроерготамин мезилатен спрей в сравнение с тези, които получават плацебо в 3 от 4 -те проучвания (вж. Таблица 2 и Таблица 3 и Фигура 1 и Фигура 2).
Таблица 2 Проучвания 1 и 2: Процент от пациентите с отговор на главоболие a 2 и 4 часа след едно лечение на изследване на лекарствата (дихидроерготамин мезилатен спрей или плацебо)
| N | 2 часа | 4 часа | ||
| Проучване 1 | Дихидроерготамин мезилатен спрей за нос | 105 | 61%** | 70%** |
| Плацебо | 98 | 23% | 28% | |
| Разлика от плацебо | 37% | 42% | ||
| Проучване 2 | Дихидроерготамин мезилатен спрей за нос | 103 | 47% | 56%* |
| Плацебо | 102 | 33% | 35% | |
| Разлика от плацебо | 14% | 21% | ||
| a Реакцията на главоболие се определя като намаляване на тежестта на главоболието до лека или никаква болка. Реакцията на главоболие се основава на интензивността на болката, както се тълкува от пациента, използвайки четириточкова скала за интензивност на болката. *P стойност <0.01 ** P стойност <0.001 |
Таблица 3 Проучвания 3 и 4: Процент от пациентите с отговор на главоболие a 2 и 4 часа след едно лечение на изследване на лекарствата (дихидроерготамин мезилатен спрей или плацебо)
| N | 2 часа | 4 часа | ||
| Проучване 3 | Дихидроерготамин мезилатен спрей за нос | 50 | 32 | 48%* |
| Плацебо | 50 | 20% | 22% | |
| Разлика от плацебо | 12% | 26% | ||
| Проучване 4 | Дихидроерготамин мезилатен спрей за нос | 47 | 30% | 47% |
| Плацебо | 50 | 20% | 30% | |
| Разлика от плацебо | 10% | 17% | ||
| a Реакцията на главоболие се определя като намаляване на тежестта на главоболието до лека или никаква болка. Реакцията на главоболие беше оценена по петточкова скала, която включва реакция на болка. *P стойност <0.01 |
Графиките на Kaplan-Meier по-долу (Фигура 1 и Фигура 2) дават оценка на вероятността пациентът да е реагирал на единична 2 mg доза дихидроерготамин мезилатен спрей като функция на времето, излязло след започване на лечението.
Фигура 1 Оценка на вероятността пациентът да отговори през четирите часа след единична 2 mg доза дихидроерготамин мезилатен спрей като функция на времето, изминало след започване на лечение*
| *Фигурата показва вероятността във времето на получаване на отговор след лечение с дихидроерготамин мезилатен спрей. Реакцията на главоболие се основава на интензивността на болката, както се тълкува от пациента, използвайки скала за интензивност на болката в четири точки. Пациентите, които не постигат отговор в рамките на 4 часа, са цензурирани до 4 часа. |
Фигура 2 Прогнозна вероятност пациент да реагира на дихидроерготамин мезилатен спрей за нос през четирите часа след дозирането*
| *Фигурата показва вероятността във времето на получаване на отговор след лечение с дихидроерготамин мезилатен спрей. Реакцията на главоболие беше оценена по петточкова скала, която включва реакция на болка. Пациентите, които не постигат отговор в рамките на 4 часа, са цензурирани до 4 часа. |
За пациенти с мигрена, свързана с гадене фотофобия и фонофобия в началото, се наблюдава по-ниска честота на тези симптоми на 2 и 4 часа след прилагане на дихидроерготамин мезилатен спрей в сравнение с плацебо.
На пациентите не е позволено да използват допълнителни лечения в продължение на 8 часа преди изследването на дозирането на лекарства и по време на 4-часовия период на наблюдение след лечението на проучването. Following the 4-hour observation period patients were allowed to use additional treatments. За всички проучвания прогнозната вероятност пациентите да използват допълнителни лечения за своите мигрени за 24 часа след единичната 2 mg доза на изследване е обобщена на фигура 3 по -долу.
Фигура 3 Причинена вероятност пациент, използващ допълнителни лечения за мигрена за 24 часа след дихидроерготамин мезилатен спрей 2 mg (или плацебо)*
| *Kaplan-Meier plot based on data obtained from all studies with patients not using additional treatments censored to 24 hours. All patients received a single treatment of study medication for their migraine attack. Сюжетът включва и пациенти, които не са отговорили на първоначалната доза. |
Neither age nor sex appear to affect the patient's response to dihydroergotamine mesylate nasal spray. Расовото разпределение на пациентите е недостатъчно, за да се определи ефекта на раса върху ефикасността на дихидроерготамин мезилатен спрей.
Информация за пациента за Trudhesa
Trusta ™
(Trae - deh - един)
(дихидроерготамин мезилат) носен спрей
Коя е най -важната информация, която трябва да знам за Trudhesa?
Trudhesa може да причини сериозни странични ефекти, включително:
-
- спазми и болка в краката или бедрата
- Усещане за тежест или стегнатост в мускулите на краката ви
- изгаряне или болна болка в краката или пръстите на краката, докато почивате
- изтръпване на изтръпване или слабост в краката ви
- Студеното усещане или цвета се променя в 1 или двата крака или крака
- размазана реч
- Внезапна слабост
-
- Ритонавир
- Еритромицин
- Netfinavir
- Кларитромицин
- Итраконазол
- Trudhesa не се използва за лечение на други видове главоболие като хемиплегични (които ви карат да не можете да се движите от едната страна на тялото си) или базиларна (рядка форма на мигрена с аура) мигрена.
- приемат лекарства, известни като силни инхибитори на CYP3A4.
- Имайте сърдечни проблеми или история на сърдечните проблеми.
- имат неконтролирано високо кръвно налягане.
- имат тежки чернодробни проблеми.
- имат тежки проблеми с бъбреците.
- са приемали някое от следните лекарства през последните 24 часа:
- Суматриптан
- Алмотриптан
- Елетриптан
- frovatriptate
- Наратриптан
- Ризатриптан
Попитайте вашия доставчик на здравни услуги, ако не сте сигурни дали приемате някое от тези лекарства. Your healthcare provider can tell you if it is safe to take TRUDHESA with other medicines.
- имат високо кръвно налягане.
- имат чернодробни проблеми.
- имат проблеми с бъбреците.
- дим.
- са бременни или планират да забременеят. Trudhesa може да причини преждевременно труд. Trudhesa трябва да се избягва по време на бременност. Говорете с вашия доставчик на здравни услуги веднага, ако сте бременна или искате да забременеете.
- са кърмещи или планират да кърмят. TRUDHESA may reduce breast milk supply and pass into your breast milk. TRUDHESA may be harmful to your baby. Do not breastfeed your baby while taking TRUDHESA and for 3 days after you use TRUDHESA. Talk with your healthcare provider about the best way to feed your baby if you take TRUDHESA.
Кажете на вашия доставчик на здравни грижи за всички лекарства, които приемате включително лекарства за рецепта и лекарства без рецепта витамини и билкови добавки. Вашият доставчик на здравни услуги ще реши дали можете да вземете Trudhesa с другите си лекарства.
Особено кажете на вашия доставчик на здравни грижи, ако вземете:
- Някои хора трябва да вземат първата си доза Трудеса в лекарския си кабинет или в друга медицинска обстановка. Попитайте Вашия лекар дали трябва да вземете първата си доза в медицинска обстановка.
- Използвайте Trudhesa точно както вашият доставчик на здравни грижи ви казва да го използвате. Read and follow the instructions in the Инструкции за употреба
- След сглобяване на Trudhesa и грундиране на спрея на устройството 1 време във всяка ноздра (пълна доза).
- Ако главоболието ви се върне след първата пълна доза или получавате само облекчение от главоболието си, можете да използвате втора доза 1 час след първата пълна доза. Използвайте ново устройство за спрей на нос на Trudhesa за втората доза.
- Не използвайте повече от 2 дози Trudhesa в рамките на 24-часов период или 3 дози в рамките на 7-дневен период.
- Ако използвате твърде много Trudhesa, обадете се на вашия доставчик на здравни услуги или отидете веднага в най -близката болнична спешна помощ.
- Вземането на Trudhesa за 10 или повече дни за 1 месец може да влоши главоболието ви. Трябва да напишете, когато имате главоболие и когато вземете Trudhesa, така че да можете да говорите с вашия доставчик на здравни грижи за това как Trudhesa работи за вас.
Какви са възможните странични ефекти на Trudhesa?
Trudhesa може да причини сериозни странични ефекти, включително:
Виж Коя е най -важната информация, която трябва да знам за Trudhesa?
- Сърдечен удар и други сърдечни проблеми. Сърдечните проблеми могат да доведат до смърт. Спрете да приемате Trudhesa и да получите спешна медицинска помощ веднага, ако имате някой от следните симптоми на a сърдечен удар :
- Дискомфорт в центъра на гърдите ви, който трае повече от няколко минути или това отминава и се връща
- Тежка налягане на болката или тежестта в гърдите на гърдите или челюстта
- Болка или дискомфорт в ръцете на ръцете на ръцете или стомаха
- задух със или без дискомфорт на гърдите
- избухване в студена пот
- гадене or повръщане
- Чувствайки се с лекота
Trudhesa не е за хора с рискови фактори за сърдечни заболявания, освен ако не се направи сърдечен изпит и не показва проблем. Имате по -висок риск от сърдечни заболявания, ако:
-
- Имайте високо кръвно налягане
- имат високи нива на холестерол
- дим
- са с наднормено тегло
- имат диабет
- имат фамилна анамнеза за сърдечни заболявания
- Удар. Спрете да приемате Trudhesa и да получите спешна медицинска помощ веднага, ако имате някой от следните симптоми на инсулт:
- лице увиснало
- необичайна слабост или изтръпване
- размазана реч
- Промени в цвета или усещането в пръстите и пръстите на краката (синдром на Рейно).
- Проблеми със стомаха и чревните (исхемични събития на стомашно -чревния и колония). Симптомите на стомашно -чревни и колонични исхемични събития включват:
- Внезапна или силна стомашна болка
- запек или диария
- Болки в стомаха след хранене
- Кървава диария
- загуба на тегло
- треска
- гадене or повръщане
- Увеличете кръвното налягане.
- Медицина Прекомерно използване главоболие. Някои хора, които използват твърде много Trudhesa, могат да влошат главоболието си (лекарство Прекомерно използване на главоболие). Ако главоболието ви се влоши, вашият доставчик на здравни услуги може да реши да спре лечението ви с Trudhesa.
- Преждевременно труд.
- Промените на тъканите (фиброзни усложнения). Nflammation и Fiber-подобна тъкан, която не е нормална (фиброза), може да се появи около белите дробове и стомаха.
- Изгаряне на чувства в носа ви уста и гърло и ненормален вкус.
Най -често срещаните странични ефекти на Trudhesa включват:
- течен нос
- Реакции на сайта на приложението
- сънливост
- гадене
- замаяност
- възпалено гърло
- Ненормален вкус
- повръщане
- диария
Това не са всички възможни странични ефекти Trudhesa.
Обадете се на Вашия лекар за медицински съвети относно страничните ефекти. Можете да отчитате странични ефекти на FDA на 1-800-FDA-1088.
Как трябва да съхранявам Trudhesa?
Дръжте Trudhesa далеч от топлина и светлина.
- Съхранявайте Trudhesa при стайна температура между 68 ° F до 77 ° F (20 ° C до 25 ° C).
- Не се охлаждайте и не замразявайте.
- След отваряне на флакон с трюдхес, той трябва да бъде изхвърлен след 8 часа.
Дръжте Trudhesa и всички лекарства извън обсега на децата.
Не хвърляйте Trudhesa в огън или изгаряне, тъй като кутията вътре в устройството може да избухне.
Обща информация за безопасното и ефективно използване на Trudhesa.
Лекарствата понякога се предписват за цели, различни от тези, изброени в ръководство за лекарства. Не използвайте Trudhesa за условие, за което не е предписано. Не давайте Trudhesa на други хора, дори ако те имат същите симптоми, които имате. Може да им навреди. Можете да попитате вашия фармацевт или доставчик на здравни грижи за информация за Trudhesa, която е написана за здравни специалисти.
Какви са съставките в Trudhesa?
Активна съставка: Дихидроерготамин мезилат
Неактивни съставки: Кофеинов въглероден диоксид декстроза и вода. Канистърът на носно спрей съдържа хидрофлуороалкан-134А (HFA) гориво. Запушалката на флакона не е направена с естествен каучуков латекс. Trudhesa е запазена марка на Impel Neuropharma Inc.
Това ръководство за лекарства е одобрено от американската администрация по храните и лекарствата.
Инструкции за употреба
Trusta ™
(Roe-Sa)
(Дихидроерготамин мезилат)
носен спрей
Само за носна употреба
Въведение
Прочетете тези инструкции за използване, преди да започнете да използвате Trudhesa и всеки път, когато получавате рецепта за пълнене. Може да има нова информация.
Тази информация не заема мястото да разговаряте с вашия доставчик на здравни грижи за вашето медицинско състояние или лечение. Вие и вашият доставчик на здравни грижи трябва да говорите за Trudhesa, когато започнете да го приемате и при редовни прегледи.
Важно е да следвате точно тези указания, за да получите правилната доза. Констактирайте вашия доставчик на здравни грижи, ако имате въпроси как да използвате този продукт.
 |
Части за носно спрей за спрей
 |
Стъклени флаколни части
 |
Важна информация, която трябва да знаете, преди да дозирате с Trudhesa
- Само за използване на носа.
- Винаги правете устройството за спрей за нос, преди да дозирате, като изпомпвате захващането на пръстите и стъкления флакон заедно точно 4 пъти
- Целта на грундирането е да приведе лекарството до върха на накрайника на спрея. Можеш или не можеш да видиш течност или спрей да излизат от дюзата по време на всяко грундиране.
- По време на PrimingMake не забравяйте да насочите пръскащата дюза от лицето си и всичко, което не искате да влезете в контакт с спрея на медицината.
- Пълна доза е 2 спрея; 1 спрей във всяка ноздра.
- Не Вземете повече от 2 дози в рамките на 24-часов период. Не Вземете повече от 3 дози за 7-дневен период.
- Винаги дръжте устройството за спрей на носа напълно изправено при грундиране и при дозиране.
- Поздравяването по време на дозирането не е необходимо. Какевъчът няма да ви навреди, нито ще направи лекарството по -малко ефективно.
- Този продукт за спрей за носно спрей е с една доза (само за една пълна доза) и трябва да бъде изхвърлен (изхвърлен) след употреба. Ще се нуждаете от нов комплект за всяка доза.
- Дръжте продукта в случая до готовност за употреба.
- След отваряне на флакон с трюдхес трябва да бъде изхвърлен след 8 часа.
- Не Отворете стъкления флакон и изложете на въздух до готовност за употреба.
- Съхранявайте на стайна температура в чиста суха зона.
- Не Използвайте, ако продуктът е повреден.
- Не Използвайте, ако продуктът е изтекъл.
- Всяко стъклен флакон и устройство за спрей на носа може да се използва само 1 път. Изхвърлете цялото устройство за спрей за нос след дозиране, без да премахнете стъкления флакон.
- Можете да вземете друга пълна доза поне 1 час след първата си доза, ако симптомите ви продължат.
Съхраняване на Trudhesa
- Съхранявайте Trudhesa при стайна температура между 68 ° F до 77 ° F (20 ° C до 25 ° C).
- Съхранявайте Trudhesa в оригиналната опаковка в чиста зона далеч от топлина и светлина ( Фигура a ).
- Дръжте Trudhesa в оригиналната опаковка, докато не сте готови да използвате.
- Не хладилник или замразяване на трюдеса.
- Дръжте Trudhesa и всички лекарства извън обсега на децата.
 |
Подготовка за доза с Trudhesa
Стъпка 1: Съберете и проверете консумативите
 |
 |
- Проверете дали използвате правилното лекарство за вашата мигрена (вижте Фигура б ).
- Проверете дали Trudhesa не е изтекъл (EXP) (вижте Фигура c ).
- Ако изтече изхвърляне и вземете нов стъклен флакон.
- Проверете, за да се уверите, че стъкленият флакон и синият пластмасов капак не изглеждат повредени.
Стъпка 2: Отстранете синьото пластмасово фолио от мотиватор и сивата гумена запушалка от стъкления флакон
 |
 |
 |
- Извадете (обърнете) синия пластмасов капак от стъкления флакон (виж Фигура г. г. ).
- Използвайте синия пластмасов капак, за да отлепите бавно металното фолио от сивата гумена запушалка в кръгово движение (виж Фигура Е. ).

- Издърпайте сивата гумена запушалка нагоре и от стъкления флакон ( Фигура f и Фигура g ).
- Хвърлете (изхвърлете) покривно фолио и сивата гумена запушалка в кошчето.
Стъпка 3: Отстранете прозрачния пластмасов капак от устройството за спрей на носа
- Задръжте устройството на носния SPPRAY изправено.
- Издърпайте върху прозрачния пластмасов капак и го отстранете от устройството за спрей на носа ( Фигура З. ).
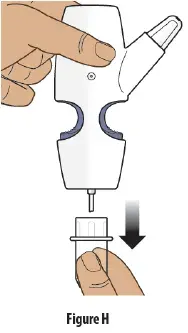
- Изхвърлете скъпия пластмасов капак.
Стъпка 4: Завийте стъкления флакон в устройството за спрей на носа
 |
 |
- Задръжте устройството за спрей на носа изправено.
- Внимателно избутайте стъклен флакон в дъното на носното устройство Sparay (виж Фигура i ) и го завийте, докато не бъде закрепено, както е показано в Фигура j .
Стъпка 5: Намерете устройството за спрей на носа, като изпомпвате четири пъти с пръсти и палец
 |
- Дръжте устройството за спрей на носа изправен .
- Насочете накрайника на пръскането далеч от лицето си.
- Поставете палеца си в долната част на стъкления флакон и поставете показалеца си (индекс) и средните пръсти на ръчките на пръстите (виж Фигура К. ).
- Помпайте устройството за спрей на носа точно 4 пъти.
- За да изпомпвате устройството за спрей на носа здраво натиснете пръста на схватката и натиснете стъкления флакон нагоре едновременно. След това пуснете (виж Фигура К. )
- Може да видите някакво лекарство спрей по време на грундиране. Това е нормално. Добре е, ако не виждате лекарство да спрете на първите няколко помпи.
Важен съвет: Целта на грундирането е да приведе лекарството до върха на накрайника на спрея. Ако не разгледате устройството за спрей на носа, няма да получите правилната си доза медицина.
Винаги преработвайте устройството за спрей за нос преди употреба, като изпомпвате точно 4 пъти.
По време на грундиране не забравяйте да насочите дюзата от лицето си и всичко, което не искате да влезете в контакт с спрея на медицината.
Използване на Trudhesa
Стъпка 6: Позиционирайте устройството за спрей на носа
 |
- Обърнете или похвалете носното Sprey устройство, така че накрайникът за спрей да се изправи пред вас.
- Уверете се, че главата ви е права и устройството за спрей за нос е изправено.
- Поставете накрайника Sparay в първата си ноздра, доколкото е удобно (вижте Фигура л ).
Стъпка 7: Напръскайте първия спрей в 1 ноздра
- Твърдо натиснете пръста на пръста надолу и натиснете стъкления флакон нагоре едновременно, за да доставите първия спрей (виж Фигура m ).Then release.
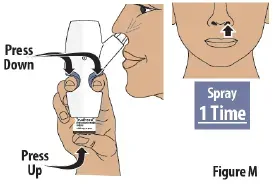
- Доставете само 1 спрей в тази ноздра.
Стъпка 8: Напръскайте втория спрей в друга ноздра
- Преместете спрей на дюзата в другата си ноздра.
- Твърдо натиснете пръста на пръста надолу и натиснете стъкления флакон нагоре едновременно, за да доставите втория спрей (виж Фигура n ).Then release.
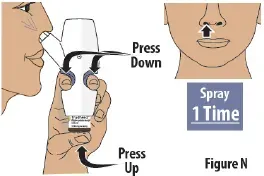
- Доставете само 1 спрей в тази ноздра.
Важен съвет: Пълна доза е 2 спрея; 1 спрей във всяка ноздра.
Максимална доза габапентин за тревожност
Не Вземете повече от 2 дози в рамките на 24-часов период. Не Вземете повече от 3 дози за 7-дневен период.Please refer to the prescribing information for more information.
Сухането, докато или след дозирането не е необходимо. Как се е наранили, няма да ви навреди или да направи лекарството по -малко ефективно.
Важни често задавани въпроси (често задавани въпроси)
ВЪПРОС: Мога ли да запазя медицината, като прескачам 4 помпи в „Стъпка 5: Направете устройството за спрей за нос“?
Отговор: Никакво пропускане на 4 -те помпи, за да се преодолее устройството за спрей за нос, не може да доведе до това, че не получавате правилната си доза лекарство.
QESTION: Когато за първи път изпомпвах устройството за спрей за нос, за да не се появи нищо не се случи. Защо?
Отговор: Целта на грундирането е да приведе лекарството до върха на дюзата. Въпреки че не можете да видите или чуете нещо на първата си помпа или две, помпеното действие ще премести лекарството от стъкления флакон през вътрешността на устройството за спрей на носа и в дюзата. Трябва да видите спрей от четвъртия си опит за помпа. Винаги, като изпомпвате точно 4 пъти преди дозирането.
ВЪПРОС: Мога ли да използвам повторно устройството за спрей на нос с нов стъклен флакон?
Отговор: Нищото устройство за спрей за нос е само за еднократна употреба и трябва да бъде изхвърлено, след като сте затворили (1 спрей във всяка ноздра). Това е така, защото устройството може да се запуши. След като дозирате стъкления флакон, завинлив върху устройството за пръскане на носа и изхвърлете сглобеното устройство за пръскане в кошчето. Не рециклирайте нито една част от продукта.
Въпрос: Мога ли да използвам лекарството, което остава в стъкления флакон за по -късна доза?
Отговор: NOALY, въпреки че е nrmal някакво лекарство да остане в стъкления флакон, той не може да се използва за по -късно дозиране. Всеки остатъчен лекарства ще стане неефективен.
Въпрос: Какво се случва, ако спарай повече от един път в една и съща ноздра?
Отговор: Пълна и правилна доза е по един спрей във всяка ноздра.
Въпрос: Колко скоро мога да взема друга доза, ако не получавам облекчение от мигрената си?
Отговор: Можете да вземете още една доза AR най -малко 1 час след първата ви доза, ако симптомите ви продължават. Не Вземете повече от 2 дози в рамките на 24-часов период. Не Вземете повече от 3 дози за 7-дневен период.Please refer to the prescribing information for more information.
Тези инструкции за употреба са одобрени от администрацията на САЩ и лекарствата.




