Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
ЛекарстваAllocord
Резюме на наркотиците
Какво е Allocord?
Allocord (Хематопоетична инжекция на клетките на прогениторните прогенитор) е алогенна терапия с хематопоетична клетъчна терапия на кръв придобити или резултат от миелоаблативно лечение.
Какви са страничните ефекти на Allocord?
Общите странични ефекти на Allocord включват:
- Високо кръвно налягане (хипертония)
- повръщане
- гадене
- Бавна сърдечна честота
- треска
- Реакции на свръхчувствителност (бронхоспазъм хриптящ кожа на кожата сърбеж и кошери)
- строгост или
- втрисане
- промиване
- задух
- Болки в гърдите
- кръв в урината
- Ниско кръвен кислород
- Бърза сърдечна честота
- промени във вкуса и
- Леко главоболие
Дозировка за Allocord
Препоръчителната минимална доза Allocord е 2,5 x 107 нуклеирани клетки/kg при криоконсервация.
Какви лекарства вещества или добавки взаимодействат с Allocord?
Allocord може да взаимодейства с други лекарства. Кажете на Вашия лекар всички лекарства и добавки, които използвате.
Алокорд по време на бременност или кърмене
Кажете на Вашия лекар, ако сте бременна или планирате да забременеете, преди да използвате Allocord; Не е известно как би се отразил на плода. Консултирайте се с Вашия лекар преди кърмене.
Допълнителна информация
Нашият Allocord (Хематопоетична прогенитална клетъчна клетъчна кръв в кръвта на човека) Странични ефекти Центърът за лекарства предоставя цялостен поглед върху наличната информация за лекарството за потенциалните странични ефекти при приемането на това лекарство.
припадъци, които започват с t
Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Странични ефекти
- Предупреждения
- Предозиране
- Клинична фармакология
- Ръководство за лекарства
Предупреждение
Фатална инфузионна реакция присаждане срещу присаждане на болест на гостоприемника и повреда на присадката
Фатални реакции на инфузия
Прилагането на Allocord може да доведе до сериозни, включително фатални реакции на инфузия. Наблюдавайте пациентите и преустановете инфузията на Allocord за тежки реакции. [Вижте ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Присаждане срещу болест на гостоприемника (GVHD)
GVHD се очаква след прилагане на алокорд и може да бъде фатален. Прилагането на имуносупресивна терапия може да намали риска от GVHD [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Синдром на присаждане
Синдромът на присаждането може да премине към многоорганна недостатъчност и смърт. Лекувайте синдрома на присаждане бързо с кортикостероиди [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Повреда на присадката
Неуспехът на присадката може да е фатален. Следете пациентите за лабораторни доказателства за възстановяване на хематопоетично. Преди да изберете специфична единица Allocord, помислете за тестване за HLA антитела за идентифициране на пациенти, които са алоимунизирани [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Описание за Allocord
Allocord се състои от хематопоетични прогениторни клетки моноцити лимфоцити и гранулоцити от човешка кръв от връв за интравенозна инфузия. Кръвта, възстановена от пъпната връв и плацентата, е намалена обем и частично изчерпана от червените кръвни клетки и плазмата.
Активната съставка са хематопоетични прогениторни клетки, които експресират маркера на клетъчната повърхност CD34. Потенциалността на кръвта от връв се определя чрез измерване на броя на общите нуклеирани клетки (TNC) и CD34 клетки и клетъчна жизнеспособност. Всяка единица на Allocord съдържа минимум 5 x 10 8 Общо нуклеирани клетки с поне 1,25 х 10 6 жизнеспособни CD34 клетки по време на криоконсервация. Клетъчният състав на Allocord зависи от състава на клетките в кръвта, възстановена от пъпната връв и плацентата на донора. Действителният брой на клетките с нуклеирани клетки CD34 броя на групата ABO и HLA въвеждането са изброени в придружаващи записи, изпратени с всяка отделна единица.
Allocord има следните неактивни съставки: разтвор на подготовка на CB Цитратфосфат-декстроза диметил сулфоксид (DMSO) и декстран 40. Когато се приготвя за инфузия съгласно инструкциите, инфузатът съдържа следните неактивни съставки: Подготвен-CB Раздел за разделяне Цитрат-фосфат-Декстрозен Dextran 40 Човешкият сервен и остатък DMSO.
Използване за Allocord
ALLOCORD HPC (Hematopoietic Progenitor Cell) Cord Blood is an allogeneic cord blood hematopoietic progenitor cell therapy indicated for use in unrelated donor hematopoietic progenitor stem cell transplantation procedures in conjunction with an appropriate preparative regimen for hematopoietic and immunologic reconstitution in patients with disorders affecting the hematopoietic system that are inherited acquired or резултат от миелоаблативно лечение.
Оценката на риска от полза за отделен пациент зависи от характеристиките на пациента, включително рисковите фактори на стадия на заболяването и специфичните прояви на заболяването върху характеристиките на присадката и други налични лечения или видове хематопоетични прогениторни клетки.
Дозировка за Allocord
- Само за интравенозна употреба.
- Не облъчвайте.
Изборът на единица и прилагането на Allocord трябва да се извършва под ръководството на лекар, преживян при трансплантация на хематопоетични прогениторни клетки.
Дозиране
Препоръчителната минимална доза е 2,5 х 10 7 нуклеирани клетки/kg при криоконсервация. Може да се изискват множество единици, за да се постигне подходящата доза.
Препоръчва се най-малко 4 от 6 HLA-A антигени HLA-B антигени и HLA-DRB1 алели. HLA типизиране и нуклеирано съдържание на клетки за всяка отделна единица на Allocord са документирани в придружаващи записи.
Подготовка за инфузия
Allocord трябва да бъде подготвен от обучен медицински специалист.
- Не облъчвайте алокорд.
- Вижте добавените подробни инструкции за приготвяне на Allocord за инфузия.
- След като бъде приготвен за инфузионна алокорд, може да се съхранява при 4 до 25 ° C за до 4 часа [виж Инструкции за подготовка за инфузия ].
- Препоръчителният лимит за прилагането на DMSO е 1 грам на kg телесно тегло на ден [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ и Предозиране ].
Администрация
Allocord трябва да се прилага под надзора на квалифициран специалист по здравни грижи, опитващ се в трансплантацията на хематопоетични прогениторни клетки.
- Потвърдете самоличността на пациента за определената единица на Allocord преди прилагането.
- Потвърдете, че аварийните лекарства са налични за употреба в непосредствена близост.
- Уверете се, че пациентът е хидратиран адекватно.
- Премика на пациента 30 до 60 минути преди прилагането на Allocord. Премедикацията може да включва всяко или всички от по -долу: антипиретици хистаминови антагонисти и кортикостероиди.
- Проверете продукта за всички аномалии като необичайни частици и за нарушения на целостта на контейнера преди администрирането. Преди инфузия обсъдете всички подобни неравности на продукта с лабораторията, издаваща продукта за инфузия.
- Администрирайте алокорд чрез интравенозна инфузия. Не се прилагайте в същата тръба едновременно с продукти, различни от 0,9% инжекция на натриев хлорид (USP). Allocord може да бъде филтриран през филтър от 170 до 260 микрона, предназначен да премахне съсиреци. Не използвайте филтър, проектиран за отстраняване на левкоцити.
- За възрастни започват инфузия на алокорд при 100 милилитра на час и увеличават скоростта като поносими. За децата започват инфузия на алокорд при 1 милилитър на kg на час и се увеличават, както се понасят. Намалете скоростта на инфузия, ако натоварването на течността не се толерира. Преустановете инфузията в случай на алергична реакция или ако пациентът развие умерена до тежка инфузионна реакция [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ и Нежелани реакции ].
- Следете пациента за нежелани реакции по време и поне шест часа след прилагането. Тъй като Allocord съдържа лизирани червени клетки, които могат да причинят и бъбречна недостатъчност, внимателно наблюдение на изхода на урината, също се препоръчва.
Забележка
Ако продуктът се подготвя за инфузионни единици за инфузия с мулти-единица независимо. Ако възникне реакция по подходящ начин реакцията, преди да бъде размразена втора единица за инфузия.
Колко се доставя
Дозирани форми и силни страни
Всяка единица на Allocord съдържа минимум 5 x 10 8 Общо нуклеирани клетки с минимум 1,25 х 10 6 Жизнеспособни CD34 клетки, суспендирани в 10% диметил сулфоксид (DMSO) и 1% декстран 40 по време на криоконсервацията.
Точното съдържание на клетъчни клетки преди крийоконсервация е предоставено в придружаващи записи.
Съхранение и обработка
Allocord се доставя като криоконсервирана клетъчна суспензия в запечатана торбичка, съдържаща минимум 5 x 10 8 Общо нуклеирани клетки с минимум 1,25 х 10 6 жизнеспособни CD34 клетки в обем от 35 милилитра (ISBT 128 Код на продукта S1393 ISBT 128 Идентификатор на съоръжението W1205). Точното съдържание на клетъчни клетки преди крийоконсервация е предоставено в придружаващи записи.
Съхранявайте Allocord при или под -150 ° C до готовност за размразяване и подготовка.
Разпространено от: SSM Cardinal Glennon Детски медицински център DBA St. Louis Cord Blood Bank 1465 South Grand Blvd. Ревизиран: юли 2015 г.
Странични ефекти за алокорд
Смъртността на ден-100 от всички причини е била 25%.
Най-често срещаните нежелани реакции, свързани с инфузия (≥ 5%), са хипертония, повръщайки гадене брадикардия и треска.
Опит с клинични изпитвания
Тъй като клиничните изпитвания се провеждат при широко различни състояния, нежелани реакционни проценти, наблюдавани при клиничните изпитвания на лекарство, не могат да бъдат пряко сравнени със проценти в клиничните изпитвания на друго лекарство и може да не отразяват процентите, наблюдавани на практика.
Оценката на безопасността на Allocord се основава предимно на преглед на данните, предоставени на докетите на FDA от различни източници, наборът от данни за изследването на COBLT и публикуваната литература.
Инфузионни реакции
Данните, описани в таблица 1, отразяват експозицията на 442 инфузии на кръвта от връв на HPC (от множество банки на кръвта на връв) при пациенти, лекувани с помощта на обща нуклеирана клетъчна доза ≥ 2,5 x 10 7 /kg на еднократна перспектива или разширена употреба на достъп (Coblt Study). Населението е 59% мъже, а средната възраст е 5 години (диапазон 0,05-68 години) и включва пациенти, лекувани за хематологични злокачествени заболявания, наследяват метаболитни разстройства, първични имунодефицити и недостатъчност на костния мозък. Подготвителните режими и профилактиката на присадката-Vs.-хост болест не са стандартизирани. Най -често срещаните инфузионни реакции са хипертония, повръщайки гадене и синусова брадикардия. Хипертонията и всякакви реакции, свързани с инфузия 3-4, се проявяват по-често при пациенти, получаващи HPC кабелна кръв в обеми, по-големи от 150 милилитра и при педиатрични пациенти. Скоростта на сериозни неблагоприятни кардиопулмонални реакции е 0,8%.
Варфарин ли е същият като Кумадин
Таблица 1: Честота на нежеланите реакции, свързани с инфуза, възникващи при ≥1% от инфузиите (COBLT проучване)
| Всяка оценка | 3-4 клас | |
| Всяка реакция | 65,4% | 27,6% |
| Хипертония | 48.0% | 21,3% |
| Повръщане | 14.5% | 0,2% |
| Гадене | 12,7% | 5.7% |
| Синус брадикардия | 10,4% | 0 |
| Треска | 5.2% | 0,2% |
| Синусова тахикардия | 4,5% | 0,2% |
| Алергия | 3.4% | 0,2% |
| Хипотония | 2,5% | 0 |
| Хемоглобинурия | 2.1% | 0 |
| Хипоксия | 2,0% | 2,0% |
Информацията за реакциите на инфузия беше налична от доброволни доклади за 737 пациенти, които са получили Allocord. Подготвителните режими и профилактиката на присадката-Vs.-хост болест не са стандартизирани. Реакциите не са оценени. Инфузионна реакция е възникнала при 13% от пациентите. Най -често срещаните инфузионни реакции, възникващи при ≥ 1%от пациентите, са хипертония (54%) повръщане (12%) диспнея (9%) брадикардия (6%) гадене (4%) болки в гърдите (2%) хемоглобинурия (2%) треска (2%) и кокички (2%).
Други нежелани реакции
За други нежелани реакции суровите клинични данни от докетите се обединяват за 1299 (120 възрастни и 1179 педиатрични) пациенти, трансплантирани с кръв от връв на HPC (от множество банки от кръв от връв) с обща ядрена клетъчна доза ≥ 2,5 x 10 7 /kg. От тези 66% (n = 862) са претърпели трансплантация като лечение на хематологично злокачествено заболяване. Подготвителните режими и профилактиката на присадката-Vs.-хост болест варираха. Средната обща нуклеирана клетъчна доза е 6,4 х 10 7 /kg (диапазон 2,5-73,8 x 10 7 /kg). За тези пациенти Смъртността от ден- 100 от всички причини е била 25%. Първичната недостатъчност на присадката е възникнала при 16%; 42% са развили 2-4 Остра болест на присадката-Vs.-хост; и 19% са развили 3-4 клас остра болест на присадката-Vs.-хост.
Данните от публикуваната литература и от наблюдателните регистри институционални бази данни и прегледите на банката на кръвта от шнур, докладвани на докетите за кръвта на връвта на HPC (от множество банки на кръвта на връвта), разкриха девет случая на донорна клетъчна левкемия, един случай на предаване на инфекция и един доклад за трансплантация от донор с наследствено генетично разстройство. Данните не са достатъчни, за да поддържат надеждни оценки на случаите на тези събития.
В изследването на COBLT 15% от пациентите са развили синдрома на присаждане.
Tylenol 4 срещу Norco 10 325
Лекарствени взаимодействия за Allocord
Не е предоставена информация
Предупреждения за Allocord
Включени като част от 'ПРЕДПАЗНИ МЕРКИ' Раздел
Предпазни мерки за Allocord
Реакции на свръхчувствителност
Алергичните реакции могат да възникнат с инфузия на кръв от връв на HPC, включително Allocord. Реакциите включват бронхоспазъм хриптящ ангиоедем сърбеж и кошери [виж Нежелани реакции ]. Serious hypersensitivity reactions including anaphylaxis also have been reported. These reactions may be due to dimethyl sulfoxide (DMSO) Dextran 40 or a plasma component of Allocord.
Allocord may contain residual antibiotics if the cord blood donor was exposed to antibiotics in utero. Patients with a history of allergic reactions to antibiotics should be monitored for allergic reactions following Allocord administration.
Инфузионни реакции
Очаква се инфузионните реакции да се появят и включват гадене, повръщащи се треска строгост или втрисане, промиване на диспнея Хипоксемия Стегнатост на гърдите Хипертония тахикардия брадикардия Дисгеус хематурия и леко главоболие. Премедикацията с антипиретици хистаминови антагонисти и кортикостероиди може да намали честотата и интензивността на инфузионните реакции.
Тежка реакция, включително респираторен дистрес, тежка бронхоспазъм Тежка брадикардия със сърдечен блок или други аритмии Сърдечно спиране Хипотония хемолиза на хемолизата Повишени чернодробни ензими Бъбречни компромиси Енцефалопатия Загуба на съзнание и припадък също може да се появи. Много от тези реакции са свързани с количеството на прилагания DMSO. Минимизирането на количеството на прилагания DMSO може да намали риска от такива реакции, въпреки че идиосинкратичните отговори могат да възникнат дори при дози DMSO, за които се смята, че се понасят. Действителното количество DMSO зависи от метода на приготвяне на продукта за инфузия. Препоръчва се ограничаване на количеството DMSO, влято в не повече от 1 грам на килограм на ден [виж Предозиране ].
Инфузионните реакции могат да започнат в рамките на минути след началото на инфузията на алокорд, въпреки че симптомите могат да продължат да се засилват, а не пик в продължение на няколко часа след приключване на инфузията. Следете внимателно пациента през този период. Ако възникне реакция, прекрати инфузията и института за поддържаща грижа, ако е необходимо.
Ако влязът на повече от една единица HPC кабелна кръв в един и същи ден не прилага последващи единици, докато всички признаци и симптоми на реакции на инфузия от предходната единица не са разрешени.
Болест на присадката срещу -хост
Острата и хроничната болест на присадката срещу гостоприемника (GVHD) може да възникне при пациенти, които са получили Allocord. Класическият остър GVHD се проявява като обрив на треска, повишен билирубин и чернодробни ензими и диария. Пациентите, трансплантирани с Allocord, също трябва да получават имуносупресивни лекарства, за да намалят риска от GVHD [виж Нежелани реакции ].
Синдром на присаждане
Синдромът на присаждането се проявява като необяснима треска и обрив в периода на присаждане. Пациентите със синдром на присаждане също могат да имат необяснимо хипоксемия на теглото и белодробни инфилтрати при липса на претоварване на течности или сърдечно заболяване. Ако нелекуваният синдром на присаждане може да премине към многоорганна недостатъчност и смърт. Започнете лечението с кортикостероиди, след като синдромът на присаждането е разпознат, за да се подобри симптомите [виж Нежелани реакции ].
Повреда на присадката
Първичната повреда на присадката, която може да бъде фатална, се определя като неуспех за постигане на Абсолютен брой неутрофили по -голяма от 500 на микролитър кръв на ден 42 след трансплантация. Имунологичното отхвърляне е основната причина за повреда на присадката. Пациентите трябва да бъдат наблюдавани за лабораторни доказателства за възстановяване на хематопоетично. Помислете за тестване за HLA антитела, за да идентифицирате пациенти, които са алоимунизирани преди трансплантацията и да помогнете при избора на единица с подходящ HLA тип за отделния пациент [виж Нежелани реакции ].
Злокачествени заболявания от донорски произход
Пациентите, които са претърпели трансплантация на кръвна кръв на HPC, могат да развият лимфопролиферативно разстройство след трансплантация (PTLD), проявено като лимфомно заболяване, благоприятстващо не-нодалните места. PTLD обикновено е фатален, ако не се лекува.
Честотата на PTLD изглежда е по -висока при пациенти, които са получили антитимоцитен глобулин. Смята се, че етиологията са донорски лимфоидни клетки, трансформирани от вируса на Epstein-Barr (EBV). Серийният мониторинг на кръвта за EBV ДНК може да бъде оправдан във високорискови групи.
Левкемия от донорски произход също е съобщено при получателите на кръв от HPC Cord. Счита се, че естествената история е същата като тази за отново левкемия.
Предаване на сериозни инфекции
Предаването на инфекциозно заболяване може да възникне, тъй като алокордът се получава от човешка кръв. Болестта може да бъде причинена от известни или неизвестни инфекциозни агенти. Донорите се проверяват за повишен риск от инфекция с вирус на имунодефицит на човека (ХИВ) Човешки Т-клетъчен лимфотропен вирус (HTLV) Хепатит В вирус (HBV) Хепатит С вирус (HCV) Т. Блек Т. Крузи Западният вирус на вируса (WNV), предаваема спонгиформна енцефалопатия (TSE) агенти и ваксини. Донорите също са прегледани за клинични доказателства за сепсис и рискове за заразни болести, свързани с ксенотрансплантация. Пробите от кръвта на майката се тестват за ХИВ типове 1 и 2 HTLV типове I и II HBV HCV Т. Блек WNV и Т. Крузи . Allocord се тества за стерилност. Тези мерки не премахват напълно риска от предаване на тези или други преносими инфекциозни заболявания и заболявания. Съобщете за появата на заподозряна предавана инфекция на банката за кръв от Сейнт Луис Корд на детския медицински център на SMM Cardinal Glennon в 1-888-253-Cord (1-888-253-2673).
Изпитването също се извършва за доказателства за донорска инфекция поради цитомегаловирус (CMV). Резултатът може да бъде намерен в придружаващи записи.
Предаване на редки генетични заболявания
Allocord may transmit rare genetic diseases involving the hematopoietic system for which donor screening и/or testing has не been performed [see Нежелани реакции ]. Cord blood donors have been screened by family history to exclude inherited disorders of the blood и marrow. Allocord has been tested to exclude donors with sickle cell anemia и anemias due to abnormalities in hemoglobins C D и E. Because of the age of the donor at the time Allocord collection takes place the ability to exclude rare genetic diseases is severely limited.
Използване в конкретни популации
Бременност
Бременност Category C
Изследванията за възпроизвеждане на животни не са проведени с Allocord. Също така не е известно дали Allocord може да причини вреда на плода, когато се прилага на бременна жена или може да повлияе на капацитета за възпроизвеждане. Няма адекватни и добре контролирани проучвания при бременни жени. Allocord трябва да се използва по време на бременност само ако потенциалната полза оправдае потенциалния риск за плода.
Педиатрична употреба
Кръвта на връвта на HPC е използвана при педиатрични пациенти с нарушения, засягащи хематопоетичната система, които са наследени или са резултат от миелоаблативно лечение [виж Доза и приложение Нежелани реакции и Клинични изследвания ].
Гериатрична употреба
Клиничните проучвания на кръвта на връвта на HPC (от множество банки на кръвта на връвта) не включват достатъчен брой лица на възраст 65 години и повече, за да се определи дали реагират по различен начин от по -младите лица. Като цяло прилагането на алокорд за пациенти на възраст над 65 години трябва да бъде предпазливо, отразяващо по -голямата им честота на намалена чернодробна бъбречна или сърдечна функция и на съпътстващо заболяване или друга лекарствена терапия.
Бъбречно заболяване
Allocord contains Dextran 40 which is eliminated by the kidneys. The safety of Allocord has не been established in patients with renal insufficiency or renal failure.
Информация за предозиране за Allocord
Възраст на човешки предотвратяване на възрастта
Не е имало опит с предозиране на кръв от връв на HPC при клинични изпитвания при хора. Единични дози Allocord до 67.0 x 10 7 Прилагат се TNC/kg. HPC кръвта от връв, приготвена за инфузия, може да съдържа диметил сулфоксид (DMSO). Максималната поносима доза на DMSO не е установена, но е обичайно да не се надвишава DMSO доза от 1 gm/kg/ден, когато се дава интравенозно. Съобщават се за няколко случая на променен психичен статус и кома с по -високи дози DMSO.
Управление на предозиране
За DMSO е посочена обща поддържаща грижа за DMSO. Ролята на други интервенции за лечение на предозиране на DMSO не е установена.
Противопоказания за Allocord
Няма
Клинична фармакология for Allocord
Механизъм на действие
Хематопоетични стволови/прогениторни клетки от кръвта на HPC кабел мигрират към костния мозък, където се разделят и узряват. Зрелите клетки се освобождават в кръвта, където някои циркулират, а други мигрират към местата на тъканите частично или напълно възстановяват кръвната картина и функцията, включително имунната функция на кръвоносните клетки от мозъчен произход [виж Клинични изследвания ].
При пациенти с ензимни аномалии поради някои тежки видове нарушения на съхранението зрели левкоцити в резултат на трансплантацията на HPC на връвта могат да синтезират ензими, които могат да могат да циркулират и подобрят клетъчните функции на някои местни тъкани. Въпреки това точният механизъм на действие е неизвестен.
Клинични изследвания
Ефективността на кръвта на връвта на HPC, дефинирана чрез хематопоетично възстановяване, беше демонстрирана в едно проспективно проучване с едно оръжие (COBLT проучване) и в ретроспективни прегледи на данни от наблюдателна база данни за алокорд и данни в докетите и обществената информация. От 1299 пациенти в докетите и публичните данни 66% (n = 862) са претърпели трансплантация като лечение на хематологично злокачествено заболяване. Резултати за пациенти, които са получили обща нуклеирана клетъчна доза ≥2,5 х 10 7 /kg са показани в таблица 2. Възстановяването на неутрофилите се определя като времето от трансплантация до абсолютен брой неутрофили повече от 500 на микролитър. Възстановяването на тромбоцитите е времето за броя на тромбоцитите над 20000 на микролитър. Възстановяването на еритроцитите е времето за броя на ретикулоцитите, по -голям от 30000 на микролитър. Общата нуклеирана клетъчна доза и степен на съвпадение на HLA бяха обратно свързани с времето за възстановяване на неутрофили в данните на Docket.
Таблица 2: Хематопоетично възстановяване за пациенти, трансплантирана с доза с нуклеирана клетка (TNC) на HPC в кръвта на HPC (TNC) ≥ 2,5 x 10 7 /kg
| Източник на данни | Coblt Study* | Docket* и обществени данни* | Allocord |
| Дизайн | Перспективна единична ръка | Ретроспектива | Ретроспектива |
| Брой пациенти | 324 | 1299 | 1086 |
| Средна възраст (години) (обхват) | 4.6 (0.07 - 52.2) | 7.0 ( <1 - 65.7) | 6.6 (NULL,05 - 70) |
| Пол | 59% мъжки 41% женска | 57% мъжки 43% жена | 54% мъжки 43% жена 3% неизвестно |
| Средна доза TNC (x 10 7 /kg) (range) | 6.7 (2.6 - 38.8) | 6.4 (2.5 - 73.8) | 6.4 (2.5 - 67.0) |
| Възстановяване на неутрофили на 42 -ия ден (95% CI) | 76% (71% - 81%) | 77% (75% - 79%) | 88%** (85% - 91%) |
| Възстановяване на тромбоцитите на ден 100 от 20000/микролитър (95% CI) | 57% (51% - 63%) | - | 87%** (83% - 91%) |
| Възстановяване на тромбоцитите на ден 100 от 50000/микролитър (95% CI) | 46% (39% - 51%) | 45% (42% - 48%) | 79%** (73% - 83%) |
| Възстановяване на еритроцитите на ден 100 (95% CI) | 65% (58% - 71%) | - | - |
| Средно време за възстановяване на неутрофили | 27 дни | 25 дни | 21 дни ** |
| Средно време за възстановяване на тромбоцитите от 20000/микролитър | 90 дни | - | 48 дни ** |
| Средно време за възстановяване на тромбоцитите от 50000/микролитър | 113 дни | 122 дни | 56 дни ** |
| Средно време за възстановяване на еритроцитите | 64 дни | - | - |
| * HPC кръв от връв (от множество банки в кръвта на шнура) ** Анализът на хематопоетичното възстановяване се основава на различен брой пациенти, вариращи от 335 до 4 4 2 за всяка променлива, тъй като количеството на липсващите данни е различно за всяка променлива. |
Информация за пациента за Allocord
Обсъдете следното с пациентите, получаващи Allocord:
- Съобщете незабавно всякакви признаци и симптоми на остри инфузионни реакции, като треска в охлаждане на умора дишане на дишането на замаяност гадене повръщане главоболие или мускулни болки.
- Докладвайте незабавно всякакви признаци или симптоми, предполагащи засаждане на болест на присадката-Vs., включително обривна диария или пожълтяване на очите.
Инструкции за подготовка за инфузия
- Оборудвани реагенти и консумативи
Оборудване:
Биологичен кабинет за безопасност
Водна баня 37 ° С
Топлинен уплътнител
Мащаб
Автоматизиран брояч на клетките
Проточен цитометър
МикроскопРеагенти:
25% албум (човек) USP
Dextran 40 при инжекция на натриев хлорид USP или Dextran 40 при инжекция на декстроза USPДоставки:
Стерилна уплътнима торбичка с цип
Спринцовки - 1 ml 3 ml 5 ml 30 ml 60 ml
18 габаритни игли за безопасност
Тъпи пластмасови канюли
Стерилни капачки за спринцовка (двоен край: мъж/жена)
Алкохолни кърпички
Плазмени трансферни комплекти (2 инчови тръби женски адаптер за луер) - включени в доставката на продукта
Трансферни пакети - 150 ml 300 ml
Флакони за кръвна култура
Устройство за кръвна култура
Хемостат
2 ml криовиал
Дългосрочни странични ефекти на кселода
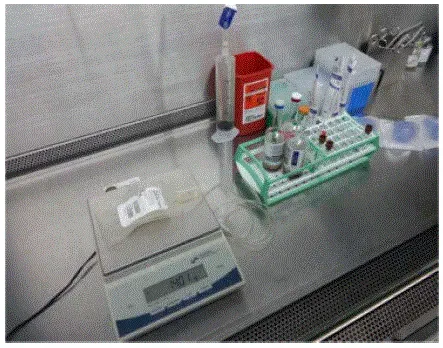
- Инструкции за получаване
Allocord is shipped frozen in a steel canister that is contained in an insulating foam sleeve. Allocord must be stored at or below -150 °C either inside the container used for shipping (dryshipper) or in a liquid nitrogen (LN 2 ) -Кохлатирано устройство за съхранение в центъра за трансплантация (препоръчително).
След получаване на пратката извършват следните стъпки:
- Потвърдете получаването на пратката и самоличността на очакваната единица.
- Проверете изпращача за подправяне или повреда преди отварянето.
- Претеглете изпращача и документирайте теглото върху формуляра за получаване на единица.
- Забележка the temperature displayed on the data logger и document the temperature on the Unit Receipt Form.
- Използване на криопротективни ръкавици Отстранете продукта от кутията и поставете в резервоар с LN 2 или във фазата на парата на aln 2 Фризер.
- Внимателно отворете касетата. Проверете целостта на получените (ите) единици и документирайте неговите условия във формуляра за получаване на единица.
- Потвърдете идентичността на единицата за кръв от връв. Включете тази проверка във формуляра за получаване на единица.
- Съхранявайте продукта в LN 2 Съдът за съхранение, който поддържа температура под -150 ° C.
- Резервирайте пробите, които придружават единицата като източник на ДНК за потвърждаващо тестване или след присаждане на проучвания:
- На единицата остава сегмент; Резервирайте го преди да размразите устройството
- Аликвота, съдържаща материала, останал от редукцията на червените кръвни клетки/плазмата
- Аликвота, съдържаща неманипулирана кръв от шнур, събрана в цитрат фосфатна декстроза (CPD)
- Спот карта, съдържаща неманипулирана кръв от шнур, събрана в CPD (в плик)
- Сменете температурата на сондата за регистрация на данните вътре в вътрешния контейнер за сух доставчик, ако е необходимо, и сглобете изпращача за връщане.
- Факс попълненият формуляр за получаване на единица до банката на Сейнт Луис Корд на банката на SSM Cardinal Glennon Детски център на 314-268-4186.
Забележка: Освен сегмента спомагателни проби са не предназначени да представят броя на клетките или потентността на криоконсервирания продукт.
Забележка: Ако има всеки Грешка или неяснота по отношение на документацията на продукта Затворете кутията и запазете продукта в LN 2 температура. Незабавно посъветвайте персонала на банката за кръв от Сейнт Луис Корд и лекар по трансплантация . Не продължете, докато проблемът не бъде решен. Ако вашият ln 2 Резервоарите за съхранение нямат място за съхранение на продукта в неговия кутий и изолиран ръкав добавете ln 2 до сухото издънка на банката на Сейнт Луис Корд, за да запази продукта замръзнал, докато не се направи напълно задоволително определяне.
- Подготовка
- Координация с клиничния екип
- Потвърдете времето за инфузия предварително коригиране на началния час за размразяване, така че устройството да е на разположение за инфузия, когато получателят е готов.
- Консултирайте се с клиницистите относно обема на крайния продукт въз основа на теглото на получателя и възможните ограничения на течностите.
- Обща информация
- Използвайте асептична техника в кабинет за биологична безопасност за всички етапи на обработка, включително цялата обработка на OpenContainer и всички разпръскване на контейнерни портове.
- Използвайте само стерилни материали при обработка на клетъчния продукт.
- Запишете номера на информацията за производителя и датата на изтичане (ако е приложимо) на всички реагенти и еднократна употреба.
- Пригответе водната баня и проверете дали температурата е 37 ° C.
- Подгответе разтвора за възстановяване
- Комбинирайте 250 ml Dextran 40 и 50 ml 25% албумин в 300 ml трансферен пакет. Закрепете тръбата с хемостат.
- Използване на подходящи спринцовки Изтеглете следното и ограничете спринцовките с тъпа пластмасова канюла:
- 50 ml разтвор за възстановяване. Ако общият замразен обем (обем на продукта DMSO) надвишава стандартния разтвор за възстановяване на 50 ml, използвайте обем на разтвор за възстановяване, равен на общия замразен обем, така че съотношението на разреждане е най -малко 1: 1
- 30 ml разтвор за възстановяване, който да се използва като контейнерно изплакване за микробно култивиране
- Получете продукт
- Пригответе преносим канистър с LN 2 Използване на подходящо лично защитно оборудване (ръкавици за рокли за ръкавици).
- Проверката на продукта изисква двама членове на лабораторния персонал. С изложбите и получателите на ръка намерете и премахнете продукта от мястото му във фризера, но поддържайки във фазата на парата. Експедитивно проверете точността на етикетирането на идентичността на продукта на информацията и целостта на контейнера.
- Извадете всеки сегмент, прикрепен към мястото на единицата, в 2 ml криовиал и съхранявайте или в пара или течна фаза на азот ( <-150°C).
- Незабавно прехвърлете продукта от LN 2 Резервоар за съхранение в преносимата кутия, съдържаща LN 2 .
- Координация с клиничния екип
- Процедура
Препоръчва се реконструкция или просто разреждане на алокорд с декстран/човешки серумен албумин (HSA), използвайки процедурите за размразяване и разреждане, описани по -долу. Алтернативната процедура - промиването може да се вземе предвид, ако обемът на инфузия и/или DMSO дозата са противопоказани (> 1 ml/kg).
Забележка: Минимизирайте времето от започване на размразяване до завършване на инфузия.
Каква е дозата за Алев
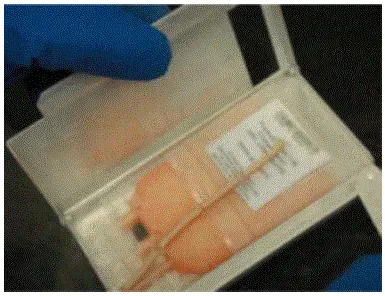
Размразяване:
- Проверете самоличността на размразяването на продукта.
- Извадете алокордната единица от касетата. Разгледайте криобага за почивки или пукнатини.
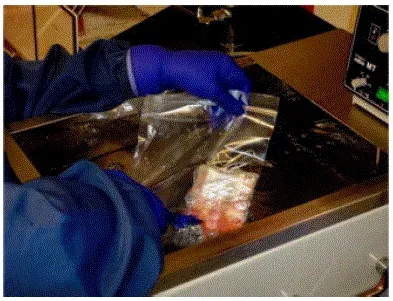
- Внимателно поставете устройството вътре в стерилна запечатана торбичка с цип и потопете във водната баня с 37 ° C, поддържаща пристанището (ите) суха и над водата.
- Документирайте началния час на размразяване.
- За да ускорите размразяването на нежно омесване на съдържанието на чантата.
Забележка: Inspect for leaks ! Ако се наблюдава целостта на контейнера, че е компрометирана позиция, криобагът и/или скобата с хемостати, за да се предотврати по -нататъшното бягство на кръвта. - Когато съдържанието на Cryobag стане киша, извадете торбата от водната баня с 37 ° C.
- Забележка the thaw stop time. Product expiration time is four hours from this step.
- Нежно избършете външната повърхност на криобага с алкохол и поставете криобага в биологичния шкаф за безопасност.
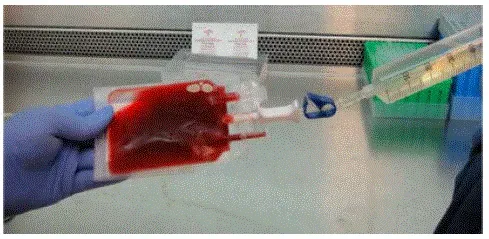
Разрешаване: - Поставете плазмен трансфер, зададен в криобага.
- Прикрепете спринцовката, съдържаща разтвора за възстановяване на 50 ml към трансферния набор на криобага.
- Бавно въведете приблизително половината от обема на разтвора за възстановяване на размразения продукт, докато смесвате течностите в торбата.
- Поставете скока на правилно обозначен пакет за прехвърляне на капацитет на подходящ обем във втория порт за достъп на Cryobag.
- Претеглете празния пакет за трансфер, за да определите теглото на чантата.
- Изцедете съдържанието от Cryobag в трансферния пакет.
- Закрепете тръбата между торбичките с хемостат.
- Добавете останалия разтвор за възстановяване към криобага.
- Смесете добре, за да изплакнете клетките от торбата и да се отцедете в трансферния пакет.
- Закрепете тръбата между торбичките.
- Претеглете трансферния пакет, изваждайки теглото на тара, за да получите обема на продукта.
- Поставете трансфер, зададен в пакета за прехвърляне на продукти.
- Асептично прикрепете 3 ml спринцовка и аспирирайте 1 ml аликвота за тестване за контрол на качеството.
- Доставете 1ML тестването на аликвота в етикетирана аликвотна тръба.
- Извадете 1ML (тестване на аликвота) от обема на продукта, за да определите обема на инфуза. Запишете обем на инфузия които ще се използват за изчисляване на номера на клетките.
- Загрейте уплътняването на тръбата между криобага и трансферния пакет.
- Нарежете тръбите на уплътненията и отделете торбичките.
Забележка: В този момент това е приблизително 30 минути от инфузия. Уведомете екипа за клинична трансплантация да лекарства пациента, както е поръчано. - Асептично въведете 30 ml разтвор за възстановяване от спринцовката, приготвена в стъпка 3.C.II.2) в (сега празен) оригинален продукт Cryobag.
- Незабавно транспортирайте продукта до мястото на клиничната трансплантация на SOP на съоръжението.




Алтернативна процедура - измиване:
Извършете стъпки a. през r. на процедурата за размразяване и процедурата за разреждане, както е посочено по -горе, след това попълнете следното:
- Поставете трансферния пакет в стерилна торбичка за презареждане, готова за центрофугиране.
- ПОДДЪРЖАНЕ НА ПЪРВО В ПОСТАВКА НА ЦЕНТРОФУГАТА, за да се предотврати образуването на гънки по време на центрофугиране.
- Балансирайте носителите и центрофугата при 650 x g (1500 об / мин) за 20 минути при 10 ° C (без спирачка).
- Внимателно отстранете трансферния пакет от центрофугата в биологичния шкаф за безопасност, поставяйки трансферния пакет в плазмен експресиращ.
- Използвайки оригиналния Cryobag за събиране на обема на отпадъците, експресирайте 75% от обема на разтвора за възстановяване, първоначално добавен към размразения продукт преди центрофугиране. Избягвайте случайно преминаване на клетки със супернатантата.
- Оставете клетките да почиват в продължение на пет минути. Ресуспендирайте утаената клетъчна пелета чрез нежна възбуда.
- Получавайте проби за контрол на качеството, както е описано на стъпки s. през АА. по -горе.

- Контрол на качеството:
Извършете анализи за контрол на качеството на политики и процедури за трансплантация на центрове, като използвате аликвота на размразения продукт, получен в стъпка U по -горе. Препоръчителните анализи включват:
- Брой на нуклеирани клетки
- Тест за жизнеспособност
- Жизнеспособен брой CD34 клетки
- Единица за формиране на колония
- Микробни култури (аеробни анаеробни и гъбични)
Изчисления:
Инфузия TNC [x10 9 ] = (Wbc / ml nrbc / ml [x10 6 ]) x инфузия 9 6 обем (ml)
TNC обхват [x10 7 /kg] = Инфузия TNC [x10 9 ]
Получател WT (kg)Пост-размразяване на TNC възстановяване [%] = TNC на размразен продукт [x10 9 ]
TNC на оригинален замразен продукт [x10 9 ]x 100 Общо CD34 клетки [x10 6 ] = CD34 клетки/ml x коефициент на разреждане x 1000 ml x обем на продукта (ml)
CD34 клетъчна доза [x10 5 /kg] = Absolute CD34+ cell cells (x10 6 ) ÷ тегло на получателя (kg)
Product RBC обем [ML] = Product Hematocrit x Обем на продукта (ML)
RBC доза [ml/kg] = продукт RBC обем [ml] ÷ тегло на получателя (kg)
Брой на CFU на продукта [x10 5 ] = Колониите вкараха на 10 5 NC X продукт TNC [x10 9 ]
10 5Доза CFU [x10 4 /kg] = Брой на CFU на продукта [x10 5 ] ÷ получател на тегло (kg)
- Информация за контакт
SSM Cardinal Glennon Детски медицински център
Банката на Сейнт Луис Корд (SLCBB)
3662 Park Avenue
Сейнт Луис МО 63110SLCBB часове:
SLCBB телефонен номер:
SLCBB факс номер:
След часове числа:
Режисьор:
Дистрибуция:










