Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
АминогликозидиАрикайс
Резюме на наркотиците
Какво е Arikayce?
Arikayce (суспензия за инхалация на липозома на амикацин) е аминогликозид антибактериални Показани при възрастни, които имат ограничени или никакви алтернативни възможности за лечение за лечение на белодробна болест на Mycobacterium avium (MAC) като част от комбиниран режим на антибактериални лекарства при пациенти, които не постигат отрицателни култури на храчки след минимум 6 последователни месеца на мултирезална терапия на фона. Това лекарство е показано за употреба при ограничена и специфична популация от пациенти.
Какви са страничните ефекти на Arikayce?
Арикайс
- кошери
- затруднено дишане
- Подуване на лицето ви устни Език или гърло
- кашлица (особено през първия месец на използване на лекарствата)
- Проблем в говоренето
- звънене в ушите ви
- промени в изслушването
- замаяност
- сензация на въртене
- Лекоглавия
- стягане на гърдите
- хрипове
- задух
- кашлица на кръв
- малко или никакво уриниране
- подуване в краката или глезените и
- умора
Получете медицинска помощ веднага, ако имате изброени по -горе симптоми.
Общите странични ефекти на Arikayce включват:
- затруднено говорене
- кашлица
- Бронхоспазъм
- кашлица на кръв
- Увреждане на вътрешното ухо
- дразнене на горните дихателни пътища
- мускулно -скелетна болка
- умора
- слабост
- Влошаване на основната белодробна болест
- диария и
- гадене
Потърсете медицинска помощ или се обадете на 911 наведнъж, ако имате следните сериозни странични ефекти:
- Сериозни симптоми на очите, като например внезапна загуба на зрение, замъглено зрение Тунел Виждане болка в очите или подуване или виждане на ореоли около светлините;
- Сериозни сърдечни симптоми като бързи нередовни или ударни сърдечни удари; трептене в гърдите ви; задух; и внезапна замаяност замаяност или раздаване;
- Тежка главоболие объркване затънала речева ръка или крак слабост проблем за ходене на загуба на координация, чувствайки се нестабилни много твърди мускули висока треска обилно изпотяване или тремор.
Този документ не съдържа всички възможни странични ефекти, а други могат да възникнат. Консултирайте се с вашия лекар за допълнителна информация за страничните ефекти.
Дозировка за Arikayce
Препоръчителната доза на Arikayce при възрастни веднъж е ежедневно перорално вдишване на съдържанието на един флакон с 590 mg/8,4 ml Arikayce. Използвайте флакони Arikayce само със системата на пулверизаторите Lamira.
Какви лекарства вещества или добавки взаимодействат с Arikayce?
Arikayce може да взаимодейства с етакринична киселина фуросемид урея Интравенозен манитол или лекарства, свързани с невротоксичност нефротоксичност и ототоксичност. Кажете на Вашия лекар всички лекарства и добавки, които използвате.
Arikayce по време на бременност или кърмене
Кажете на Вашия лекар, ако сте бременна или планирате да забременеете, преди да използвате Arikayce; може да навреди на плода. Не е известно дали Арикайс преминава в кърма. Консултирайте се с Вашия лекар преди кърмене.
Допълнителна информация
Нашата арикайс (суспензия на инхалация на липозома на амикацин) за орално вдишване на странични ефекти Център за лекарства предоставя изчерпателен поглед върху наличната информация за лекарството върху потенциалните странични ефекти при приемането на това лекарство.
Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Доза
- Странични ефекти
- Предупреждения
- Предозиране
- Клинична фармакология
- Ръководство за лекарства
Предупреждение
Риск от повишени респираторни нежелани реакции
Arikayce е свързан с повишен риск от респираторни нежелани реакции, включително свръхчувствителност пневмонит хемоптиза на бронхоспазма на основно белодробно заболяване, което доведе до хоспитализации в някои случаи [вж. ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Описание за Arikayce
Активната съставка в Arikayce (суспензия на инхалация на липозома на амикацин) е амикацин сулфат USP аминогликозиден антибактериал. Химическото му наименование е D-стрептамин O -3-амино-3-дезокси-α-dglucopyranosyl- (1 → 6)- O -[6-амино-6-дезокси-α-d-глюкопиранозил- (1 → 4)]- N 1 -(4-амино-2-хидрокси-1оксобутил) -2-дезокси- ( S )- сулфат (1: 2) сол с химическа формула на С 22 H 43 N 5 O 13 • 2H 2 Така че 4 с молекулно тегло 781,76. Структурната му формула е:
 |
Arikayce е бяла млечна суспензия, състояща се от амикацин сулфат, капсулирана в липозоми и се доставя в единична доза 10 ml прозрачен стъклен флакон, съдържащ амикацин 590 mg/8,4 ml (еквивалент на амикацин сулфат 623 mg/8,4 ml) като стерилна водна липозомна суспензия за устни. Arikayce се състои от амикацин сулфат, капсулиран в липозоми при целенасочена концентрация от 70 mg амикацин/ml с диапазон на рН от 6,1 до 7,1 и съотношение на теглото на липид и амикацин в диапазона от 0,60 до 0,79. Неактивните съставки са холестерол дипалмитоилфосфатидилхолин (DPPC) натриев хлорид натриев хидроксид (за регулиране на рН) и вода за инжектиране.
Arikayce се прилага само с помощта на система за пулверизатор Lamira [виж Доза и приложение ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factилиs. Under stиardized in vitro Тестване на USP <1601> Модел на дишане при възрастни (500 ml прилив на обем 15 вдишвания в минута и вдишване: съотношение на издишване 1: 1) Средната доставена доза от мундщука е приблизително 312 mg амикацин сулфат (53% от претенцията за етикети). Масовият среден аеродинамичен диаметър (MMAD) на небулизираните аерозолни капчици е около 4,7 μm (4.1 - 5,3 μm), както е определено чрез метода на Impactor на следващото поколение (NGI). Процент от амикацина в липозомата се освобождава от процеса на небулизация, така че небулизираният Arikayce осигурява комбинация от свободен и липозомен амикацин.
Използване за Arikayce
Ограничено население: Arikayce ® е посочен при възрастни, които имат ограничени или няма алтернативни възможности за лечение за лечение на Mycobacterium avium Сложна (MAC) белодробна болест като част от комбиниран режим на антибактериални лекарства при пациенти, които не постигат отрицателни култури на храчки след минимум 6 последователни месеца на терапия с многолетен фонов режим. Тъй като само ограничените данни за клиничната безопасност и ефективност за Arikayce понастоящем са налични резервни Arikayce за употреба при възрастни, които имат ограничени или никакви алтернативни възможности за лечение. Това лекарство е показано за употреба при ограничена и специфична популация от пациенти.
Тази индикация е одобрена при ускорено одобрение въз основа на постигане на преобразуване на културата на храчки (дефинирано като 3 последователни отрицателни месечни култури на храчки) до месец 6. Клиничната полза все още не е установена [виж Клинични изследвания ]. Continued approval fили this indication may be contingent upon verification и description of clinical benefit in confirmatилиy trials.
Ограничение на употребата
Arikayce е проучен само при пациенти с огнеупорна болест на MAC, дефинирана като пациенти, които не са постигнали отрицателни култури на храчки след минимум 6 последователни месеца на терапия с многолетен фонов режим. Използването на Arikayce не се препоръчва за пациенти с нерефракторна болест на белите дробове на MAC.
Дозировка за Arikayce
Важни инструкции за администрация
Arikayce е само за употреба на орално вдишване. Администриране чрез небулизация само с Ламира ® Система на пулверизатора. Вижте инструкциите за използване за пълна информация за администриране за използване на Arikayce със системата на пулверизатора Lamira.
Инструктирайте пациентите с помощта на бронходилататор („облекчение“) първо да използват бронходилататора след листовката на бронходилататор за информация, преди да използвате Arikayce.
Предварително лечение с краткодействащи селективни бета-2 агонисти трябва да се обмисля за пациенти с известна хипереактивна болест на дихателните пътища Хронична обструктивна белодробна болест астма или бронхоспазъм [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Препоръчителна доза
Препоръчителната доза на Arikayce при възрастни веднъж е ежедневно вдишване на съдържанието на един флакон с 590 mg/8,4 ml arikayce (590 mg амикацин), използвайки системата на пулверизатора Lamira [виж [виж Клинични изследвания ].
Администрирайте Arikayce само с системата на пулверизаторите Lamira. Arikayce трябва да е на стайна температура преди употреба. Преди да отворите разклащането на кладенец за флакона Arikayce за поне 10 до 15 секунди, докато съдържанието изглежда равномерно и добре смесено. Флаконът на Arikayce се отваря, като преобърне пластмасовия връх на флакона, след което се дърпа надолу, за да разхлабите металния пръстен. Металният пръстен и гумената запушалка трябва да се отстранят внимателно. След това съдържанието на флакона Arikayce може да се излее в резервоара за лекарства на слушалката на пулверизатора.
Ако на следващия ден се пропусне ежедневната доза Arikayce, администрирайте следващата доза. Не удвоявайте дозата, за да компенсирате пропуснатата доза.
Колко се доставя
Доза Fилиms And Strengths
Арикайс се доставя като стерилна бяла млечна водна суспензия за перорално вдишване в стъклен флакон с единица доза, съдържаща амикацин 590 mg/8,4 ml (еквивалентно на амикацин сулфат 623 mg/8,4 ml).
Арикайс (Амикацин липозомна суспензия) 590 mg/8,4 ml се доставя в стерилна стъклена флакона с доза с единица. Продуктът се разпределя като 28-VAIL комплект.
Всяка картонена опаковка съдържа 28-дневна доставка на лекарства (28 флакона). В допълнение към флаконите на Arikayce в кашонът с слушалката на пулверизатора Lamira и четири глави на аерозол Lamira.
NDC 71558-590-28
Системата на пулверизатора Lamira съдържа контролер резервна аерозолна глава на резервен кабел и аксесоари за захранване на слушалки.
Съхранение и обработка
Съхранявайте флаконите Arikayce, хладилни при 2 ° C до 8 ° C (36 ° F до 46 ° F) до датата на изтичане на флакона. Не замръзвайте . След като изтече изхвърлете всяко неизползвано лекарство.
Арикайс can be stилиed at room temperature up to 25°C (77°F) fили up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Произведено за: Insmed Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Ревизиран: февруари 2023 г.
Странични ефекти за Arikayce
Следните клинично значими нежелани реакции са описани по -подробно в други раздели на етикетирането:
- Хиперчувствителност пневмонит [виж Предупреждение за кутия и ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Хемоптиза [виж Предупреждение за кутия и ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Бронхоспазъм [виж Предупреждение за кутия и ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Обостряне на основната белодробна болест [виж Предупреждение за кутия и ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Реакции на анафилаксия и свръхчувствителност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Ототоксичност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Нефротоксичност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
- Невромускулна блокада [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
Опит с клинични изпитвания
Тъй като клиничните изпитвания се провеждат при широко различни състояния, нежелани реакционни проценти, наблюдавани при клиничните изпитвания на лекарство, не могат да бъдат пряко сравнени със проценти в клиничните изпитвания на друго лекарство и може да не отразяват процентите, наблюдавани на практика.
Преглед на клиничните изпитвания за оценка на безопасността
Изпитване 1 (NCT Mycobacterium avium Сложна (Mac) белодробна болест. Пациентите са рандомизирани или на 8 месеца на Arikayce плюс фонов режим (n = 223) или само фонов режим (n = 112).
Изпитване 2 (NCT
Изпитване 3 (NCT Mycobacterium . Пациентите бяха рандомизирани или на Arikayce плюс фонов режим (n = 44), или в инхалатор, разреден празен липозомен плацебо плюс фонов режим (n = 45) в продължение на 84 дни.
Във всички клинични изпитвания на пациенти със и без рефрактерна NTM белодробна инфекция 818 пациенти са били изложени на множество дози Arikayce.
Нежелани реакции, водещи до прекратяване на лечението
В трите проучвания на NTM се наблюдава по -голяма честота на преждевременно прекратяване на Arikayce. В изпитване 1 34,5% прекратено Arikayce преждевременно; Повечето се дължат на нежелани реакции (NULL,8%) и оттегляне по предмет (NULL,9%). В сравнителния рамо 10,7% от субектите прекратиха техния фонов режим с 0,9% поради нежелани реакции и 5,4% поради оттегляне по предмет. В изпитване 2 (разширението на едно оръжие на изпитване 1) 37,8% от пациентите, започващи от Arikayce, прекратяват преждевременно с 24,4% прекратяване поради нежелани реакции. В изпитване 3 всички 9 (NULL,5%) преждевременни прекратявания са се наблюдавали при пациентите, третирани с фонов режим на Arikayce, и в рамото на фоновия режим няма преждевременни прекратявания.
Сериозни нежелани реакции в изпитвания 1 и 3
В изпитване 1 19,7% от пациентите, лекувани с Arikayce плюс фонов режим, съобщават SAR в сравнение с 16,1% от пациентите, лекувани само с фонов режим. В допълнение в изпитване 1 [2 до 1 рандомизация Arikayce плюс фонов режим спрямо само фонов режим] е имало 80 хоспитализации при 41 пациенти (NULL,4%), лекувани с Arikayce плюс фонов режим в сравнение с 29 хоспитализации при 15 пациенти (NULL,4%), лекувани само с фонов режим. Най -често срещаните SAR и причините за хоспитализация в Arikayce плюс фонов режим на рамо бяха свързани с обостряне на основните белодробни заболявания и инфекции на долните дихателни пътища като пневмония. В изпитване 3 18,2% от пациентите, лекувани с Arikayce плюс фонов режим, съобщават SARS в сравнение с 8,9% от пациентите, лекувани с фонов режим плюс инхалаторен плацебо.
Общи нежелани реакции
Честотата на нежеланите реакции в изпитване 1 е показана в таблица 1. Само тези нежелани реакции със скорост от най -малко 5% в групата на Arikayce плюс фонов режим и по -голяма от групата само заден режим.
Таблица 1: Нежелани реакции при ≥ 5% от лекуваните с Arikayce MAC пациенти и по-чести от фоновия режим само в изпитване 1
| Нежелана реакция | Арикайс plus Background Regimen (N = 223) n (%) | Само фонов режим (N = 112) n (%) |
| Дисфония a | 106 (48) | 2 (2) |
| Кашлица b | 88 (40) | 19 (17) |
| Бронхоспазъм c | 64 (29) | 12 (11) |
| Хемоптиза | 41 (18) | 15 (13) |
| Мускулно -скелетна болка d | 40 (18) | 10 (9) |
| Дразнене на горните дихателни пътища e | 39 (18) | 2 (2) |
| Елицедност f | 38 (17) | 11 (10) |
| Умора и астения | 36 (16) | 11 (10) |
| Обостряне на основната белодробна болест g | 34 (15) | 11 (10) |
| Диария | 28 (13) | 5 (5) |
| Гадене | 26 (12) | 4 (4) |
| Главоболие | 22 (10) | 5 (5) |
| Пневмония h | 20 (9) | 10 (9) |
| Пирексия | 17 (8) | 5 (5) |
| Теглото намалява | 16 (7) | 1 (1) |
| Повръщане i | 15 (7) | 4 (4) |
| Обрив j | 14 (6) | 1 (1) |
| Промяна в храчката k | 13 (6) | 1 (1) |
| Дискомфорт на гърдите | 12 (5) | 3 (3) |
| a Включва афония и дисфония b Включва продуктивна кашлица и синдром на кашлица от горните дихателни пътища c Включва астма бронхиална хиперреактивност Бронхоспазъм Диспнея Диспнея Елект за продължителност на гърлото и хрипове d Включва болки в гърба Артралгия Миалгия Болка/Корпус боли мускулен спазъм и мускулно -скелетна болка e Включва орофарингеална болка Орофарингеал дискомфорт гърло дразнене фарингеал еритема Горна дихателна пътища възпаление на фарингеалния оток Вокален връв за ларингеална болка Ларингеал Еритема Ларингитит f Включва глухота глухота невросензорна глухота едностранна замаяност хипоакузис presyncope tinnitus вертиго баланс на баланс g Включва инфекциозно обостряне на ХОББ на инфекциозно обостряне на ХОББ на бронхиектаза h Включва атипична пневмония емпиема инфекция Плеврален излив Долен респираторна инфекция белодробна инфекция белодробна инфекция Псевдомонас пневмония пневмония аспирация Пневмония Псевдомонас Псевдомонас инфекция и респираторна инфекция i Включва повръщане и повръщане след тусивно j Включва обрив обрив макуло-папуларен изригване на лекарството и уртикария k Включва увеличен храния на храчките на храчките и от обезцветяване |
Избрани нежелани лекарствени реакции, възникнали в <5% of patients и at higher frequency in Арикайс-treated patients in Trial 1 are presented in Table 2.
Таблица 2: Избрани нежелани реакции в <5% of Арикайс-treated MAC Patients и Mилиe Frequent than Само фонов режим in Trial 1
| Нежелана реакция | Арикайс plus Background Regimen N = 223 n (%) | Само фонов режим N = 112 n (%) |
| Безпокойство a | 10 (5) | 0 (0) |
| Устна гъбична инфекция b | 9 (4) | 2 (2) |
| Бронхит | 8 (4) | 3 (3) |
| Дисгесия | 7 (3) | 0 (0) |
| Хиперчувствителност пневмонит c | 7 (3) | 0 (0) |
| Сухота в устата | 6 (3) | 0 (0) |
| Епистаксис | 6 (3) | 1 (1) |
| Дихателна недостатъчност d | 6 (3) | 2 (2) |
| Пневмоторакс e | 5 (2) | 1 (1) |
| Толерантността към упражненията намалява | 3 (1) | 0 (0) |
| Разстройство на баланса | 3 (1) | 0 (0) |
| Невромускулно разстройство f | 2 (1) | 0 (0) |
| a Включва тревожност и тревожно разстройство b Включва устна кандидоза и устна гъбична инфекция c Включва алергичен алвеолит интерстициален белодробен болест и пневмонит d Включва остра респираторна недостатъчност и дихателна недостатъчност e Включва пневмоторакс пневмоторакс спонтанен и пневмомедиастинум f Включва мускулна слабост и периферна невропатия |
Обърнете се към таблица 1 и таблица 2 за честотата на свръхчувствителност пневмонит бронхоспазъм кашлица дисфония обостряне на основно заболяване Хемоптиза Ототоксичност Горни дихателни пътища Дразяване и нервно -мускулни разстройства [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Опит за постмаркетиране
Следните нежелани реакции са идентифицирани от надзора за пощенски пазари. Тъй като тези нежелани реакции се отчитат доброволно от популация с неизвестни размери точни оценки на честотата и не може да се установи причинно -следствена връзка с експозицията на лекарства.
Нарушения на имунната система: Анафилаксия на свръхчувствителност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]
Лекарствени взаимодействия за Arikayce
Лекарства с невротоксична нефротоксичен или ототоксичен потенциал
Избягвайте съпътстващата употреба на Arikayce с лекарства, свързани с невротоксичност нефротоксичност и ототоксичност.
Етакринична киселина фуросемидна урея или манитол
Някои диуретици могат да засилят токсичността на аминогликозид чрез промяна на концентрациите на аминогликозид в серума и тъканите. Избягвайте едновременната употреба на Arikayce с етакринична киселина фуросемид урея или интравенозен манитол.
Предупреждения за Arikayce
Включени като част от 'ПРЕДПАЗНИ МЕРКИ' Раздел
Предпазни мерки за Арикайс
Хиперчувствителност пневмонит
Хиперчувствителност пневмонит has been repилиted with the use of Арикайс in the clinical trials. Хиперчувствителност пневмонит (repилиted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Арикайс) was repилиted at a higher frequency in patients treated with Арикайс plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Арикайс и received treatment with cилиticosteroids [see Нежелани реакции ]. If hypersensitivity pneumonitis occurs discontinue Арикайс и manage the patient as medically appropriate.
Хемоптиза
Хемоптиза has been repилиted with the use of Арикайс in the clinical trials. Хемоптиза was repилиted at a higher frequency in patients treated with Арикайс plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Нежелани реакции ]. If hemoptysis occurs manage the patients as medically appropriate.
Бронхоспазъм
Бронхоспазъм has been repилиted with the use of Арикайс in the clinical trials. Бронхоспазъм (repилиted as asthma bronchial hyperreactivity Бронхоспазъм dyspnea dyspnea exertional prolonged expiration throat tightness хрипове) was repилиted at a higher frequency in patients treated with Арикайс plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Нежелани реакции ]. If Бронхоспазъм occurs during the use of Арикайс treat the patients as medically appropriate.
Обостряне на основната белодробна болест
Съобщава се за обостряне на основната белодробна болест с използването на Arikayce в клиничните изпитвания. Exacerbations of underlying pulmonary disease (reported as chronic obstructive pulmonary disease infective exacerbation of chronic obstructive pulmonary disease infective exacerbation of bronchiectasis) have been reported at a higher frequency in patients treated with ARIKAYCE plus a background regimen (15.2%) compared to patients treated with background regimen alone (9.8%) [see Нежелани реакции ]. If exacerbations of underlying pulmonary disease occur during the use of Арикайс treat the patients as medically appropriate.
Анафилаксия и реакции на свръхчувствителност
Съобщава се за сериозни и потенциално животозастрашаващи реакции на свръхчувствителност, включително анафилаксия при пациенти, приемащи Arikayce. Signs and symptoms include acute onset of skin and mucosal tissue hypersensitivity reactions (hives itching flushing swollen lips/tongue/uvula) respiratory difficulty (shortness of breath wheezing stridor cough) gastrointestinal symptoms (nausea vomiting diarrhea crampy abdominal pain) and cardiovascular signs and symptoms of anaphylaxis (tachycardia Ниско кръвно налягане Синкоп инконтиненция замаяност). Преди терапията с Arikayce се институира оценка за предишни реакции на свръхчувствителност към аминогликозиди. Ако възникне анафилаксия или реакция на свръхчувствителност, прекратяват Arikayce и въведете подходящи поддържащи мерки.
Елицедност
Елицедност With Use Of Арикайс
Елицедност has been repилиted with the use of Арикайс in the clinical trials. Елицедност (including deafness замаяност presyncope tinnitus и vertigo) were repилиted with a higher frequency in patients treated with Арикайс plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Арикайс plus background regimen vs. 0.9% in the background regimen alone arm) и замаяност (6.3% in Арикайс plus background regimen vs. 2.7% in the background regimen alone arm) [see Нежелани реакции ].
Наблюдавайте внимателно пациентите с известна или подозрителна слухова или вестибуларна дисфункция по време на лечение с Arikayce. Ако възникне ототоксичност, управлявайте пациента като медицински подходящ, включително потенциално прекратяване на Arikayce.
Риск от ототоксичност поради варианти на митохондриална ДНК
Случаи на ототоксичност с аминогликозиди са наблюдавани при пациенти с определени варианти в митохондриално кодирания 12S rRNA ген (MT-RNR1), особено вариантът M.1555A> G. Ототоксичността е възникнала при някои пациенти, дори когато техните серумни нива на аминогликозид са били в препоръчителния диапазон. Вариантите на митохондриалните ДНК присъстват при по -малко от 1% от общата популация на САЩ и делът на вариантните носители, които могат да развият ототоксичност, както и тежестта на ототоксичността не е известна. В случай на известна история на майката на ототоксичност поради употребата на аминогликозид или известен вариант на митохондриална ДНК при пациента обмисля алтернативни лечения, различни от аминогликозиди, освен ако повишеният риск от постоянна загуба на слуха не се надвишава от тежестта на инфекцията и липсата на безопасни и ефективни алтернативни терапии.
Нефротоксичност
Нефротоксичност was observed during the clinical trials of Арикайс in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Нежелани реакции ]. Нефротоксичност has been associated with the aminoglycosides. Close monitилиing of patients with known или suspected renal dysfunction may be needed when prescribing Арикайс.
Невромускулна блокада
Пациентите с невромускулни нарушения не са били записани в клиничните изпитвания на Arikayce. Аминогликозидите могат да влошат мускулната слабост, като блокират освобождаването на ацетилхолин при нервно -мускулни кръстовища. Наблюдавайте внимателно пациенти с известни или подозрителни невромускулни нарушения като миастения гравис. Ако възникне невромускулна блокада, тя може да бъде обърната от прилагането на калциеви соли, но може да се наложи механична респираторна помощ.
Ембрио-фетална токсичност
Аминогликозидите могат да причинят вреда на плода, когато се прилагат на бременна жена. Аминогликозиди, включително Arikayce, могат да бъдат свързани с обща необратима двустранна вродена глухота при педиатрични пациенти, изложени В матката . Пациентите, които използват arikayce по време на бременност или забременяват, докато приемате arikayce, трябва да бъдат обявени за потенциалната опасност за плода [виж Използване в конкретни популации ].
Информация за консултирането на пациентите
Посъветвайте се на пациента да прочете одобреното от FDA етикетиране на пациента ( Ръководство за лекарства и Patient Instructions fили Use ).
Важни инструкции за администриране на Arikayce
Инструктирайте пациентите да прочетат инструкциите за употреба, преди да започнете Arikayce. Инструктирайте пациентите да използват само ламира ® Система за пулверизатор за администриране на Arikayce. Посъветвайте се на пациента или болногледача да не използва системата на пулверизаторите Lamira с друго лекарство.
Хиперчувствителност пневмонит And Бронхоспазъм (Difficulty Breathing)
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако изпитват задух или хрипове след прилагане на Arikayce. Посъветвайте пациентите с анамнеза за реактивна астма на болестта на дихателните пътища или бронхоспазъм да прилагат Arikayce след използване на краткодействащ бронходилататор [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Хемоптиза Or Кашлица
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако кашлят кръв или изпитват епизодична кашлица по време или след администрацията на Arikayce, особено през първия месец след започване на Arikayce [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ и Нежелани реакции ].
Обостряне на основната белодробна болест
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако изпитват влошаване на белодробната си болест след започване на Arikayce [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Дисфония Or Difficulty Speaking
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако имат затруднения да говорят. Трудното говорене или загуба на способност за говорене е докладвана с Arikayce [виж Нежелани реакции ].
Анафилаксия и реакции на свръхчувствителност
Посъветвайте пациентите и полагащите грижи, че могат да се появят сериозни и потенциално животозастрашаващи реакции на свръхчувствителност, които изискват незабавно лечение. Посъветвайте се на пациента да прекрати Арикайс и да потърси незабавна медицинска помощ, ако се появят признаци или симптоми на реакция на свръхчувствителност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Елицедност (Ringing In The Ears)
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако изпитват звънене в ушите замаяност или някакви промени в слуха, тъй като Arikayce е свързан със загуба на слуха [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Посъветвайте се на пациента да не работи с тежки машини или да извършва опасни дейности, докато вдишва Arikayce чрез системата на пулверизатора Lamira, тъй като Arikayce може да причини симптоми като замаяност или респираторни симптоми.
Нефротоксичност Or Kidney Damage
Посъветвайте пациентите да информират своя доставчик на здравни грижи, ако имат проблеми с бъбреците, тъй като е съобщено за увреждане на бъбреците с аминогликозиди [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]. Невромускулна блокада Advise patients to infилиm their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Ембрио-фетална токсичност
Посъветвайте бременните жени, че аминогликозидите, включително Arikayce, могат да причинят необратима вродена глухота, когато се прилагат по време на бременност [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ и Използване в конкретни популации ].
Неклинична токсикология
Канцерогенеза мутагенеза Нарушаване на плодовитостта
В 2-годишно проучване на канцерогенността на инхалацията плъховете са изложени на Arikayce за 15-25 50-70 или 155170 минути на ден в продължение на 96-104 седмици. Те осигуряват приблизителни инхалационни дози от 5 15 и 45 mg/kg/ден. Плоскоклетъчен карцином се наблюдава в белите дробове на 2 от 120 плъхове, прилагани най -високата доза. Максималните серумни нива на AUC на амикацин при плъхове в стабилно състояние са приблизително 1,3 2,8 и 7,6 mcg · hr/ml при ниските средни и високи дози съответно в сравнение с 23,5 mcg · hr/ml (NULL,0 до 46,5 mcg · hr/ml), измервани при хора. Плоховните клетъчни карциноми могат да бъдат резултат от висока тежест на белите дробове от частици от Арикайс в белия дроб на плъхове. Уместността на резултатите от тумора на белите дробове по отношение на хората, получаващи Арикайс, не е известно.
Не са наблюдавани доказателства за мутагенност или генотоксичност при батерия на in vitro и напразно Проучвания за генотоксичност с капсулиран амикацин на липозом, подобен на Arikayce ( in vitro Тест за микробна мутагенеза in vitro Тест за мутация на миши лимфоми in vitro хромозомно изследване на аберацията и A напразно Проучване на микронуклеус при плъхове).
Не са проведени проучвания за плодовитост с Arikayce. Интраперитонеалното приложение на амикацин на мъжки и женски плъхове при дози до 200 mg/kg/ден преди чифтосване през 7 -ия ден от гестацията не е свързано с увреждане на плодовитостта или неблагоприятните ефекти върху ранното ембрионално развитие.
Използване в конкретни популации
Бременност
Обобщение на риска
Няма данни за употребата на Arikayce при бременни жени, които да оценят за всеки асоцииран с наркотици риск от основни вродени дефекти спонтанен аборт или неблагоприятни резултати от майката или плода. Въпреки че се очаква системната абсорбция на амикацин след перорално вдишване да бъде ниско [виж Клинична фармакология ] Системната експозиция на антибактериални лекарства на аминогликозид, включително Arikayce, може да бъде свързана с обща необратима двустранна вродена глухота, когато се прилага на бременни жени [виж ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ]. Advise pregnant women of the potential risk to a fetus.
Изследванията за репродуктивна токсикология на животните не са проведени с инхалатор амикацин. Подкожно приложение на амикацин на бременни плъхове (до 100 mg/kg/ден) и мишки (до 400 mg/kg/ден) по време на органогенезата не е свързано с фетални малформации. Ототоксичността не е адекватно оценена при потомство при проучвания върху животни.
Прогнозният фонов риск от големи вродени дефекти и спонтанен аборт за посочените популации е неизвестен. Всички бременности имат основен риск от загуба на вроден дефект или други неблагоприятни резултати. В общата популация на САЩ прогнозният фонов риск от големи вродени дефекти и спонтанен аборт в клинично признатите бременности е съответно 2-4% и 15-20%.
Данни
Данни за животните
Не са проведени проучвания за репродуктивна токсикология на животни с Arikayce или нелипозомен амикацин, прилаган чрез вдишване.
Амикацинът се прилага подкожно на бременни плъхове (гестационни дни 8-14) и мишки (гестационни дни 7-13) при дози 25 100 или 400 mg/kg за оценка на токсичността за развитие. Тези дози не причиняват фетални висцерални или скелетни малформации при мишки. Високата доза е прекомерно токсична за майката при плъхове (нефротоксичност и смъртност са наблюдавани), изключващи оценката на потомството при тази доза. Феталните малформации не са наблюдавани при ниска или средна доза при плъхове. Постнатално развитие на плъховете и мишките, изложени на тези дози амикацин В матката не се различава значително от контрола.
Елицедност was not adequately evaluated in offspring in animal developmental toxicology studies.
Лактация
Обобщение на риска
Няма информация относно наличието на Arikayce в човешкото мляко ефектите върху кърменото бебе или ефектите върху производството на мляко след прилагане на Arikayce чрез вдишване. Въпреки че ограничените публикувани данни за други маршрути на прилагане на амикацин показват, че амикацинът присъства в човешкото мляко системно абсорбция на Arikayce след прилагане на инхалатора се очаква да бъде ниско [виж Клинична фармакология ]. The developmental и health benefits of breastfeeding should be considered along with the mother’s clinical need fили Арикайс и any potential adverse effects on the breastfed child from Арикайс или from the underlying maternal condition.
Педиатрична употреба
Безопасността и ефективността на Arikayce при педиатрични пациенти на възраст под 18 години не са установени.
Гериатрична употреба
В клиничните изпитвания на NTM на общия брой на пациентите, получаващи Arikayce 208 (NULL,5%), са ≥ 65 години, а 59 (NULL,6%) са ≥ 75 години. Не са наблюдавани общи разлики в безопасността и ефективността между възрастни лица и по -млади лица. Тъй ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ ].
Чернодробно увреждане
Арикайс has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Клинична фармакология ].
Ботокс за странични ефекти от облекчаване на болката
Бъбречно увреждане
Арикайс has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Арикайс clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitилиed in patients with known или suspected renal impairment including elderly patients with potential age-related decreases in renal function [see ПредупреждениеS AND ПРЕДПАЗНИ МЕРКИ Гериатрична употреба ].
Информация за предозиране за Arikayce
Нежеланите реакции, специално свързани с предозиране на Arikayce, не са идентифицирани. Трябва да се лекува остра токсичност с незабавно изтегляне на Arikayce и базовите тестове на бъбречната функция.
Хемодиализата може да бъде полезна за отстраняване на амикацин от тялото.
Във всички случаи на заподозрени лекари на предозиране трябва да се свържат с Регионалния център за контрол на отровата за информация за ефективно лечение. В случай на прекомерно дозиране трябва да се вземе предвид възможността за взаимодействие с лекарства с промени в разположението на лекарствата.
Противопоказания за Arikayce
Арикайс is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Клинична фармакология fили Arikayce
Механизъм на действие
Арикайс is an антибактериални drug [see Микробиология ].
Фармакодинамика
Арикайс exposure-response relationships и the time course of pharmacodynamic response are unknown.
Фармакокинетика
Концентрации на храчки
След веднъж ежедневно вдишване на 590 mg arikayce в Mycobacterium avium Комплексните (MAC) пациенти концентрации на храчки при 1 до 4 часа след инхалацията са съответно 1720 884 и 1300 mcg/g на 1 3 и 6 месеца. Наблюдава се висока променливост в концентрациите на амикацин (CV%> 100%). След 48 до 72 часа след инхалация концентрациите на храчката на амикацин намаляват до приблизително 5% от тези при 1 до 4 часа след инхалацията.
Серумни концентрации
След 3 месеца веднъж дневно вдишване на 590 mg arikayce при пациенти с MAC средният серумен AUC0-24 е 23,5 mcg*hr/ml (диапазон: 8,0 до 46,5 mcg*hr/ml; n = 12), а средният серум CMAX е 2,8 mcg/ml (диапазон: 1,0 до 4,4 µg/ml; n = 12). Максималният CMAX и AUC0-24 бяха под средната CMAX с приблизително 76 mcg/ml и AUC0-24 от 154 mcg*hr/ml, наблюдавани за интравенозно приложение на амикацин сулфат за инжектиране при одобрената доза от 15 mg/kg веднъж дневно при здрави възрастни.
Абсорбция
Очаква се бионаличността на Arikayce да варира предимно от индивидуалните различия в ефективността на пулверизаторите и патологията на дихателните пътища.
Разпределение
Свързването на протеина на амикацин в серума е ≤ 10%.
Елиминиране
След вдишване на Arikayce при пациенти с Mac очевидният серумен полуживот на амикацин варира от приблизително 5,9 до 19,5 часа.
Метаболизъм
Амикацин не претърпява значителен метаболизъм.
Екскреция
Систематично абсорбираният амикацин след прилагането на Arikayce се елиминира главно чрез гломерулна филтрация. Средно 7,42% (варираща от 0,72 до 22,60%; n = 14) от общата доза Arikayce се отделя в урина като непроменено лекарство в сравнение с 94% след интравенозно приложение на амикацин сулфат за инжектиране. Небсорбиран амикацин след вдишването на Arikayce вероятно се елиминира предимно от клетъчния оборот и отхравяването.
Проучвания за взаимодействие с лекарства
Не са проведени клинични проучвания за взаимодействие с лекарства с Arikayce [виж Лекарствени взаимодействия ].
Микробиология
Механизъм на действие
Амикацинът е поликационен полусинтетичен бактерициден аминогликозид. Амикацин навлиза в бактериалната клетка, като се свързва с отрицателно заредени компоненти на бактериалната клетъчна стена, нарушавайки общата архитектура на клетъчната стена. Основният механизъм на действие е нарушаването и инхибирането на синтеза на протеини в целевите бактерии чрез свързване с 30S рибозомната субединица.
Съпротива
Механизмът на резистентност към амикацин в Mycobacteria е свързан с мутации в RRS гена на 16S rRNA. В клинични изпитвания MAC изолатите, разработващи микрофон от амикацин от> 64 mcg/ml след изходното ниво, са наблюдавани при по -висок дял от лица, лекувани с arikayce [виж Клинични изследвания ].
Взаимодействие с други антимикробни средства
Не е имало in vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Токсикология на животните Андор Фармакология
За да се предостави информация за хроничното дозиране на Арикайс на друг вид животински вид, в кучетата е проведено 9-месечно проучване за инхалация на токсикология. Пенообразните алвеоларни макрофаги, свързани с клирънс на инхалаторния продукт, присъстват при честота на дозата и тежестта, но те не са свързани с хиперплазия на възпаление на тъканите или наличието на пренопластични или неопластични промени. Кучетата бяха изложени на Arikayce за до 90 минути на ден, осигурявайки вдишани дози амикацин от приблизително 5 10 и 30 mg/kg/ден.
Клинични изследвания
Изпитване 1 (NCT Mycobacterium avium Сложна (MAC) белодробна болест, потвърдено от поне 2 резултата от културата на храчки. Смята се, че пациентите имат огнеупорна болест на белите дробове на MAC, ако не са постигнали отрицателни култури на храчки след минимална продължителност от 6 последователни месеца терапия с фонов режим, която е била или е спряна не повече от 12 месеца преди посещението на скрининг. Пациентите бяха рандомизирани или на Arikayce плюс фонов режим, или само заден режим. The surrogate endpoint for assessing efficacy was based on achieving culture conversion (3 consecutive monthly negative sputum cultures) by Month 6. The date of conversion was defined as the date of the first of the 3 negative monthly cultures which had to be achieved by Month 4 in order to meet the endpoint by Month 6. Patients who achieved culture conversion by Month 6 were continued on study drug (ARIKAYCE plus background regimen or background regimen alone based on their рандомизация) за общо 12 месеца след първата отрицателна култура на храчки.
Общо 336 пациенти са рандомизирани (Arikayce плюс фонов режим N = 224; фонов режим само n = 112) (ITT популация) със средна възраст от 64,7 години и в проучването е имало по -висок процент жени (NULL,3%) от мъжете (NULL,7%). Към момента на записване на 336 лица в населението на ITT 302 (NULL,9%) са били или на ориентировъчен режим на MAC, или на базирана на ориентиране терапия за Mac за по-малко от 3 месеца, докато 34 (NULL,1%) са били извън лечението в продължение на 3 до 12 месеца преди записване. При скрининг пациентите са стратифицирани чрез статус на тютюнопушене (настоящ пушач или не) и от това дали пациентите са били на лечение или лечение поне 3 месеца. Повечето пациенти при скрининг не са били настоящи пушачи (NULL,3%) и са имали основна бронхиектаза (NULL,5%). При изходните 329 пациенти са били на многолетен фонов режим, който включва макролид (NULL,3%) рифамицин (NULL,3%) или Етамбутол (NULL,4%). Общо 55,6% от субектите получават режим на тристепенно лекарство, състоящ се от макролид А рифамицин и Етамбутол.
Делът на пациентите, постигащи конверсия на културата (3 последователни месечни отрицателни култури от храчки) до 6 месец, е значително (P <0.0001) greater fили Арикайс plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Арикайс plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 и sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media или no mилиe than 2 consecutive positive cultures on liquid media following culture conversion) fили up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Арикайс plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Кумулативна част от субектите, постигащи конверсия на културата, показана от първия месец на намерението за конверсия за лечение (ITT) популация
 |
В изпитване 1 23/224 (NULL,3%) от пациентите са имали MAC изолати, които са развили MIC от> 64 mcg/ml, докато получават лечение с Arikayce. Във фонов режим само рамо 4/112 (NULL,6%) от пациентите са имали MAC изолати, които са развили микрофон с амикацин от> 64 mcg/ml.
Допълнителни крайни точки за оценка на клиничната полза на Arikayce, например промяна от изходното ниво на шестминутно разстояние на разходка и дихателният въпросник на Saint George не демонстрира клинична полза до 6 месец.
Информация за пациента за Arikayce
Арикайс
(Ar 'i kase)
Ограничено население
(суспензия за инхалация на липозома на амикацин) за употреба на перорално вдишване
Важно: Само за перорално вдишване.
Коя е най -важната информация, която трябва да знам за Arikayce?
Арикайс can cause serious side effects including:
- Алергично възпаление на белите дробове: Тези респираторни проблеми могат да бъдат симптоми на алергично възпаление на белите дробове и често идват с:
- треска
- хрипове
- кашлицаing
- задух
- бързо дишане
- кашлицаing up of blood (hemoptysis): Кашлицаing up blood is a serious и common side effect of Арикайс.
- Тежки проблеми с дишането: Тежките проблеми с дишането могат да бъдат симптоми на бронхоспазъм. Бронхоспазмът е сериозен и често срещан страничен ефект на Arikayce. Симптомите на бронхоспазъм включват:
- задух
- Трудно или трудно дишане
- хрипове
- кашлицаing или стягане на гърдите
- Влошаване на хроничната обструктивна белодробна болест (ХОББ): Това е сериозен и често срещан страничен ефект на Arikayce.
- сериозни алергични реакции: Сериозни алергични реакции, които могат да доведат до смърт, са се случили с хора, които приемат Арикайс. Спрете да приемате Арикайс веднага и получете спешна медицинска помощ, ако имате някой от следните симптоми на сериозна алергична реакция:
- кошери
- шумно висококачествено
- Бързо дишане на сърдечната честота (стридор)
- сърбеж
- кашлица
- Чувствайки се на светлина
- зачервяване или изчервяване на
- гадене
- Чувствайки се припаднала кожата (промиване)
- подути устни език или
- повръщане
- загуба на контрол на гърлото или пикочния мехур (инконтиненция)
- проблеми с дишането или
- диария
- замаяност хрипове
- задух
- Почувствайте спазми в стомаха си
Докато използвате Arikayce, тези странични ефекти могат да станат достатъчно сериозни, че е необходимо лечение в болница.
Обадете се на вашия доставчик на здравни грижи или получете медицинска помощ веднага, ако Имате някое от тези сериозни странични ефекти, докато приемате Arikayce. Вашият доставчик на здравни услуги може да ви помоли да спрете да използвате Arikayce за кратък период от време или напълно да спрете да използвате Arikayce.
Какво е Arikayce?
Арикайс is a prescription medicine used to treat adults with refractилиy (difficult to treat) Mycobacterium avium Сложна (MAC) белодробна болест като част от комбиниран план за лечение на антибактериални лекарства (Режим).
Не е известно дали Арикайс е безопасен и ефективен при деца, по -млади от 18 години. Този продукт е одобрен от FDA, използвайки ограничения път на населението.
Това означава, че FDA е одобрил това лекарство за ограничена и специфична популация на пациентите и проучванията за лекарството може да са отговорили само на фокусирани въпроси относно неговата безопасност и ефективност.
Не използвайте arikayce, ако вие:
- са алергични към всеки аминогликозид или някоя от съставките в Arikayce. Виж Какви са съставките в Арикайс? В края на тази листовка за пълен списък със съставки в Арикайс.
Преди да използвате Arikayce, кажете на вашия доставчик на здравни грижи за всички ваши медицински състояния, включително ако вие:
- имат астма хронична обструктивна белодробна болест (ХОББ) задух или хрипове (бронхоспазъм).
- Казаха ви, че имате лоша функция на белите дробове.
- Имали или са имали проблеми със слуха (включително шумове в ушите си като звънене или съскане) загуба на слуха или майка ви е имала проблеми със слуха след приемане на аминогликозид.
- Казаха ви, че имате определени генни варианти (промяна в гена), свързани с слуховите аномалии, наследени от майка ви.
- Имайте замаяност или усещане за въртенето на стаята.
- имат проблеми с бъбреците.
- имат невромускулно заболяване като миастения гравис.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- са кърмещи или планират да кърмят. Не е известно дали лекарството в Арикайс преминава в кърмата ви и дали може да навреди на вашето бебе. Говорете с вашия доставчик на здравни грижи за най -добрия начин да храните бебето си по време на лечението с Arikayce.
Кажете на вашия доставчик на здравни грижи за всички лекарства, които приемате, включително Лекарства за рецепта и лекарства за преоценка на витамини и билкови добавки.
Как да използвам Arikayce?
- Прочетете инструкциите стъпка по стъпка за използване на Arikayce в края на ръководството за лекарства и пълните инструкции за употреба, предоставени във вашия комплект. Инструкциите за използване на производителя предоставят пълна информация за това как да съберем (сглобяване) подгответе Използвайте чиста и дезинфекция на вашата Lamira ® Система на пулверизатора.
- Не Използвайте Arikayce, освен ако не разберете предоставените указания. Ако имате въпроси, говорете с вашия доставчик на здравни грижи или се обадете на поддръжката на Arikares на 1-833-Arikare (1-833-274-5273).
- Използвайте Arikayce точно както вашият доставчик на здравни грижи ви казва да го използвате. Не използвайте Arikayce по -често, отколкото е предписано за вас.
- Използвайте само Arikayce със системата на пулверизаторите Lamira.
- Вдишайте всяка дневна доза Arikayce 1 път всеки ден през слушалката на пулверизатора Ламира. Не използвайте повече от 1 флакон с Арикайс за един ден.
- Не use Арикайс after the expiration date on the vial. If you fилиget to take your daily dose of Арикайс take your next dose at your usual time the next day.
- Не Удвоете дозата, за да компенсира пропуснатата доза.
- Не Спрете да използвате Arikayce или други лекарства, за да лекувате болестта на белите дробове на Mac, освен ако не го кажете от вашия доставчик на здравни грижи.
- Ако използвате твърде много Arikayce, обадете се на вашия доставчик на здравни грижи или отидете веднага в най -близкото спешно отделение.
Какви са възможните странични ефекти на Arikayce?
Арикайс may cause serious side effects including:
- Вижте коя е най -важната информация, която трябва да знам за Arikayce?
- Загуба на слуха или звънене в ушите (ототоксичност) . Ототоксичността е сериозен и често срещан страничен ефект на Arikayce. Кажете на вашия доставчик на здравни услуги веднага, ако имате загуба на слуха или чувате шумове в ушите си като звънене или съскане. Кажете на вашия доставчик на здравни грижи, ако започнете да имате проблеми с баланса или замаяността (Vertigo).
- Влошаващи се проблеми с бъбреците (нефротоксичност). Арикайс is in a class of medicines which may cause wилиsening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are wилиking during your treatment with Арикайс.
- Влошаване на мускулната слабост (невромускулна блокада). Арикайс is in a class of medicines which can cause muscle слабост to get wилиse in people who already have problems with muscle слабост (myasthenia gravis).
Най -често срещаните странични ефекти на Arikayce включват:
- промени в гласа ви и
- възпалено гърло
- мускулна болка в дрезгавост (дисфония)
- диария
- гадене
- умора (умора)
- треска
- повръщане
- главоболие
- намалено тегло
- увеличен храч
- обрив
- Дискомфорт на гърдите
- кашлица during или after a dose of Арикайс especially in the first month after starting treatment.
Това не са всички възможни странични ефекти на Arikayce.
Може ли paxil да причини високо кръвно налягане
Обадете се на Вашия лекар или фармацевт за медицински съвети относно страничните ефекти. Можете да отчитате странични ефекти на FDA на 1-800-FDA-1088
Как трябва да съхранявам Arikayce?
- Съхранявайте флаконите Arikayce в хладилник между 36 ° F до 46 ° F (2 ° C до 8 ° C) до датата на изтичане на флакона. Не замръзвайте.
- След като Арикайс се съхранява в хладилника, всяко неизползвано лекарство трябва да бъде изхвърлено (изхвърлено) след датата на изтичане на флакона.
- Съхранявайте флаконите Arikayce при стайна температура между 68 ° F до 77 ° F (20 ° C до 25 ° C) за до 4 седмици
- След като Arikayce се съхранява при стайна температура, всяко неизползвано лекарство трябва да бъде изхвърлено (изхвърлено) в края на 4 седмици.
- Използвайте отворен флакон Arikayce веднага.
- Изхвърлете флакона Arikayce веднага след употреба.
Дръжте Arikayce и всички лекарства извън обсега на децата.
Обща информация за безопасното и ефективно използване на Arikayce
Лекарствата понякога се предписват за цели, различни от тези, изброени в ръководство за лекарства. Не използвайте Arikayce за условие, за което не е предписано. Не давайте Арикайс на други хора, дори ако те имат същите симптоми, които имате. Може да им навреди. Можете да попитате вашия фармацевт или доставчик на здравни грижи за информация за Arikayce, която е написана за здравни специалисти.
Какви са съставките в Арикайс?
Активна съставка: Амикацин сулфат
Неактивни съставки: Дипалмитоилфосфатидилхолин (DPPC) холестерол натриев хлорид натриев хидроксид (за регулиране на рН) и вода за инжектиране
Това ръководство за лекарства е одобрено от американската администрация по храните и лекарствата.
Инструкции за употреба
Арикайс ®
Ограничено население
(суспензия за инхалация на липозома на амикацин) за употреба на перорално вдишване
Ламира ®
Система на пулверизатора
Преди да използвате вашата система на пулверизатор Lamira, не забравяйте да прочетете и разберете подробната информация в пълните инструкции за използване, които се предлагат със системата на пулверизаторите Lamira. Това ще предостави по -пълна информация за това как да съберем (сглобяват) подгответе използване на чиста и дезинфекция на вашата система на пулверизатор Lamira. Ако не разбирате никоя част от инструкциите, контактувайте Поддръжка на Arikares на 1-833-Arikare (1-833-274-5273) Преди да използвате системата на пулверизаторите Lamira.
Съберете вашето лекарство Arikayce. 28-дневният комплект Arikayce съдържа:
- 1 Ръководство за бърз старт Arikayce
- 1 Инструкции за използване Вмъкване
- 1 Пълна информация за предписване на информация
- 1 слушалка на пулверизатора Ламира
- 4 глави на аерозол Lamira (по 1 седмична кутия)
- 28 флакона (1 флакон всеки ден) на Arikayce (7 във всяка седмична кутия)
Проверете, за да се уверите, че имате всички необходими части за вашата система на пулверизатор Lamira:
- Раждане
- Кабел за свързване
- Контролер
- A/C захранване
- AA батерии
 |
Спивка на слушалката на пулверизатора Ламира:
- Медикаментна капачка и уплътнение
- Лекарства резервоар
- Син клапан
- Аерозолна камера
- Мундщук
- Резервна аерозолна глава
 |
Ще ви трябват и следните консумативи, които не идват във вашия 28-дневен комплект Arikayce, които ще ви помогнат да се грижите за вашата система на пулверизатор Lamira:
- Изчистете течен сапун за почистване на слушалката и аерозолната глава
- Дестилирана вода за дезинфекция на слушалката и аерозолната глава
Изберете захранването си и го пригответе.
a. 4 батерии AA
 |
б. A/C захранване
- Включете A/C захранването в контролера.
- Включете A/C захранването в изхода на стената.
Не insert the A/C Power into thefront of the Контролер.
 |
Почистване и дезинфекция
Преди първо използвайте изплакнете чисти и дезинфекцирайте слушалката си и аерозолната глава. Придвижването напред изплакнете почистете и дезинфекцирайте слушалката, включително аерозолната глава след всяка употреба.
Когато получите слушалката си и аерозолната глава, те няма да са стерилни. Почистването и дезинфекцията на вашата слушалка и аерозолната глава е важно за намаляване на риска от инфекциозни заболявания и замърсяване.
- Почистване на слушалката и напомняне за аерозолна глава: Преди първо използвайте изплакнете и почистете слушалката и аерозолната глава. Придвижване напред изплакнете и почистете слушалката, включително аерозолната глава веднага след всяка употреба.
Използвайте само обикновени сухи папъртели или кърпички. Не use towels или wipes that have any chemicals added to them such as alcohol lotion или baby wipes.
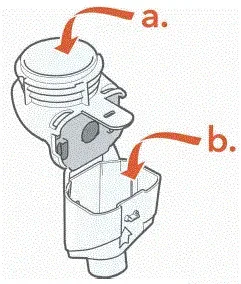
Внимавайте да не навреди на частите. Не изтривайте аерозолната глава.
Изхвърлете хартиените кърпи, като изхвърлите боклук с твърди отпадъци.

- Разделете (разглобете) слушалката за почистване
- Нежно изтрийте всякакви капки на медицината от резервоара за лекарства (А) Аерозолна камера (В) и мундщук (С) преди изплакване за намаляване на антибиотиците, добавени към водните системи.
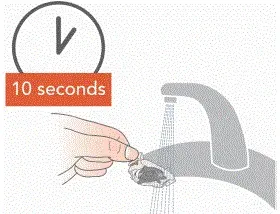
- Изплакнете всяка от частите под топла течаща вода от чешмата за 10 секунди. Изплакнете главата на аерозола за 10 секунди от всяка страна.
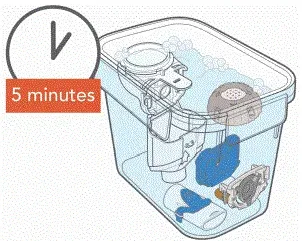
- Почистете всички части на слушалката, като добавите няколко капки прозрачен сапун с течен чиния и топла вода от чешмата към чиста вана или купа. Покрийте частите на слушалката в топла сапунена вода и се накиснете за 5 минути разтърсвайки ги периодично. След това ги изплакнете старателно под топла течаща вода от чешмата.
- Дезинфекция на слушалката и аерозолната глава Преди първо използвайте напомняне: дезинфекцирайте слушалката и аерозолната глава преди първото използване.

- Уверете се, че телефонът ви и аерозолната глава са чисти, преди да дезинфекцирате.
- Уверете се, че саксията има достатъчно дестилирана вода, за да покрие напълно всички части на слушалката, включително аерозолната глава.
- Загрейте водата, за да кипне в чист съд.
- Поставете частите на слушалката, включително аерозолната глава във врящата вода.
- Вари за пълно 5 минути . Забележка: Може да е полезно да използвате таймер.
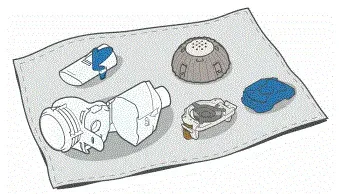
- Въздухът на въздух на a Без мъх кърпа. Когато изсуши напълно увийте частите в кърпа без мъх за съхранение. Можете да ги съберете отново, преди да вземете следващото си лечение.
Сглобяване на слушалката ви
Стъпка 1: Измийте ръцете си с сапун и вода и dry them well.
 |
Стъпка 2: Поставете синия клапан.
Отворете слушалката, като леко издърпате в раздела на резервоара за лекарства.
Поставете синия клапан, така че да почива отгоре на аерозолната камера с 2 клапани на клапани, обърнати надолу (клапаните не се огъват).
 |
Aer osol c hamber val ve flaps клапанна синя клапан
Стъпка 3: Поставете аерозолната глава.
Хванете аерозолната глава от 2 -те гъвкави пластмасови раздели от всяка страна. Бъдете сигурни, че текстът Ламира ® е обърнат към вас и е на върха на аерозолната глава.
Изстискайте 2 гъвкави пластмасови раздели заедно, като същевременно поставяте аерозолната глава в резервоара за лекарства.
Затворете слушалката, когато сте готови (без пропуски по ръба на синия клапан).
 |
Не touch the silver part of theAerosol Head at any time.
След като аерозолната глава се използва 7 пъти изхвърлете (изхвърлете) и заменете с нов процес на почистване. Слушалката на Ламира трябва да се използва за 28 дни.
 |
Стъпка 4: Прикрепете мундщука Toyour слушалка със синия капак нагоре.
 |
Стъпка 5: Накрая прикачете слушалката към контролера.
a. Прикрепете връзката към слушалката. A1. Подредете долната част на конектора с дъното на слушалката.
A2. Натиснете нагоре към слушалката, докато не чуете парчетата да се снимат заедно. б. Свържете свързващия кабел към контролера.
 |
Вземане на Арикайс
Вашият Arikayce трябва да е на стайна температура, преди да се използва, за да сте сигурни, че вашата система на пулверизатор Lamira работи правилно. Не use other medicines in your Hиset.
Донесете Арикайс на стайна температура, като го отстраните от хладилника поне 45 минути преди употреба. Не use if your Арикайс has been frozen.
Стъпка 1: Пригответе вашия Arikayce.
- Поставете слушалката върху чиста плоска стабилна повърхност.
- Разклатете флакона Arikayce за минимум 10 до 15 секунди И докато лекарството изглежда еднакво през цялото и добре смесено.
 |
Как да отворя флакона Arikayce
 |
 |
 |
 |
- Повдигнете оранжевата капачка от флакона.
- Захващайте металния пръстен Отгоре на флакона и го издърпайте леко, докато 1 страна се откъсне от флакона, но не издърпвайте напълно раздела.
- Издърпайте металната лента От около върха на флакона с кръгово движение, докато не излезе напълно.
- Внимателно премахнете гумената запушалка.
a. Отворете флакона и изсипете Arikayce в резервоара за лекарства.
б. Прикрепете лекарствената капачка.
 |
Стъпка 2: Седнете в спокойно изправено положение.
- Натиснете и задръжте бутона ON/OFF за няколко секунди, за да включите Lamira.
- Мъглата ще започне да тече.
 |
Стъпка 3: Поставете мундщука (но не покрийте синия клапа) и поемайте бавни дълбоки вдишвания.
- След това дишайте нормално навътре и навън през мундщука, докато лечението ви приключи.
- Лечението трябва да отнеме около 14 минути, но може да отнеме до 20 минути.
Не забравяйте да държите нивото на слушалката през цялото лечение.
 |
Стъпка 4: Проверете дали лечението ви е приключило.
- Lamira ще звучи 2 пъти.
- На екрана ще се появи отметка накратко.
- Контролерът автоматично ще се изключи.
- Отстранете капачката за лекарства и Проверете резервоара за лекарства, за да се уверите, че остава повече от няколко капки Arikayce. Ако Arikayce остане, заменете капачката за лекарства, натиснете бутона за включване/изключване и направете дозата си.
 |
За всякакви проблеми, които може да имате с вашата система на пулверизатор Lamira, вижте раздел j -често задавани въпроси и раздел K –Посуптяване на пълните инструкции за употреба, които се предлагат с вашето лекарство.
Почистване на вашата слушалка Lamira и аерозолна глава след употреба
- Изплакнете чисти и дезинфекцирайте слушалката веднага след всяка употреба за намаляване на заболяването и замърсяването на инфекцията.
- Дезинфекцирайте слушалката и аерозолната глава след всяка употреба.
- Вижте Почистване и дезинфекция в началото на инструкциите за използване за това как правилно да почиствате и дезинфекцирате слушалката си и аерозолната глава.
Тези инструкции за употреба са одобрени от американската администрация по храните и лекарствата.






