Информацията В Сайта Не Е Медицински Съвет. Ние Не Продаваме Нищо. Точността На Превода Не Е Гарантирана. Отказ От Отговорност
Декарбоксилазни инхибиториСталево
Резюме на наркотиците
Какво е Stalevo?
Stalevo (Carbidopa Levodopa и Entacapone) е комбинация от няколко лекарства, използвани за лечение на симптоми на Parkinson, като например мускулна скованост трепереща спазми и лоша мускулна контрола. Леводопа се преобразува в химикал, наречен допамин в мозъка. Симптоми на Болест на Паркинсон може да бъде причинен от допамин с ниски нива в мозъка. Карбидопа помага да се предотврати разпадането на Леводопа, преди да може да достигне до мозъка и да влезе в сила. Когато се използва с Carbidopa и Levodopa entacapone, увеличава нивата на леводопа в организма.
Какви са страничните ефекти на Сталево?
Сталево
- кошери
- затруднено дишане
- Подуване на лицето ви устни Език или гърло
- Нов или влошаващ се мускулен спазъм
- значително засилено мигане или потрепване
- припадък
- диария
- Визията се променя
- замъглено зрение
- Болки в очите
- силна коремна болка
- Черни или тари столове
- повръщане, което прилича на кафене
- Мускулна болка нежност или слабост
- промяна в количеството урина
- промени в настроението
- объркване
- халюцинации
- Мисли за самоубийство
- постоянен възпалено гърло
- Лесно кървене или синини
- необичайна умора
- изтръпване на ръцете или краката
- Необичайни силни пориви (увеличени сексуални подтици за хазарт)
- Болки в гърдите
- треска
- необичайна мускулна скованост
- Тежка объркване
- изпотяване
- бърз или нередовен сърдечен ритъм
- бързо дишане и
- Тежка замаяност
Получете медицинска помощ веднага, ако имате изброени по -горе симптоми.
Общите странични ефекти на Stalevo включват:
- диария
- гадене
- повръщане
- главоболие
- замаяност
- сънливост
- замъглено зрение
- Болки в стомаха или разстройство
- загуба на апетит
- запек
- сухота в устата
- Промени в чувството ви за вкус
- кожен обрив или сърбеж
- необичайни промени в кожата
- мускулни крампи
- Болки в гърба
- агитация
- безпокойство
- затруднено сън (безсъние) или
- странно Сънища .
Кажете на Вашия лекар, ако имате сериозни странични ефекти на Stalevo, включително:
- неволно Движения (особено потрепване на клепача)
- припадък or falling
- затруднено преглъщане
- Болки в стомаха/корема
- постоянен диария
- Визията се променя (including замъглено зрение)
- Черни/тари за тари
- мускулна болка
- Промени в количеството на урината
- Психични/промени в настроението (като объркване на халюцинации мисли за самоубийство)
- признаци на инфекция (например постоянно възпалено гърло) или
- необичайни силни пориви (като увеличен хазарт повишени сексуални подтици).
Потърсете медицинска помощ или се обадете на 911 наведнъж, ако имате следните сериозни странични ефекти:
- Сериозни симптоми на очите, като например внезапна загуба на зрение, замъглено зрение Тунел Виждане болка в очите или подуване или виждане на ореоли около светлините;
- Сериозни сърдечни симптоми като бързи нередовни или ударни сърдечни удари; трептене в гърдите ви; задух; и внезапно замаяност Лекоглавия или раздаване;
- Тежка главоболие объркване затънала речева ръка или крак слабост проблем за ходене на загуба на координация, чувствайки се нестабилни много твърди мускули висока треска обилно изпотяване или тремор.
Този документ не съдържа всички възможни странични ефекти, а други могат да възникнат. Консултирайте се с вашия лекар за допълнителна информация за страничните ефекти.
Дозировка за Сталево
Оптималната дневна доза на Сталево трябва да бъде определена за всеки пациент. Терапията трябва да бъде индивидуализирана и коригирана според желания терапевтичен отговор.
Какви лекарства вещества или добавки взаимодействат със Stalevo?
Сталево може да взаимодейства с апоморфин холестирамин Добутамин епинефрин Изониазиден изопротеренол Метилдопа Метоклопрамид папаверн фенитоин пробенецид антибиотици лекарства за кръвно налягане Антидепресанти лекарства за лечение на психиатрични разстройства настинка или алергия Медицина наркотици хапчета за сън мускулни релаксира лекарство за припадъци или лекарства против тревожност. Кажете на Вашия лекар всички лекарства, които приемате.
Сталево по време на бременност и кърмене
Stalevo трябва да се използва само когато е предписано по време на бременност. Леводопа преминава в кърма. Не е известно дали Карбидопа или Ентакапон преминават в кърма. Консултирайте се с Вашия лекар преди кърмене.
Допълнителна информация
Нашият Stalevo (Carbidopa Levodopa и Entacapone) Странични ефекти в центъра за лекарства предоставя цялостен поглед върху наличната информация за лекарството за потенциалните странични ефекти при приемането на това лекарство.Информация за наркотиците на FDA
- Описание на лекарството
- Показания
- Странични ефекти
- Лекарствени взаимодействия
- Предупреждения
- Предозиране
- Клинична фармакология
- Ръководство за лекарства
Описание за Сталево
Сталево е комбинация от Карбидопа Леводопа и Ентакапон за лечение на болестта на Паркинсон.
Карбидопа Инхибиторът на ароматното аминокиселинно декарбоксилиране е бяло кристално съединение, леко разтворимо във вода с молекулно тегло 244,3. Той е обозначен химически като (-)-L- (α-хидразино- (α-метил-β- (34-дихидроксибензен) пропанова киселина монохидрат. Емпиричната му формула е c 10 H 14 N 2 O 4 · H 2 O и структурната му формула е:
 |
Съдържанието на таблети се изразява по отношение на безводна карбидопа, която има молекулно тегло 226,3.
Леводопа Ароматна аминокиселина е бяло кристално съединение, леко разтворимо във вода с молекулно тегло 197.2. Той е обозначен химически като (-)-L-α-амино-β- (34-дихидроксибензен) пропанова киселина. Емпиричната му формула е c 9 H 11 Не 4 И структурната му формула е:
 |
Entacapone COMT инхибиторът е нитро-катахол-структурирано съединение с молекулно тегло 305,3. Химичното наименование на ентакапона е (E) -2-циано-3- (34-дихидрокси-5-нитрофенил) -NN-диетил-2-пропенамид. Емпиричната му формула е c 14 H 15 N 3 O 5 И структурната му формула е:
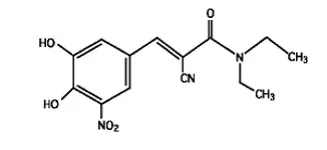 |
Stalevo се доставя като таблетки в 6 силни страни:
Stalevo 50: 12,5 mg Carbidopa 50 mg леводопа и 200 mg ентакапон
Stalevo 75: 18.75 mg Carbidopa 75 mg леводопа и 200 mg ентакапон
Stalevo 100: 25 mg Carbidopa 100 mg леводопа и 200 mg ентакапон
Stalevo125: 31,25 mg carbidopa 125 mg леводопа и 200 mg ентакапон
Stalevo 150: 37,5 mg Carbidopa 150 mg леводопа и 200 mg ентакапон
Stalevo 200: 50 mg carbidopa 200 mg леводопа и 200 mg entacapone
Неактивни съставки: Царевично нишесте Croscarmellose Натриев глицерол 85% хипромелозен магнезиев стеарат манитол полисорбат 80 Повидон захароза червен железен оксид и титанов диоксид. Stalevo 50 Stalevo 100 и Stalevo 150 също съдържат жълто железен оксид.
Използване за Stalevo
Сталево е посочен за лечение на болестта на Паркинсон.
Сталево може да се използва:
- За да замените (с еквивалентни силни страни на всеки от трите компонента) Carbidopa/Levodopa и Entacapone, преди това се прилагат като отделни продукти.
- Да се замени терапията на Карбидопа/Леводопа (без ентакапон), когато пациентите изпитват признаци и симптоми на износване на ендоза и когато са приемали обща дневна доза леводопа от 600 mg или по-малко и не са имали дискинезии.
Дозировка за Сталево
Stalevo трябва да се използва като заместител на пациентите, които вече са стабилизирани на еквивалентни дози на Карбидопа/Леводопа и ентакапон. Някои пациенти, които са стабилизирани в дадена доза Карбидопа/Леводопа, могат да бъдат лекувани със Сталево, ако е взето решение за добавяне на ентакапон (виж отдолу ). Терапията трябва да бъде индивидуализирана и коригирана според желания терапевтичен отговор.
Дозиране на информация
Оптималната дневна доза на Сталево трябва да бъде определена чрез внимателно титруване при всеки пациент.
Клиничният опит с дневни дози над 1600 mg ентакапон е ограничен. Максималната препоръчителна дневна доза Stalevo зависи от използваната здравина. Максималният брой таблетки, които ще се използват за 24-часов период, е по-малък с най-висока якост (Stalevo 200), отколкото с по-ниски якост (виж таблица 1). Проучванията показват, че периферната DOPA декарбоксилаза е наситена от Карбидопа при приблизително 70 mg на ден до 100 mg на ден. Пациентите, получаващи по -малко от това количество Карбидопа, са по -склонни да изпитат гадене и повръщане.
Таблица 1: Максимална препоръчителна доза Сталево за 24-часов период
| Силата на дозата на сталево | Максимален брой таблетки за 24-часов период |
| Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 | 8 |
| Stalevo 200 | 6 |
Преобразуване на пациенти от Карбидопа Леводопа и Ентакапон в Сталево
Понастоящем пациентите, лекувани с ентакапон 200 mg, с всяка доза от таблетка без изключване Carbidopa/Levodopa могат да преминат към съответната сила на Сталево, съдържаща същите количества леводопа и Карбидопа. Например пациенти, получаващи една таблетка от Carbidopa/levodopa 25 mg/100 mg и една таблетка от ентакапон 200 mg при всяко приложение, могат да преминат към единична сталево 100 таблет (съдържаща 25 mg карбидопа 100 mg леводопа и 200 mg ентакапон).
Преобразуване на пациенти от продукти на Карбидопа и Леводопа в Сталево
Няма опит в прехвърлянето на пациенти, които понастоящем се лекуват с формулировки за разширено освобождаване на продуктите на Carbidopa/Levodopa или Carbidopa/Levodopa, които не се комбинират в съотношение 1: 4 на Карбидопа към Леводопа.
Пациентите с анамнеза за умерени или тежки дискинезии или приемане на повече от 600 mg от компонента на леводопа на ден вероятно ще изискват намаляване на дневната им доза леводопа, когато се добави ентакапон. Тъй като регулирането на дозата на отделния компонент на Карбидопа или Леводопа не е възможно с продукти с фиксирана доза, първоначално титрат пациенти до доза, която се толерира и която отговаря на индивидуалната им терапевтична нужда, използвайки отделна таблетка на Карбидопа/Леводопа (съотношение 1: 4) плюс таблетка в ентакапон. След като се установи индивидуалната доза на пациента от дозата на Карбидопа/Леводопа плюс ентакапон, като се използва две отделни таблетки; Превключете пациента в съответния единичен таблет на Stalevo.
Когато се изисква по -малко леводопа намалете общата дневна доза на Карбидопа/Леводопа или чрез намаляване на силата на Сталево при всяко приложение, или чрез намаляване на честотата на приложение чрез удължаване на времето между дозите.
Еднозначна употреба с други лекарства за болестта на Паркинсон
Антихолинергични средства допамин Агонисти моноамино оксидаза (MAO) - В инхибиторите амантадин и други стандартни лекарства за болестта на Паркинсон могат да се използват едновременно, докато Сталево се прилага; Въпреки това могат да се изискват корекции на дозата на съпътстващото лекарство или сталево.
Намаляване или прекъсване на дозирането
Избягвайте прекъсването на дозирането на Stalevo, тъй като е съобщено за хиперпирексия при пациенти, които внезапно преустановят или намалят употребата на леводопа [виж Предупреждения и предпазни мерки ].
Важни инструкции за администрация
Не разделяйте Crush и не дъвчете таблетки Stalevo. Администрирайте само по един таблет при всеки интервал на дозиране. Всички силни страни на Stalevo съдържат 200 mg entacapone. Комбинирането на множество таблетки или части от таблетки за постигане на по -висока доза леводопа може да доведе до предозиране на ентакапон.
Администрирайте Stalevo със или без храна. Въпреки това висококалоричното хранене с високо съдържание на мазнини може да забави усвояването на леводопа с около 2 часа [виж Клинична фармакология ].
Колко се доставя
Дозирани форми и силни страни
Всяка таблетка Stalevo, предоставена в 6 силови страни с една доза, съдържа Карбидопа и леводопа в съотношение 1: 4 и доза от 200 mg ентакапон. Stalevo (Carbidopa Levodopa и Entacapone) се доставя като таблетки, покрити с филми за орално приложение в следващите 6 силни страни:
Сталево 50 Таблетки с покритие, съдържащи 12,5 mg Карбидопа 50 mg леводопа и 200 mg ентакапон. Кръглата двуконвексни таблетки са кафеникаво-или сиво-червени несериозни и релефни LCE 50 от едната страна.
Сталево 75 Таблетки с покритие, съдържащи 18,75 mg Карбидопа 75 mg леводопа и 200 mg ентакапон. Таблетките с овален вид са светлокафяво червено несериозно и релефни с код LCE 75 от едната страна.
Сталево 100 Таблетки с покритие, съдържащи 25 mg Carbidopa 100 mg леводопа и 200 mg ентакапон. Таблетките с овален оформен са кафеникаво-или сиво-червени несериозни и релефни LCE 100 от едната страна.
Сталево 125 Таблетки с покритие, съдържащи 31,25 mg Карбидопа 125 mg леводопа и 200 mg ентакапон. Таблетките с овална форма са светлокафяво червено несериозно и релефни с код LCE 125 от едната страна.
Сталево 150 Таблетки с покритие, съдържащи 37,5 mg Carbidopa 150 mg Levodopa и 200 mg entacapone. Таблетките с оформена форма са кафяво или сиво-червено несериозно и релефно LCE 150 от едната страна.
Stalevo 200 Таблетки с покритие, съдържащи 50 mg Carbidopa 200 mg леводопа и 200 mg ентакапон. Таблетките с овална форма са тъмнокафяво червено несериозно и релефно LCE 200 от едната страна.
Съхранение и обработка
Сталево (Carbidopa levodopa и entacapone) се доставя като таблетки с филмово покритие за орално приложение в следващите шест силни страни:
Сталево 50 film-coated tablets съдържащ 12,5 mg карбидопа 50 mg леводопа и 200 mg ентакапон.
Кръглата двуконвексни таблетки са кафеникаво-или сиво-червени несериозни и релефни LCE 50 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-805-01
Сталево 75 film-coated tablets съдържащ 18,75 mg Carbidopa 75 mg леводопа и 200 mg ентакапон.
Таблетките с овална форма са светлокафяво червено несериозно и релефни с код LCE 75 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-809-01
Сталево 100 film-coated tablets съдържащ 25 mg carbidopa 100 mg леводопа и 200 mg ентакапон.
Таблетките с овална форма са кафеникаво-или сиво-червени несериозни и релефни LCE 100 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-816-01
Сталево 125 film-coated tablets съдържащ 31,25 mg Carbidopa 125 mg леводопа и 200 mg ентакапон.
Таблетките с овална форма са светлокафяво червено несериозно и релефни с код LCE 125 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-827-01
Сталево 150 film-coated tablets съдържащ 37,5 mg Carbidopa 150 mg леводопа и 200 mg ентакапон.
Таблетките с оформена форма са кафяво или сиво-червено несериозно и релефно LCE 150 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-834-01
Stalevo 200 film-coated tablets съдържащ 50 mg Carbidopa 200 mg леводопа и 200 mg ентакапон.
Таблетките с овална форма са тъмнокафяво червено несериозно и релефно LCE 200 от едната страна.
HDPE бутилка от 100 таблетки NDC 52427-842-01
Съхранявайте при 25 ° C (77 ° F); Екскурзии, разрешени до 15 ° C до 30 ° C (59 ° F до 86 ° F).
[Вижте USP контролирана стайна температура .]
Разпределете в тесен контейнер (USP).
Произведена от: Orion Corporation Orion Pharma Orionintie 1 Fi-02200 Espoo Finland. Разпространено от: Almatica Pharma LLC Morristown NJ 07960 USA. Ревизиран: май 2020 г.
Странични ефекти for Сталево
Следните нежелани реакции са разгледани по -подробно в раздели на предупрежденията и предпазните мерки за етикетиране:
- Заспиване по време на ежедневни дейности и сънливост [виж Предупреждения и предпазни мерки ]
- Хипотония /Ортостатична хипотония и синкоп [виж Предупреждения и предпазни мерки ]
- Дискинезия [виж Предупреждения и предпазни мерки ]
- Депресия и самоубийство [виж Предупреждения и предпазни мерки ]
- Халюцинации/психотично поведение [виж Предупреждения и предпазни мерки ]
- Импулсно контрол и/или натрапчиво поведение [виж Предупреждения и предпазни мерки ]
- Изтеглена хиперпирексия и объркване [виж Предупреждения и предпазни мерки ]
- Диария и колит [виж Предупреждения и предпазни мерки ]
- Рабдомиолиза [виж Предупреждения и предпазни мерки ]
- Пептична язва болест [виж Предупреждения и предпазни мерки ]
Опит с клинични изпитвания
Because clinical trials are conducted under widely varying conditions the incidence of adverse reactions (number of unique patients experiencing an adverse reaction associated with treatment/total number of patients treated) observed in the clinical trials of a drug cannot be directly compared to the incidence of adverse reactions in the clinical trials of another drug and may not reflect the incidence of adverse reactions observed in clinical practice.
Entacapone
The most commonly observed adverse reactions (incidence at least 3% greater than placebo incidence) in the double-blind carbidopa-levodopa-placebo-controlled trials of entacapone (N=1003 patients) associated with the use of carbidopalevodopa- entacapone alone and not seen at an equivalent frequency among the placebo-treated patients were: dyskinesia diarrhea nausea hyperkinesia Коремна болка повръща сухота в устата и обезцветяването на урината.
Различията в разликата на лечението за преждевременна прекратяване на изследването за ентакапон с инхибитор на леводопа и DOPA декарбоксилаза в двойно-сляпо плацебо-контролирани изпитвания е 5%. Различията в разликата на лечението за най -честите причини за прекратяване на изследването е 2% за диария и 1% за други специфични нежелани реакции, включително психиатрични причини дискинезия/ хиперкинезия гадене или коремна болка.
Нежелана реакционна честота при контролирани клинични проучвания на ентакапон
В таблица 2 са изброени възникващи нежелани реакции, които са се наблюдавали при поне 1% от пациентите, лекувани с Карбидопа/Леводопа и 200 mg ентакапон, които са участвали в двойно-сляпо плацебо-контролирани проучвания и които са били числено по-често срещани в тази група, отколкото в групата на Карбидопа/Леводопа плюс плацебо група. В тези проучвания или ентакапон или плацебо се добавя към Карбидопа/Леводопа (или бенсеразид/леводопа).
Таблица 2: Обобщение на пациенти с нежелани реакции след началото на прилагането на пробни лекарства най -малко 1% в групата на ентакапоне и по -голямо от плацебо
| Нежелана реакция на системния орган | Карбидопа/Леводопа плюс ентакапон (n = 603) % от пациентите | Карбидопа/Леводопа плюс плацебо (n = 400) % от пациентите |
| Разстройства на кожата и придатъците | ||
| Потенето се увеличи | 2 | 1 |
| Мускулно -скелетни нарушения на системата | ||
| Болки в гърба | 5 | 3 |
| Разстройства на централната и периферната нервна система | ||
| Дискинезия | 25 | 15 |
| Хиперкинезия | 10 | 5 |
| Хипокинезия | 9 | 8 |
| Замаяност | 8 | 6 |
| Специални сетива други нарушения | ||
| Вкуса извращение | 1 | 0 |
| Психиатрични разстройства | ||
| Безпокойство | 2 | 1 |
| Сънливост | 2 | 0 |
| Агитация | 1 | 0 |
| Разстройства на стомашно -чревната система | ||
| Гадене | 14 | 8 |
| Диария | 10 | 4 |
| Коремна болка | 8 | 4 |
| Запек | 6 | 4 |
| Повръщане | 4 | 1 |
| Устата суха | 3 | 0 |
| Диспепсия | 2 | 1 |
| Метеоризъм | 2 | 0 |
| Гастрит | 1 | 0 |
| Стомашно -чревни разстройства № | 1 | 0 |
| Нарушения на дихателната система | ||
| Диспнея | 3 | 1 |
| Тромбоцитно кървене и съсирване Разстройства | ||
| Purpura | 2 | 1 |
| Нарушения на уринарната система | ||
| Обезцветяване на урината | 10 | 0 |
| Тяло като разстройства на целия генерал | ||
| Умора | 6 | 4 |
| Астения | 2 | 1 |
| Разстройства на механизма на съпротивление | ||
| Инфекция бактериал | 1 | 0 |
Опит за постмаркетиране
Следните спонтанни съобщения за нежелани събития, временно свързани с ентакапон или Сталево, са идентифицирани след въвеждането на пазара и не са изброени в таблица 2. Тъй като тези реакции се отчитат доброволно от популация с неизвестен размер, не винаги е възможно да се оцени нататък тяхната честота или да се установи причинно -следствена връзка с ентакапон или излагане на Сталево.
Съобщава се за хепатит с главно холестатични характеристики.
Ефекти на пола и възрастта върху нежеланите реакции
Не са отбелязани разлики в степента на нежелани реакции, които се дължат само на ентакапон по възраст или пол.
Лекарствени взаимодействия for Сталево
MAO инхибитори
Пациентите, получаващи неселективни MAO инхибитори и Carbidopa levodopa и entacapone, могат да бъдат изложени на риск от повишен адренергичен тонус. Следователно използването на Stalevo е противопоказано при пациенти, получаващи неселективни MAO инхибитори [виж Противопоказания ].
Лекарства, метаболизирани от катехол-о-метилтрансфераза (COMT)
Drugs known to be metabolized by COMT such as isoproterenol epinephrine norepinephrine dopamine dobutamine alpha-methyldopa apomorphine isoetherine and bitolterol should be administered with caution in patients receiving entacapone regardless of the route of administration (including inhalation) as their interaction may result in increased heart rates possibly arrhythmias and excessive changes in blood pressure [Вижте Предупреждения и предпазни мерки ].
Антихипертензивни агенти
Симптоматичен постурална хипотония е възникнал, когато Карбидопа/Леводопа е добавен към лечението на пациенти, получаващи антихипертензивни лекарства. При започване на терапия със сталево дозировка може да се наложи антихипертензивно лекарство.
Трициклични антидепресанти
Има съобщения за нежелани реакции, включително хипертония и дискинезия, произтичащи от едновременната употреба на трициклични антидепресанти и Карбидопа/Леводопа.
Допамин D2 рецепторни антагонисти
Допамин D2 рецепторни антагонисти (напр. Метоклопрамид фенотиазини Бутирофенони рисперидон) могат да намалят терапевтичните ефекти на леводопа.
Изониазид
Изониазид may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Phable
Съобщава се, че благоприятните ефекти на леводопа при болестта на Паркинсон са обърнати от фенитоин. Пациентите, приемащи фенитоин с Карбидопа/Леводопа, трябва да бъдат внимателно наблюдавани за загуба на терапевтичен отговор. Дозировката на Stalevo трябва да се увеличи, както е клинично необходимо при пациенти, получаващи фенитоин.
Папаверин
Съобщава се, че благоприятните ефекти на леводопа при болестта на Паркинсон са обърнати от папаверин. Пациентите, приемащи папаверин с Карбидопа/Леводопа, трябва да бъдат внимателно наблюдавани за загуба на терапевтичен отговор. Дозировката на Stalevo трябва да бъде увеличена, както е клинично необходима при пациенти, получаващи папаверин.
Железни соли
Железните соли или мулти витамини, съдържащи железни соли, трябва да бъдат съвместни с повишено внимание. Железните соли могат да образуват хелати с леводопа Карбидопа и ентакапон и следователно да намалят бионаличността на леводопа Карбидопа и ентакапон.
Лекарства, за които се знае, че пречат на жлъчната екскреция глюкуронидация и чревната бета-глюкуронидаза
Тъй като повечето екскреция на ентакапон е чрез дори Трябва да се внимава, когато лекарствата, за които се знае, че пречат на жлъчната екскреция глюкуронидация и чревната бета-глюкуронидаза се прилагат едновременно с ентакапон. Те включват probenecid холестирамин и някои антибиотици (например еритромицин рифампицин ампицилин и хлорамфеникол).
Лекарства, метаболизирани чрез CYP2C9 (например кумадин)
Дозировката на Сталево трябва да бъде коригирана като клинично необходима при пациенти, използващи други лекарства, метаболизирани чрез CYP2C9. Проучване на взаимодействието при здрави доброволци entacapone увеличава AUC на R-Warfarin средно с 18%, а стойностите на INR средно с 13%. Съобщава се за случаи на повишен INR при пациенти при използване на варфарин по време на употребата на ентакапон след одобрение. По този начин се препоръчва мониторинг на INR, когато се започне лечение със сталево за пациенти, получаващи варфарин.
Предупреждения за Сталево
Включени като част от ПРЕДПАЗНИ МЕРКИ раздел.
Предпазни мерки за Сталево
Следните нежелани реакции, описани в този раздел, са свързани с поне един от компонентите на Сталево (т.е. Леводопа Карбидопа и/или ентакапон) въз основа на опита на безопасността в клиничните изпитвания (особено на основните изпитвания) или в докладите за постпарминг.
Заспиване по време на ежедневни дейности и сънливост
Пациентите с болестта на Паркинсон, лекувани със сталево или други продукти на Карбидопа/Леводопа, съобщават, че внезапно заспиват без предварително предупреждение за сънливост, докато са участвали в ежедневни дейности (включително работата на моторните превозни средства). Някои от тези епизоди доведоха до злополуки. Въпреки че много от тези пациенти съобщават за сънливост, докато приемат ентакапон, някои не възприемат предупредителни знаци като прекомерна сънливост и вярваха, че те са нащрек непосредствено преди събитието. Съобщава се, че някои от тези събития се срещат до една година след започване на лечението.
Сънливост was reported in 2% of patients taking entacapone и 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for сънливост or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge сънливост or sleepiness until directly questioned about сънливост or sleepiness during specific activities. Patients who have already experienced somnolence и/or an episode of sudden sleep onset should not participate in these activities during treatment with Сталево.
Преди да започнете лечението със Stalevo посъветвайте пациентите за потенциала да развият сънливостта и конкретно да попитате за фактори, които могат да увеличат този риск, като употреба на съпътстващи седиращи лекарства и наличието на нарушения на съня. Ако пациентът развие дневна сънливост или епизоди на заспиване по време на дейности, които изискват активно участие (например разговори за хранене и т.н.), Сталево обикновено трябва да бъде прекратен [виж Доза и приложение и Предупреждения и предпазни мерки ]. If the decision is made to continue Сталево patients should be advised not to drive и to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Хипотония Orthostatic Хипотония And Syncope
Съобщенията за синкоп обикновено са по -чести при пациенти и в двете групи за лечение, които са имали предишен епизод на документирана хипотония (въпреки че епизодите на синкоп, получени от историята, сами по себе си не са документирани с жизненоважно измерване на знака). Ортостатична хипостатична хипостатика и синкоп се наблюдават при пациенти, лекувани с лекарства, които увеличават централния допаминергичен тонус, включително Stalevo.
Дискинезия
Дискинезия (неволно movements) may occur or be exacerbated at lower dosages и sooner with Сталево than with preparations containing only carbidopa и levodopa. The occurrence of dyskinesias may require dosage reduction.
При основни изпитвания разликата в разликата в лечението на дискинезия е 10%, а за Carbidopa-Levodopa плюс 200 mg entacapone. Въпреки че намаляването на дозата на леводопа може да подобри този страничен ефект, много пациенти в контролирани изпитвания продължават да изпитват чести дискинезии, въпреки намаляването на дозата им леводопа. Различията в разликата в лечението на оттеглянето на проучването за дискинезия е 1% за Карбидопа-Леводопа-Ентакапон.
Депресия и самоубийство
Всички пациенти трябва да се наблюдават внимателно за развитието на депресия със съпътстващи самоубийствени тенденции. Пациентите с минали или настоящи психози трябва да се лекуват с повишено внимание.
Халюцинации и/или психотично поведение
Допаминергичната терапия при пациенти с болест на Паркинсон е свързана с халюцинации. Халюцинациите доведоха до прекратяване на лекарството и преждевременно оттегляне от клинични изпитвания при 0,8% и 0% от пациентите, лекувани съответно с Carbidopa levodopa entacapone и Carbidopa levodopa. Халюцинациите доведоха до хоспитализация при 1,0% и 0,3% от пациентите в групите Carbidopa Levodopa Entacapone и Carbidopa Levodopa съответно. Агитацията е възникнала при 1% от пациентите, лекувани с Carbidopa levodopa entacapone и 0% лекувани с Carbidopa levodopa.
Импулсно контрол и/или натрапчиво поведение
Докладите за постмаркетиране предполагат, че пациентите, лекувани с лекарства против Паркинсон, могат да изпитат интензивни призиви за залагане на повишени сексуални подтици интензивни подтици да харчат пари неконтролируемо и други интензивни подтици. Пациентите може да не са в състояние да контролират тези пориви, докато приемат едно или повече от лекарствата, които обикновено се използват за лечение на болестта на Паркинсон и които увеличават централния допаминергичен тон, включително ентакапон, взет с леводопа и Карбидопа. В някои случаи, въпреки че не се съобщава, че всички тези призиви са спрели, когато дозата анти-Паркинсонови лекарства е намалена или прекратена. Тъй като пациентите може да не разпознават това поведение като ненормално, за предписанията е важно да питат конкретно пациентите или техните грижи за развитието на нови или увеличени хазартни игри притиска сексуалните подтиквания неконтролирани разходи или други подтици, докато се лекуват с ентакапон. Physicians should consider dose reduction or stopping Stalevo if a patient develops such urges while taking Stalevo [see Доза и приложение Предупреждения и предпазни мерки ].
Изтеглена хиперпирексия и объркване
Съобщава се за случаи на хиперпирексия и объркване, наподобяващи невролептичен злокачествен синдром (NMS) във връзка с намаляване на дозата или изтегляне на терапия с Carbidopa levodopa и ентакапон. Въпреки това в някои случаи се съобщават за хиперпирексия и объркване след започване на лечение с ентакапон. Хиперпирексията и объркването са рядкост, но те могат да бъдат животозастрашаващи с различни характеристики, включително хиперпирексия/треска/хипертермия мускулна твърдост неволни движения Променени съзнание/Психичен статус Промени делириум Автономна дисфункция Тахикардия Тахипнея Сутинг Хипер-или Хипотония и анормална лаборатория (напр Миоглобинурия и повишен серумен миоглобин).
Ако пациентът трябва да прекрати или намали дневната си доза Stalevo, дозата трябва да се намалява бавно с надзор от доставчик на здравни грижи [виж Доза и приложение ]. Specific methods for tapering entacapone have not been systematically evaluated.
Диария And Colitis
В клинични изпитвания на диария на ентакапон се развива при 60 от 603 (NULL,0%) и 16 от 400 (NULL,0%) от пациентите, лекувани с 200 mg ентакапон или плацебо в комбинация с инхибитор на леводопа и DOPA декарбоксилаза. При пациенти, лекувани с диария на ентакапон, като цяло е лека до умерена тежест (NULL,6%), но се счита за тежко при 1,3%. Диарията доведе до оттегляне при 10 от 603 (NULL,7%) пациенти 7 (NULL,2%) с лека и умерена диария и 3 (NULL,5%) с тежка диария. Диария обикновено се разрешава след прекратяване на ентакапона. Двама пациенти с диария бяха хоспитализирани. Обикновено диарията се представя в рамките на 4 до 12 седмици след стартирането на Entacapone, но може да изглежда още през първата седмица и още толкова месеци след започване на лечението. Диарията може да бъде свързана с дехидратация на отслабване и хипокалиемия.
Опитът с постмаркетинг показа, че диарията може да е знак за индуциран от лекарства микроскопичен колит, предимно лимфоцитен колит. В тези случаи диарията обикновено е умерена до тежко водниста и нелична в моменти, свързани с загуба на тегло и хипокалиемия на дехидратация на корема. В по-голямата част от случаите диарията и други симптоми, свързани с колит, са разрешени или значително подобрени при спиране на лечението с ентакапон. При някои пациенти с биопсия потвърждава, че диарията на колит е разрешена или значително се е подобрила след прекратяване на ентакапона, но се е повторно след оттегляне с ентакапон.
Ако се подозира, че продължителната диария е свързана със Сталево, лекарството трябва да бъде прекратено и да се разгледа подходяща медицинска терапия. Ако причината за продължителна диария остава неясна или продължава след спиране на ентакапон, тогава трябва да се вземат предвид допълнителни диагностични изследвания, включително колоноскопия и биопсии.
Рабдомиолиза
Съобщава се за случаи на тежка рабдомиолиза с ентакапон, когато се използват в комбинация с Карбидопа и Леводопа. Тежката продължителна двигателна активност, включително дискинезия, евентуално може да отчита рабдомиолиза. Повечето от случаите се проявяват от миалгия и повишени стойности на креатин фосфокиназа (CPK) и миоглобин. Някои от реакциите също включваха треска и/или промяна на съзнанието. Възможно е също така рабдомиолизата да е резултат от синдрома, описан в хиперпирексията и объркване на изтеглянето [виж Предупреждения и предпазни мерки ].
Взаимодействие с лекарства, метаболизирани от COMT
Лекарствата, за които се знае, че са метаболизирани от COMT, като изопротеренол епинефрин норепинефрин допамин добутамин алфа-метилдопа апоморфин изофинин, независимо от начина на прилагане (включително вдишването им.
Фиброзни усложнения
При някои пациенти са съобщени случаи на ретроперитонеални фиброза белодробни инфилтрати плеврално излив и плеврален удебелен механизъм, лекувани с допаминергични средства, получени от ерго. Тези усложнения могат да разрешат, когато лекарството е прекратено, но пълната резолюция не винаги се случва. Въпреки че тези нежелани реакции могат да бъдат свързани с ерголиновата структура на тези съединения, възможна причинно -следствена роля на лекарства, получени от нерготи (например entacapone levodopa), които увеличават допаминергичната активност. Очакваната честота на фиброзни усложнения е толкова ниска, че дори ако ентакапонът е причинил тези усложнения със скорости, подобни на тези, които се дължат на други допаминергични терапии, е малко вероятно той да бъде открит в кохорта с размера, изложен на ентеракапон по време на клиничното му развитие. Четири случая на белодробна фиброза са съобщени по време на клинично развитие на ентакапон; 3 от тези пациенти също са лекувани с перголид и 1 с бромокриптин. Продължителността на лечението с ентакапон варира от 7 месеца до 17 месеца.
Пептична язва болест
Както при лечението на леводопа със сталево може да увеличи възможността за горен стомашно -чревен кръвоизлив при пациенти с анамнеза за пептична язва.
Чернодробно увреждане
Пациентите с чернодробно увреждане трябва да се лекуват с повишено внимание [виж Клинична фармакология ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Лабораторни тестове
Аномалиите при лабораторни тестове могат да включват повишаване на тестовете за чернодробна функция като алкална фосфатаза SGOT (AST) SGPT (ALT) млечна дехидрогеназа и билирубин. Аномалии в кръвта урея Съобщава се и за тест за азот и положителен Coombs. Обикновено нивата на азотния креатинин от урея в кръвта са по -ниски по време на прилагане на сталево, отколкото при леводопа.
Сталево may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
Трябва да се внимава при интерпретиране на нивата на плазмата и урината на катехоламини и техните метаболити при пациенти на терапия на Карбидопа/Леводопа.
Информация за консултирането на пациентите
Заспиване по време на ежедневни дейности и сънливост
Посъветвайте се с пациентите за потенциала за успокояващи ефекти, свързани със Сталево, включително сънливост и възможността за заспиване, докато се занимават с ежедневни дейности. Тъй като сънливостта може да бъде честа нежелана реакция с потенциално сериозни последици, които пациентите не трябва да управляват моторно превозно средство, работещи с тежки машини или да се занимават с други потенциално опасни дейности, докато не придобият достатъчен опит със Сталево, за да се определи дали това се отразява или не за тяхното психическо и/или двигателните характеристики [виж или не се отразява [вижте неблагоприятно [виж [виж Предупреждения и предпазни мерки ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Посъветвайте се с пациентите да разговарят със своите здравни предписания, преди да приемат лекарства за успокояване на алкохол или други депресанти на ЦНС (напр. Бензодиазепини антипсихотични антидепресанти и т.н.) поради възможните адитивни ефекти в комбинация със Сталево.
Хипотония Orthostatic Хипотония And Syncope
Посъветвайте пациентите, че те могат да развият симптоматична (или асимптоматична) постурална (ортостатична) хипотония или неортостатична хипотония, като същевременно приемат сталево. Хипотонията/ортостатичната хипотония може да се появи по -често по време на първоначалната терапия. Пациентите не трябва да се издигат бързо след седене или лежат, особено ако са го правили за продължителни периоди и особено при започване на лечение със Сталево.
Консултирайте пациентите за потенциала за синкоп при пациенти, използващи допаминови агонисти. Поради тази причина информирайте пациентите за възможността за синкоп, докато приемате Сталево [виж Предупреждения и предпазни мерки ].
Дискинезияs
Информирайте пациентите, че Сталево може да причини и/или изостря съществуващите дискинезии [виж Предупреждения и предпазни мерки ].
Халюцинации и/или психотично поведение
Информирайте пациентите, че халюцинациите и друго психотично поведение могат да възникнат по време на приемане на Сталево [виж Предупреждения и предпазни мерки ].
Импулсно контрол и/или натрапчиво поведение
Посъветвайте се с пациентите, че могат да изпитат импулсен контрол и/или натрапчиво поведение, като същевременно приемат едно или повече лекарства, използвани за лечение на болестта на Паркинсон, включително Сталево. Попитайте пациентите за развитието на нови или засилени хазартни призиви за сексуални призиви Позиони за неконтролирани разходи или други интензивни подтици, докато се лекуват със Сталево. Посъветвайте се с пациентите да информират своя лекар или доставчик на здравни грижи, ако изпитват нови или увеличени хазартни призиви за повишени сексуални подтици или други интензивни подтици, докато приемат Сталево. Лекарите трябва да обмислят намаляване на дозата или спиране на лекарствата, ако пациентът развие такива пориви, докато приема Сталево [виж Предупреждения и предпазни мерки ].
Изтеглена хиперпирексия и объркване
Посъветвайте се с пациентите, че те могат да развият треска и объркване като част от синдром, наподобяващ НМ и евентуално с други клинични характеристики (например мускулна твърдост Автономна дисфункция хипер- или хипотония и т.н.). Този синдром на треска и объркване може да се появи особено с намаляване на дозата или изтегляне на Сталево, но може да се развие и след започване на лечението. Посъветвайте пациентите да се свържат с доставчика на здравни грижи, ако желаят да преустановят или намалят дозата на Сталево и да се свържат с доставчик на здравни грижи, ако развият треска и объркване [виж Предупреждения и предпазни мерки ].
Диария And Colitis
Информирайте пациентите, че диарията може да възникне при Сталево и може да има забавено начало. Понякога продължителната диария може да бъде причинена от колит (възпаление на дебелото черво). Пациентите с диария трябва да пият течности, за да поддържат адекватна хидратация и да наблюдават отслабване. Ако диарията, свързана със Сталево, е продължително прекратяване на лекарството, се очаква лекарството да доведе до разрешаване. Ако диарията продължава след спиране на Сталево може да се наложи допълнителни диагностични изследвания. В някои случаи диарията може да бъде свързана с колит [виж Предупреждения и предпазни мерки ].
Рабдомиолиза
Посъветвайте се с пациентите, че могат да развият рабдомиолиза и миалгия, ако изпитват продължителна двигателна активност, включително дискинезия. Това събитие може също да бъде свързано с треска и объркване [виж Предупреждения и предпазни мерки ].
Гадене And Повръщане
Информирайте пациентите, че Сталево може да причини гадене и повръщане може да се появи по -често по време на първоначалната терапия и може да изисква корекция на дозата.
Инструкции за употреба
Инструктирайте пациентите да приемат Сталево само както е предписано. Инструктирайте пациентите да приемат само един таблет Stalevo при всеки интервал на дозиране. Инструктирайте пациентите да не приемат множество таблетки или допълнителни части от таблетки, за да постигнат по -висока доза леводопа. Посъветвайте пациентите да не разделят смачкване или да дъвчат Сталево.
Информирайте пациента, че Stalevo е формулировка на Carbidopa/Levodopa, комбинирана с Entacapone, която е предназначена да започне освобождаване на съставки в рамките на 30 минути след поглъщането. Важно е Stalevo да се приема на редовни интервали според графика, очертан от лекаря. Внимавайте пациентът да не променя предписания режим на дозиране и да не добавя допълнителни антипаркинсонски лекарства, включително други препарати на Carbidopa/Levodopa, без първо да се консултирате с лекаря.
Съветвайте пациентите, че в края на интервала на дозиране се появяват епизоди (износване на лекарствен ефект), но по всяко време могат да възникнат непредсказуеми епизоди. Посъветвайте се на пациента да уведоми доставчик на здравни грижи за възможни корекции на лечението, ако такъв отговор създава проблем с ежедневието на пациента.
Посъветвайте се пациентите, че тъмно оцветяване (червено кафяво или черно) може да се появи в урината на слюнката или потта след приемане на Сталево. Въпреки че цветът изглежда клинично незначителни дрехи, може да се обезцвете.
Посъветвайте пациентите, че промяна в диетата на храни с високо съдържание на протеин може да забави абсорбцията на леводопа. Прекомерната киселинност също забавя изпразването на стомаха, като по този начин забавя абсорбцията на леводопа. Железните соли (като например в мулти-витамин таблетки) също могат да намалят ефективността на Stalevo.
Бременност
Инструктирайте пациентите да уведомят своя доставчик на здравни грижи, ако забременеят или възнамеряват да забременеят по време на терапията [виж Използване в конкретни популации ].
Лактация
Инструктирайте пациентите да уведомят своя доставчик на здравни грижи, ако възнамеряват да кърмят или кърмят бебе [виж Използване в конкретни популации ].
Неклинична токсикология
Канцерогенеза мутагенеза Нарушаване на плодовитостта
Карциногенеза
При плъхове пероралното приложение на Карбидопа-Леводопа в продължение на 2 години доведе до никакви доказателства за канцерогенност при дози приблизително 2 пъти (Карбидопа) -4 пъти (Леводопа) максималната препоръчителна човешка доза (MRHD).
Двугодишните канцерогенни изследвания на ентакапон са проведени при мишки и плъхове. При мишки не се наблюдава увеличаване на туморите при перорални дози от 100 200 и 400 mg/kg/ден. При най -високата доза тествани плазмени експозиции (AUC) са 4 пъти по -високи от тези при хората при максимално препоръчителната дневна доза (MRDD) от 1600 mg. При плъхове, прилагани перорални дози от 20 90 или 400 mg/kg/ден, се наблюдава повишена честота на бъбречните тръбни аденоми и карциноми при мъже при най -високата тествана доза. Плазмените AUC при по -високата доза, които не са свързани с повишени бъбречни тумори (90 mg/kg/ден), са приблизително 5 пъти по -големи от тези при хората при MRDD на ентакапон.
Канцерогенният потенциал на ентакапон, прилаган в комбинация с Карбидопа-Леводопа, не е оценен.
Мутагенеза
Карбидопа е мутагенна в in vitro бактериалната обратна мутация (AMES) в присъствието и отсъствието на метаболитна активация и в in vitro миши лимфом тимидин киназа (TK) при липса на метаболитна активация. Карбидопа е отрицателен при in vivo миши микронуклеус.
Entacapone was mutagenic и clastogenic in the in vitro mouse lymphoma tk assay in the presence и absence of metabolic activation и was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapone either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus и in the Ames assays.
Увреждане на плодовитостта
В репродукционните проучвания не са открити ефекти върху плодовитостта при плъхове, получаващи Карбидопа-Леводопа при дози приблизително 2 пъти (Карбидопа) -4 пъти (Леводопа) MRHD.
При плъхове, лекувани перорално с ентакапон (до 700 mg/kg/ден), не са наблюдавани ефекти върху плодовитостта или общите репродуктивни показатели. Плазмените експозиции (AUC) при най -високата тествана доза са приблизително 30 пъти по -голямо от това при хората при MRHD на Entacapone. Забавеното чифтосване беше очевидно при жените при най -високата тествана доза.
Използване в конкретни популации
Бременност
Обобщение на риска
Няма адекватни данни за риска от развитие, свързани с използването на Сталево при бременни жени. При животните прилагането на Карбидопа-Леводопа или ентакапон по време на бременност се свързва с токсичност за развитие, включително повишени случаи на зомални малформации на плода (виж Данни ). Прогнозният фонов риск от големи вродени дефекти и спонтанен аборт в посоченото население не е известен. В общото население на САЩ прогнозните фонови рискове от големи вродени дефекти и спонтанен аборт в клинично признатите бременности са съответно от 2 до 4% и 15 до 20%.
Данни
Данни за животните
In nonclinical studies in which carbidopa-levodopa was administered to pregnant animals increased incidences of visceral and skeletal malformations were observed in rabbits at all doses and ratios of carbidopa-levodopa tested which ranged from 10 times (carbidopa)-5 times (levodopa) to 20 times (carbidopa)-10 times (levodopa) the maximum recommended human dose (MRHD) от 1600 mg/ден. При плъхове се наблюдава намаление на броя на живите кученца, доставени от язовири, получаващи приблизително два пъти (Carbidopa)-пет пъти (Levodopa) MRHD през цялата органогенеза. Не са наблюдавани ефекти върху честотите на малформация при мишки, получаващи до 20 пъти по-голямо от MRHD на Карбидопа-Леводопа.
В ембрио-феталните проучвания за развитие на ентакапон бременни животни са получавали дози до 1000 mg/kg/ден (плъхове) или 300 mg/kg/ден (зайци) по време на органогенезата. Повишените случаи на вариациите на плода са очевидни при носилки от плъхове, лекувани с най -висока доза при липса на явни признаци на майчината токсичност. Експозицията на плазмата на майката (AUC), свързана с тази доза, е приблизително 34 пъти по -голямо от това при хората при MRHD. Повишени честоти на аборти и късни/общи резорпи и намалени тегла на плода са наблюдавани при носителите на зайци, лекувани с токсични дози от 100 mg/kg/ден (плазмени AUC, по -малко от тази при хора при MRHD) или по -голяма. В тези проучвания няма увеличение на степента на малформация.
When entacapone was administered to female rats prior to mating and during early gestation an increased incidence of fetal eye anomalies (macrophthalmia microphthalmia anophthalmia) was observed in the litters of dams treated with doses of 160 mg/kg/day (plasma AUCs seven times that in humans at the MRHD) or greater in the absence of maternal toxicity. Прилагането на до 700 mg/kg/ден (плазмен AUCs 28 пъти по -голям от хората при MRHD) на плъхове по време на последната част на бременността и по време на лактация не доведе до доказателство за нарушаване на развитието в потомството.
Лактация
Обобщение на риска
Леводопа е открит в човешко мляко след прилагане на Карбидопа-Леводопа. Няма данни за наличието на ентакапон или карбидопа в човешкото мляко ефектите на леводопа Карбидопа или ентакапон върху кърменото бебе или ефектите върху производството на мляко. Въпреки това може да възникне инхибиране на лактацията, тъй като леводопа намалява секрецията на пролактин [виж Клинична фармакология ]. Карбидопа и entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone и/or metabolites in milk up to 2 to 3 times that in plasma. The developmental и health benefits of breastfeeding should be considered along with the mother's clinical need for Сталево и any potential adverse effects on the breastfed infant from Сталево or from the underlying maternal condition.
Педиатрична употреба
Безопасността и ефективността при педиатрични пациенти не са установени.
Гериатрична употреба
От общия брой на пациентите в клиничните проучвания на Stalevo 43,8% са били на 65 години и повече, докато 7,2% са били на 75 години и повече. No overall differences in safety or effectiveness were observed between these subjects and younger subjects and other reported clinical experience has not identified differences in responses between the elderly and younger patients; Въпреки това по -голямата чувствителност на някои по -възрастни индивиди не може да бъде изключена.
Сталево tablets have not been studied in Болест на Паркинсон patients or in healthy volunteers older than 75 years [see Клинична фармакология ].
Бъбречно увреждане
Бъбречното увреждане не влияе на фармакокинетиката на ентакапона. Няма проучвания за фармакокинетиката на Леводопа и Карбидопа при пациенти с бъбречно увреждане [виж Клинична фармакология ].
Чернодробно увреждане Or Biliary Obstruction
Няма проучвания за фармакокинетиката на Карбидопа и Леводопа при пациенти с чернодробно увреждане. Stalevo should be administered cautiously to patients with biliary obstruction or hepatic disease since biliary excretion appears to be the major route of excretion of entacapone and hepatic impairment had a significant effect on the pharmacokinetics of entacapone when 200 mg entacapone was administered alone [see Клинична фармакология ].
Информация за предозиране за Сталево
Признаци и симптоми на предозиране
Има много малко случаи на предозиране с Levodopa, докладвани в публикуваната литература. Въз основа на наличната информация може да се очаква острите симптоми на предозиране на леводопа и DOPA декарбоксилаза да възникнат от допаминергичната свръхстимулация. Дози от няколко грама могат да доведат до нарушения на ЦНС с нарастваща вероятност от сърдечно -съдови смущения (например хипотония тахикардия) и по -тежки психиатрични проблеми при по -високи дози. Изолиран доклад за рабдомиолиза и друг от преходна бъбречна недостатъчност предполагат, че предозиране на леводопа може да доведе до системни усложнения, вторични за допаминергичната свръхстимулация.
Инхибирането на COMT чрез лечение с ентакапон зависи от дозата. Масивно предозиране на ентакапон може теоретично да доведе до 100% инхибиране на COMT ензима при хора, като по този начин предотвратява о-метилирането на ендогенни и екзогенни катехоли.
При клинични изпитвания най -високата единична доза ентакапон, прилагана на хора, е била 800 mg, което води до плазмена концентрация от 14,1 mcg на ml. Най -високата дневна доза, дадена на хората, е била 2400 mg, прилагана в едно проучване като 400 mg шест пъти дневно с Carbidopa/levodopa в продължение на 14 дни при 15 пациенти на Паркинсон и в друго проучване като 800 mg три пъти дневно в продължение на 7 дни при 8 здрави доброволци. При тази дневна доза пиковите плазмени концентрации на ентакапон са средно 2,0 mcg на ml (при 45 минути в сравнение с 1,0 mcg на ml и 1,2 mcg на ml с 200 mg ентакапон на 45 минути). Болката на корема и свободните изпражнения са най -често наблюдаваните нежелани събития по време на това проучване. Ежедневните дози до 2000 mg ентакапон се прилагат като 200 mg 10 пъти дневно с Carbidopa/levodopa или Benserazide/levodopa за поне 1 година при 10 пациенти за поне 2 години при 8 пациенти и поне 3 години при 7 пациенти. Като цяло обаче клиничният опит с дневни дози над 1600 mg е ограничен.
Управление на предозиране
Препоръчва се хоспитализацията и трябва да се използват общи поддържащи мерки, заедно с незабавно стомашно промиване и многократни дози въглен във времето. Това може да ускори елиминирането на ентакапона, по -специално чрез намаляване на неговата абсорбция и реабсорбция от GI тракта. Интравенозните течности трябва да се прилагат разумно и да се поддържа адекватен дихателен път.
Респираторната кръвоносна и бъбречната функция трябва да се следи и да се използват подходящи поддържащи мерки. Електрокардиографският мониторинг трябва да бъде въведен и пациентът внимателно да се наблюдава за развитието на аритмии; Ако е необходимо, трябва да се даде подходяща антиаритмична терапия. Трябва да се вземе предвид възможността пациентът да е взел други лекарства, увеличавайки риска от лекарствени взаимодействия (особено структурирани от катехол лекарства). Към днешна дата не се съобщава за опит с диализа; Следователно стойността му при предозиране не е известна. Хемодиализата или хемоперфузията е малко вероятно да намалят нивата на ентакапон поради високото му свързване с плазмените протеини. Пиридоксинът не е ефективен при обръщане на действията на Сталево.
Противопоказания за Сталево
Сталево is contraindicated in patients:
- Приемане на неселективни инхибитори на моноамино оксидаза (MAO) (напр. Фенелзин и транзилципромин). Тези неселективни MAO инхибитори трябва да бъдат прекратени най -малко две седмици преди започване на терапия със сталево.
- С тесен ъгъл глаукома .
Клинична фармакология for Сталево
Механизъм на действие
Леводопа
Настоящите доказателства показват, че симптомите на болестта на Паркинсон са свързани с изчерпването на допамин в корпуса на стриатума. Прилагането на допамин е неефективно при лечението на болестта на Паркинсон, тъй като не преминава кръвно-мозъчната бариера. Въпреки това Levodopa метаболитният предшественик на допамин прекосява кръвно-мозъчната бариера и вероятно се превръща в допамин в мозъка. Смята се, че това е механизмът, при който Леводопа облекчава симптомите на болестта на Паркинсон.
Карбидопа
Когато се прилага леводопа перорално, той бързо се декарбоксилира до допамин в извънцеребрални тъкани, така че само малка част от дадена доза се транспортира непроменена до централната нервна система. Карбидопа инхибира декарбоксилирането на периферната леводопа, което прави повече леводопа достъпна за доставка до мозъка.
Entacapone
Entacapone is a selective и reversible inhibitor of catechol-O-methyltransferase (COMT).
Comt катализира прехвърлянето на метиловата група на S-аденозил-L-метионин към фенолната група субстрати, които съдържат катехолна структура. Физиологичните субстрати на COMT включват DOPA катехоламини (допамин норепинефрин и епинефрин) и техните хидроксилирани метаболити. Когато декарбоксилирането на леводопа се предотвратява от Carbidopa comt се превръща в основния метаболизиращ ензим за катализиране на леводопа неговия метаболизъм до 3-метокси-4-хидрокси-L-фенилаланин (3-OMD).
Фармакокинетика
Фармакокинетиката на таблетките Stalevo е проучена при здрави лица (възраст от 45 години до 75 години). Като цяло след прилагане на съответните дози Levodopa carbidopa и entacapone като Stalevo или като Carbidopa и Levodopa Product Plus Comtan (entacapone) таблетки са съпоставими средните плазмени концентрации на леводопа карбибидопа и ентакапон.
Абсорбция и разпределение
Както леводопа, така и ентакапон бързо се абсорбират и елиминират и обемът им на разпределение е умерено малък. Карбидопа се абсорбира и елиминира малко по -бавно в сравнение с леводопа и ентакапон. Съществуват съществени между- и вътрешно-индивидуални вариации в абсорбцията на леводопа карбидопа и ентакапон, особено по отношение на неговия CMAX.
Ефектът от храна на таблета Stalevo не е оценен. Тъй като леводопа се конкурира с определени аминокиселини за транспортиране през стената на червата, абсорбцията на леводопа може да бъде нарушено при някои пациенти след хранене с високо съдържание на протеини. Храните, богати на големи неутрални аминокиселини, могат да забавят и намалят абсорбцията на леводопа [виж Информация за консултирането на пациентите ].
Леводопа
Фармакокинетичните свойства на леводопа след прилагането на таблетки с една доза Stalevo (Carbidopa Levodopa и Entacapone) са обобщени в таблица 3.
Таблица 3: Фармакокинетични характеристики на леводопа с различна якост на таблета на Сталево (средно ± SD)
| Сила на таблета | AUC0 -∞ (Нанограма • H чрез ML) | CMAX (Нанограма на ml) | Tmax (H) |
| 12,5 mg на 50 mg на 200 mg | 1040 ± 314 | 470 ± 154 | 1.1 ± 0.5 |
| 25 mg на 100 mg на 200 mg | 2910 ± 715 | 975 ± 247 | 1,4 ± 0,6 |
| 37,5 mg на 150 mg на 200 mg | 3770 ± 1120 | 1270 ± 329 | 1,5 ± 0,9 |
| 50 mg на 200 mg на 200 mg | 6115 ± 1536 | 1859 ± 455 | 1,76 ± 0,7 |
Леводопа is bound to plasma protein only to a minor extent (about 10% to 30%).
Карбидопа
След прилагането на Сталево като единична доза на здрави мъже и жени, пиковата концентрация на Карбидопа е достигната средно в рамките на 2,5 часа до 3,4 часа. Средната CMAX варира от около 40 нанограма на ml до 225 нанограма на ml, а средната AUC от 170 нанограма • H на ml до 1200 нанограма • H на ml с различни сталево якост, осигуряваща 12,5 mg 25 mg 37,5 mg или 50 mg карбидопа.
Карбидопа is approximately 36% bound to plasma protein.
Entacapone
След прилагане на Сталево като единична доза на здрави мъже и жени, пиковата концентрация на ентакапон в плазмата е достигната средно в рамките на 0,8 часа до 1,2 часа. Средната CMAX на ентакапон е около 1200 нанограма на ml до 1500 нанограма на ml и AUC 1250 нанограма • H на ml до 1750 Nanagram • H на ml след прилагане на различни силови сталево, всички осигуряващи 200 mg ентакапон.
Свързването на плазмения протеин на ентакапон е 98% в диапазона на концентрация от 0,4 mcg на ml до 50 mcg на ml. Entacapone се свързва главно със серумен албумин.
Метаболизъм и елиминиране
Леводопа
Елиминационният полуживот на леводопа активната част на антипаркинсоновата активност е 1,7 часа (диапазон от 1,1 часа до 3,2 часа).
Леводопа is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) и O-methylation by COMT.
Карбидопа
Елиминационният полуживот на Карбидопа беше средно от 1,6 часа до 2 часа (диапазон от 0,7 часа до 4,0 часа).
Карбидопа is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid и α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapone
Елиминационният полуживот на ентакапон беше средно от 0,8 часа до 1 час (NULL,3 час до 4,5 часа).
Entacapone is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapone и the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent и 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 C-белязана доза на ентакапон 10% от белязания родител и метаболит се отделя в урина и 90% в изпражненията.
Поради краткия елиминационен полуживот не се появява истинско натрупване на леводопа или ентакапон, когато те се прилагат многократно.
Бъбречно увреждане
Entacapone
Фармакокинетиката на ентакапон е изследвана след единична доза от 200 mg ентакапон при лица с нормална умерена и силно нарушена бъбречни функции без инхибитор на леводопа и DOPA декарбоксилаза. Не са открити значителни ефекти на бъбречната функция върху фармакокинетиката на ентакапона.
Леводопа And carbidopa
Няма проучвания за фармакокинетиката на Леводопа и Карбидопа при пациенти с бъбречно увреждане.
Чернодробно увреждане
Entacapone
Чернодробното увреждане оказва значително влияние върху фармакокинетиката на ентакапона, когато 200 mg ентакапон се прилага самостоятелно. Единична доза от 200 mg ентакапон без леводопа и инхибитор на DOPA декарбоксилаза коадминацията показва приблизително 2 пъти по-високи стойности на AUC и CMAX при пациенти с анамнеза за алкохолизъм и чернодробно увреждане (n = 10) в сравнение с нормалните лица (n = 10). Всички пациенти са имали чернодробна цироза, доказана от биопсия, причинена от алкохол. Според детския преден клас 7 пациенти с чернодробно заболяване са имали леко чернодробно увреждане, а 3 пациенти са имали умерено чернодробно увреждане. Тъй като само около 10% от дозата на ентакапон се отделя в урината като родителско съединение и конюгираната глюкуронидна жлъчна екскреция изглежда е основният път на екскреция на това лекарство. Stalevo трябва да се прилага внимателно на пациенти с жлъчна обструкция или чернодробна болест.
Леводопа And Карбидопа
Няма проучвания за фармакокинетиката на Леводопа и Карбидопа при пациенти с чернодробно увреждане.
Гериатрична употреба
В фармакокинетичните проучвания, проведени при здрави доброволци след единична доза карбидопа-леводопа и ентакапон (като сталево или като отделни таблетки Карбидопа/Леводопа и Комтан):
Леводопа
AUC на леводопа е значително (средно с 10% до 20%) по -висок при възрастни хора (60 години до 75 години) от по -младите лица (45 години до 60 години). Няма значима разлика в CMAX на леводопа между по -млади (45 години до 60 години) и възрастни субекти (60 години до 75 години).
Карбидопа
Няма значителна разлика в CMAX и AUC на Карбидопа между по -млади (45 години до 60 години) и възрастни субекти (60 години до 75 години).
Entacapone
AUC на Entacapone е значително (средно 15%) по -висок при възрастни хора (60 години до 75 години), отколкото по -младите субекти (45 години до 60 години). Няма значителна разлика в CMAX на ентакапона между по -млади (45 години до 60 години) и възрастни субекти (60 години до 75 години).
Пол
Фармакокинетика following a single dose of carbidopa levodopa и entacapone together either as Сталево or as separate carbidopa/levodopa и Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Леводопа
Плазмената експозиция (AUC и CMAX) на леводопа е значително по -висока при жените, отколкото мъжете (средно 40% за AUC и 30% за CMAX). Тези разлики се обясняват предимно с телесното тегло. Друга публикувана литература показа значителен ефект на пола (по -високи концентрации при жените) дори след корекция на телесното тегло.
Карбидопа
Няма разлика между половете във фармакокинетиката на Карбидопа.
Entacapone
Няма разлика между половете във фармакокинетиката на ентакапона.
Проучвания за взаимодействие с лекарства
Лекарство, метаболизирано от comt
Когато единична доза от ентакапон от 400 mg се дава заедно с интравенозен изопналин (изопротеренол) и епинефрин без съвместно ограден леводопа и инхибитор на DOPA декарбоксилаза, общите средни максимални промени в сърдечната честота по време на инфузия са съответно 50% и 80% по -високи, отколкото с плацебо за изопрениден и епинефрин.
Лекарствата, за които се знае, че са метаболизирани от COMT, трябва да се прилагат с повишено внимание при пациенти, получаващи ентакапон, независимо от начина на приложение [виж Лекарствени взаимодействия ].
Лекарствата, метаболизирани чрез CYP2C9
Поради афинитета му към CYP2C9 in vitro entacapone може потенциално да попречи на лекарствените продукти с метаболизъм, зависим от този изоензим. В проучване за взаимодействие при здрави доброволци entacapone увеличава AUC на R-Warfarin средно с 18%, а стойностите на INR се увеличават средно с 13% [виж Лекарствени взаимодействия ].
Нива на хормони
От съставките в Сталево Леводопа е известно, че потиска секрецията на пролактин и се увеличава растежен хормон нива.
Клинични изследвания
Ефективността на ентакапон като допълнение към леводопа при лечението на болестта на Паркинсон е установена в три 24-седмични многоцентрови рандомизирани двойно-слепи плацебо-контролирани изследвания при пациенти с болест на Паркинсон. В 2 от тези проучвания (проучвания 1 и 2) болестта на пациентите се колебае, т.е. се характеризира с документирани периоди на ON (периоди на сравнително добро функциониране) и извън (периоди на сравнително лошо функциониране), въпреки оптималната терапия на леводопа. Имаше и период на оттегляне след 6 месеца лечение. В третото изпитване на пациентите не се изисква да изпитват колебания. Преди контролираната част от тези изследвания пациентите са стабилизирани на леводопа в продължение на 2 седмици до 4 седмици.
Има ограничен опит в използването на ентакапон при пациенти, които не изпитват колебания.
В проучвания 1 и 2 пациенти са рандомизирани да получават плацебо или ентакапон 200 mg, прилагани едновременно с всяка доза Карбидопа/Леводопа (до 10 пъти дневно, но пациентите са средно 4 дози до 6 дози на ден). Двойното сляпо част от двете проучвания беше дълга 6 месеца. Пациентите периодично регистрираха времето, прекарано в държави ON и OFF в дневните дневници през целия период на изпитването. В едно проучване, проведено в скандинавските страни, основната мярка за резултат е общото средно време, прекарано в държавата ON по време на 18 -часов дневник, регистриран (от 6:00 до полунощ). В другото проучване основната мярка за резултат е делът на будното време, прекарано над 24 часа в държавата ON.
В допълнение към мярката за първичен резултат, времето, прекарано в OFF държавата, е оценено и пациентите са оценени и чрез подчасти на скалата за оценка на болестта на Съединените Паркинсон (UPDRS) често използвана скала за оценка на многоцелни точки, предназначена за оценка на ментацията (част I) дейности на ежедневния живот (част II) двигателна функция (част III) Усложнения на терапията (част IV) и стагнадирането на заболяването (част V); Глобалната оценка на изследовател и пациент от клинично състояние 7-точкова субективна скала, предназначена да оцени глобалното функциониране при болестта на Паркинсон; и промяната в ежедневната доза Карбидопа/Леводопа.
За какво се използва калиев глюконат за
В проучване 1 171 пациентите са рандомизирани в 16 центъра във Финландия Норвегия Швеция и Дания (проучване 1) всички от които са получили съпътстваща леводопа плюс инхибитор на DOPA декарбоксилаза (или Carbidopa/Levodopa, или Benserazide/Levodopa). В проучване 2 205 пациенти са рандомизирани в 17 центъра в Северна Америка (САЩ и Канада); Всички пациенти са получили съпътстваща Карбидопа/Леводопа.
Следните таблици (Таблица 4 и Таблица 5) показват резултатите от тези две проучвания:
Таблица 4: Резултати от ефикасността на проучване 1
| Основна мярка от домашния дневник (от 18-часов ден на дневника) | |||
| Базова линия | Промяна от изходното ниво на 6 -и месец* | P-стойност срещу плацебо | |
| Часове будно време на | |||
| Плацебо | 9.2 | 0.1 | - |
| Entacapone | 9.3 | 1.5 | по -малко от 0,001 |
| Продължителност на времето след първата доза (HRS) | |||
| Плацебо | 2.2 | 0.0 | - |
| Entacapone | 2.1 | 0.2 | по -малко от 0,05 |
| Вторични мерки от домашния дневник (от 18-часов ден на дневника) † | |||
| Часове на събуждане на почивка | |||
| Плацебо | 5.3 | 0.0 | - |
| Entacapone | 5.5 | -1.3 | по -малко от 0,001 |
| Пропорция на будното време на ‡ (%) | |||
| Плацебо | 63.8 | 0.6 | - |
| Entacapone | 62.7 | 9.3 | по -малко от 0,001 |
| Леводопа Total Daily Dose (mg) | |||
| Плацебо | 705 | 14 | - |
| Entacapone | 701 | -87 | по -малко от 0,001 |
| Честота на ежедневните приема на леводопа | |||
| Плацебо | 6.1 | 0.1 | - |
| Entacapone | 6.2 | - 0,4 | по -малко от 0,001 |
| Други вторични мерки | |||
| Базова линия | Промяна от изходното ниво на 6 месец | P-стойност срещу плацебо | |
| Глобалният (като цяло) % е подобрен § | |||
| Плацебо | - | 28 | - |
| Entacapone | - | 56 | по -малко от 0,01 |
| Глобалният (като цяло) % е подобрен § | |||
| Плацебо | - | 22 | - |
| Entacapone | - | 39 | N.S.¶ |
| UPDRS общо | |||
| Плацебо | 37.4 | -1.1 | - |
| Entacapone | 38.5 | -4.8 | по -малко от 0,01 |
| UPDRS двигател | |||
| Плацебо | 24.6 | -0.7 | - |
| Entacapone | 25.5 | -3.3 | по -малко от 0,05 |
| UPDRS ADL | |||
| Плацебо | 11.0 | -0.4 | - |
| Entacapone | 11.2 | -1.8 | по -малко от 0,05 |
| *Средно; Стойностите на месец 6 представляват средната стойност от 8 16 и 24 седмици по мярка за изход, дефинирана от протокол. † P Стойности за вторични мерки са номинални P стойности без никаква корекция за множеството. ‡ Не е крайна точка за това проучване, а първична крайна точка в проучването в Северна Америка. § Най -малко една категория се променя в крайната точка. ¶ Не значим. |
Таблица 5: Резултати от ефикасността на проучване 2
| Основна мярка от домашния дневник (за 24-часов ден на дневника) | |||
| Базова линия | Промяна от изходното ниво на 6 -и месец* | P-стойност срещу плацебо | |
| Процент от будно време на | |||
| Плацебо | 60.8 | 2.0 | - |
| Entacapone | 60.0 | 6.7 | по -малко от 0,05 |
| Вторични мерки от домашния дневник (за 24-часов ден на дневника) † | |||
| Часове на събуждане на почивка | |||
| Плацебо | 6.6 | -0.3 | - |
| Entacapone | 6.8 | -1.2 | по -малко от 0,01 |
| Часове будно време на | |||
| Плацебо | 10.3 | 0.4 | - |
| Entacapone | 10.2 | 1.0 | N.S. ‡ |
| Леводопа Total Daily Dose (mg) | |||
| Плацебо | 758 | 19 | - |
| Entacapone | 804 | -93 | по -малко от 0,001 |
| Честота на ежедневните приема на леводопа | |||
| Плацебо | 6.0 | 0.2 | - |
| Entacapone | 6.2 | 0.0 | N.S. ‡ ‡ ‡ |
| Други вторични мерки† | |||
| Базова линия | Промяна от изходното ниво на 6 месец | P-стойност срещу плацебо | |
| Глобалният (като цяло) % е подобрен § | |||
| Плацебо | - | 21 | - |
| Entacapone | - | 34 | по -малко от 0,05 |
| Глобалният (като цяло) % е подобрен § | |||
| Плацебо | - | 20 | - |
| Entacapone | - | 31 | по -малко от 0,05 |
| UPDRS общо¶ | |||
| Плацебо | 35.6 | 2.8 | - |
| Entacapone | 35.1 | -0.6 | по -малко от 0,05 |
| UPDRS двигател ¶ | |||
| Плацебо | 22.6 | 1.2 | - |
| Entacapone | 22.0 | -0.9 | по -малко от 0,05 |
| UPDRS ADL¶ | |||
| Плацебо | 11.7 | 1.1 | - |
| Entacapone | 11.9 | 0.0 | по -малко от 0,05 |
| *Средно; Стойностите на месец 6 представляват средната стойност от 8 16 и 24 седмици по мярка за изход, дефинирана от протокол. † P Стойности за вторични мерки са номинални P стойности без никаква корекция за множеството. ‡ Не е значително. § Най -малко една категория се променя в крайната точка. ¶Score Промяна в крайната точка, подобно на скандинавското проучване. |
Ефектите върху времето не се различават по възрастова тежест на пола тежест на тежестта на дозата на леводопа и едновременното лечение с допаминови агонисти или селегилин.
Оттегляне на entacapone
В проучване 2 рязко изтегляне на ентакапон без промяна на дозата на Карбидопа/Леводопа доведе до значително влошаване на колебанията в сравнение с плацебо. В някои случаи симптомите са малко по -лоши, отколкото при изходното ниво, но са се върнали до приблизително базова тежест в рамките на 2 седмици след увеличаването на дозата на леводопа средно с 80 mg. В проучване 1 по подобен начин се наблюдава значително влошаване на симптомите на Паркинсон след оттеглянето на ентакапон, както е оценено 2 седмици след оттеглянето на лекарството. На тази фаза симптомите са приблизително при тежестта на изхода след увеличаване на дозата на леводопа с около 50 mg.
In the third placebo-controlled trial (Study 3) a total of 301 patients were randomized in 32 centers in Germany and Austria. В това проучване, както и в останалите 2 проучвания, ентакапон 200 mg се прилага с всяка доза леводопа и инхибитор на DOPA декарбоксилаза (до 10 пъти дневно) и UPDRS части II и III и общите ежедневно навреме бяха основните мерки за ефективност. Резултатите за основните мерки, както и за някои вторични мерки са представени в таблица 6.
Таблица 6: Резултати от ефикасността на проучване 3
| Първични мерки | |||
| Базова линия | Промяна от изходното ниво на 6 месец | P-стойност срещу плацебо (LOCF) | |
| Updrsadl* | |||
| Плацебо | 12.0 | 0.5 | - |
| Entacapone | 12.4 | -0.4 | по -малко от 0,05 |
| UPDRS двигател* | |||
| Плацебо | 24.1 | 0.1 | - |
| Entacapone | 24.9 | -2.5 | по -малко от 0,05 |
| Часове будно време на (Home Diary)† | |||
| Плацебо | 10.1 | 0.5 | - |
| Entacapone | 10.2 | 1.1 | N.S. ‡ |
| Вторични мерки§ | |||
| Базова линия | Промяна от изходното ниво на 6 месец | P-стойност срещу плацебо | |
| UPDRS общо * | |||
| Плацебо | 37.7 | 0.6 | - |
| Entacapone | 39.0 | -3.4 | по -малко от 0,05 |
| Процент от будно време на (Home Diary) ** | |||
| Плацебо | 59.8 | 3.5 | - |
| Entacapone | 62.0 | 6.5 | N.S. ‡ ‡ ‡ |
| Часове на събуждане на почивка (Home Diary) | |||
| Плацебо | 6.8 | -0.6 | - |
| Entacapone | 6.3 | -1.2 | 0.07 |
| Леводопа Total Daily Dose (mg)* | |||
| Плацебо | 572 | 4 | - |
| Entacapone | 566 | -35 | N.S. |
| Честота на дневния прием на леводопа* | |||
| Плацебо | 5.6 | 0.2 | - |
| Entacapone | 5.4 | 0.0 | по -малко от 0,01 |
| Глобален (като цяло) % подобрен ¶ | |||
| Плацебо | - | 34 | - |
| Entacapone | - | 38 | N.S. ‡ |
| *Общо население; Промяна на резултата в крайната точка. † колебая на популацията с 5 дози до 10 дози; Промяна на резултата в крайната точка. ‡ Не е значително. §P Стойности за вторични мерки са номинални p стойности без никаква корекция за множеството. ¶Total население; Поне една категория се променя в крайната точка. |
Информация за пациента за Сталево
Заспиване по време на ежедневни дейности и сънливост
Посъветвайте се с пациентите за потенциала за успокояващи ефекти, свързани със Сталево, включително сънливост и възможността за заспиване, докато се занимават с ежедневни дейности. Тъй като сънливостта може да бъде честа нежелана реакция с потенциално сериозни последици, които пациентите не трябва да управляват моторно превозно средство, работещи с тежки машини или да се занимават с други потенциално опасни дейности, докато не придобият достатъчен опит със Сталево, за да се определи дали това се отразява или не за тяхното психическо и/или двигателните характеристики [виж или не се отразява [вижте неблагоприятно [виж [виж Предупреждения и предпазни мерки ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Посъветвайте се с пациентите да разговарят със своите здравни предписания, преди да приемат лекарства за успокояване на алкохол или други депресанти на ЦНС (напр. Бензодиазепини антипсихотични антидепресанти и т.н.) поради възможните адитивни ефекти в комбинация със Сталево.
Хипотония Orthostatic Хипотония And Syncope
Посъветвайте пациентите, че те могат да развият симптоматична (или асимптоматична) постурална (ортостатична) хипотония или неортостатична хипотония, като същевременно приемат сталево. Хипотонията/ортостатичната хипотония може да се появи по -често по време на първоначалната терапия. Пациентите не трябва да се издигат бързо след седене или лежат, особено ако са го правили за продължителни периоди и особено при започване на лечение със Сталево.
Консултирайте пациентите за потенциала за синкоп при пациенти, използващи допаминови агонисти. Поради тази причина информирайте пациентите за възможността за синкоп, докато приемате Сталево [виж Предупреждения и предпазни мерки ].
Дискинезияs
Информирайте пациентите, че Сталево може да причини и/или изостря съществуващите дискинезии [виж Предупреждения и предпазни мерки ].
Халюцинации и/или психотично поведение
Информирайте пациентите, че халюцинациите и друго психотично поведение могат да възникнат по време на приемане на Сталево [виж Предупреждения и предпазни мерки ].
Импулсно контрол и/или натрапчиво поведение
Посъветвайте се с пациентите, че могат да изпитат импулсен контрол и/или натрапчиво поведение, като същевременно приемат едно или повече лекарства, използвани за лечение на болестта на Паркинсон, включително Сталево. Попитайте пациентите за развитието на нови или засилени хазартни призиви за сексуални призиви Позиони за неконтролирани разходи или други интензивни подтици, докато се лекуват със Сталево. Посъветвайте се с пациентите да информират своя лекар или доставчик на здравни грижи, ако изпитват нови или увеличени хазартни призиви за повишени сексуални подтици или други интензивни подтици, докато приемат Сталево. Лекарите трябва да обмислят намаляване на дозата или спиране на лекарствата, ако пациентът развие такива пориви, докато приема Сталево [виж Предупреждения и предпазни мерки ].
Изтеглена хиперпирексия и объркване
Посъветвайте се с пациентите, че те могат да развият треска и объркване като част от синдром, наподобяващ НМ и евентуално с други клинични характеристики (например мускулна твърдост Автономна дисфункция хипер- или хипотония и т.н.). Този синдром на треска и объркване може да се появи особено с намаляване на дозата или изтегляне на Сталево, но може да се развие и след започване на лечението. Посъветвайте пациентите да се свържат с доставчика на здравни грижи, ако желаят да преустановят или намалят дозата на Сталево и да се свържат с доставчик на здравни грижи, ако развият треска и объркване [виж Предупреждения и предпазни мерки ].
Диария And Colitis
Информирайте пациентите, че диарията може да възникне при Сталево и може да има забавено начало. Понякога продължителната диария може да бъде причинена от колит (възпаление на дебелото черво). Пациентите с диария трябва да пият течности, за да поддържат адекватна хидратация и да наблюдават отслабване. Ако диарията, свързана със Сталево, е продължително прекратяване на лекарството, се очаква лекарството да доведе до разрешаване. Ако диарията продължава след спиране на Сталево може да се наложи допълнителни диагностични изследвания. В някои случаи диарията може да бъде свързана с колит [виж Предупреждения и предпазни мерки ].
Рабдомиолиза
Посъветвайте се с пациентите, че могат да развият рабдомиолиза и миалгия, ако изпитват продължителна двигателна активност, включително дискинезия. Това събитие може също да бъде свързано с треска и объркване [виж Предупреждения и предпазни мерки ].
Гадене And Повръщане
Информирайте пациентите, че Сталево може да причини гадене и повръщане може да се появи по -често по време на първоначалната терапия и може да изисква корекция на дозата.
Инструкции за употреба
Инструктирайте пациентите да приемат Сталево само както е предписано. Инструктирайте пациентите да приемат само един таблет Stalevo при всеки интервал на дозиране. Инструктирайте пациентите да не приемат множество таблетки или допълнителни части от таблетки, за да постигнат по -висока доза леводопа. Посъветвайте пациентите да не разделят смачкване или да дъвчат Сталево.
Информирайте пациента, че Stalevo е формулировка на Carbidopa/Levodopa, комбинирана с Entacapone, която е предназначена да започне освобождаване на съставки в рамките на 30 минути след поглъщането. Важно е Stalevo да се приема на редовни интервали според графика, очертан от лекаря. Внимавайте пациентът да не променя предписания режим на дозиране и да не добавя допълнителни антипаркинсонски лекарства, включително други препарати на Carbidopa/Levodopa, без първо да се консултирате с лекаря.
Съветвайте пациентите, че в края на интервала на дозиране се появяват епизоди (износване на лекарствен ефект), но по всяко време могат да възникнат непредсказуеми епизоди. Посъветвайте се на пациента да уведоми доставчик на здравни грижи за възможни корекции на лечението, ако такъв отговор създава проблем с ежедневието на пациента.
Посъветвайте се пациентите, че тъмно оцветяване (червено кафяво или черно) може да се появи в урината на слюнката или потта след приемане на Сталево. Въпреки че цветът изглежда клинично незначителни дрехи, може да се обезцвете.
Посъветвайте пациентите, че промяна в диетата на храни с високо съдържание на протеин може да забави абсорбцията на леводопа. Прекомерната киселинност също забавя изпразването на стомаха, като по този начин забавя абсорбцията на леводопа. Железните соли (като например в мулти-витамин таблетки) също могат да намалят ефективността на Stalevo.
Бременност
Инструктирайте пациентите да уведомят своя доставчик на здравни грижи, ако забременеят или възнамеряват да забременеят по време на терапията [виж Използване в конкретни популации ].
Лактация
Инструктирайте пациентите да уведомят своя доставчик на здравни грижи, ако възнамеряват да кърмят или кърмят бебе [виж Използване в конкретни популации ].
